Clear Sky Science · ar
FCHo2، وليس تالين، يمكّن التنشيط من الداخل للخارج لإنتغرين ɑvβ5 في الالتصاقات المنحنية
كيف تشعر الخلايا بشكل محيطها
أجسامنا مبنية من خلايا تلتقط محيطها باستمرار، تجذب وتدفع للتحرك أو الانقسام أو الثبات في مكانها. تكشف هذه الورقة أن الخلايا لا تقيس فقط صلابة بيئتها—بل تقرأ أيضاً شكلها. من خلال اكتشاف نظام تثبيت خاص يتنشط فقط حيث ينحني غشاء الخلية بشدة، يوضح الباحثون أن الخلايا تستخدم "أمساكات" داخلية مختلفة للأسطح المسطحة مقابل المحيطات الليفية، وهو ما يحمل دلالات هامة لتكوّن الأنسجة وانتشار السرطان.
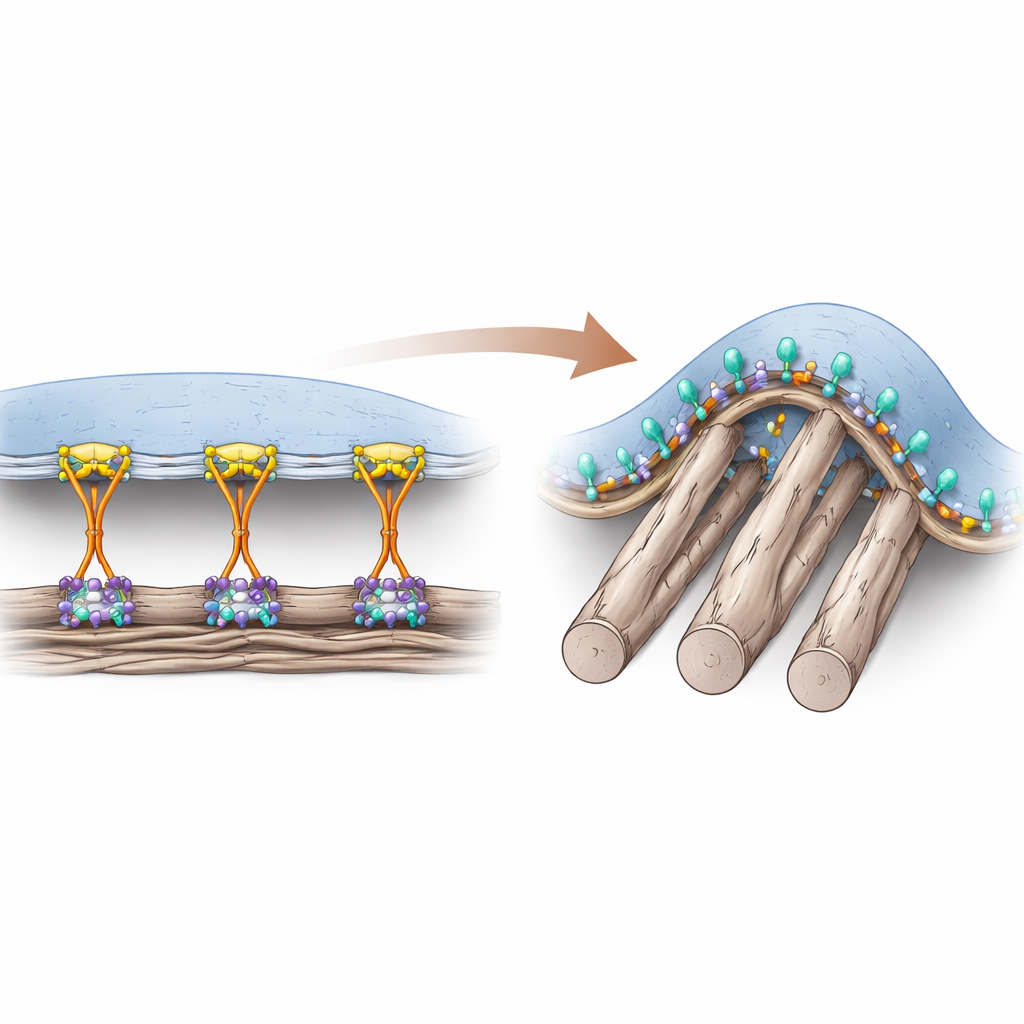
طريقتان تمسكان بهما الخلايا
تلتصق الخلايا بالمادة الغنية بالبروتين المحيطة بها عبر مستقبلات سطحية تسمى الإنتغرينات. لسنوات، اعتقد الباحثون أن بروتين مساعد اسمه تالين لا غنى عنه لتنشيط الإنتغرينات "من الداخل"، ما يمكّن الالتصاق القوي في مواقع تثبيت كلاسيكية تعرف بالالتصاقات البؤرية. تتكوّن هذه الالتصاقات أساساً على الأسطح المسطحة والصلبة وتنقل قوى سحب كبيرة عبر هيكل الخلية. ومع ذلك، في الأنسجة الحية، الكثير من الألياف المحيطة لينة واسطوانية، فتخلق نقاط اتصال منحنية لا تدعم بسهولة هذه التراكيب المحشوة بالقوى. وجد المؤلفون سابقاً نوعاً مختلفاً من التراكيب اللاصقة، يُسمى الالتصاق المنحني، الذي يظهر حيث ينحني الغشاء حول ألياف رفيعة ويعتمد على إنتغرين محدد، αvβ5.
الأمساكات المنحنية تستخدم مساعداً مختلفاً
في الدراسة الجديدة، يبين الفريق أن تالين، رغم وجوده، ليس المنشط الأساسي لإنتغرين αvβ5 في الالتصاقات المنحنية. بدل ذلك، يتولى بروتين حساس للانحناء يدعى FCHo2 هذه المهمة. باستخدام قضبان وأعمدة نانوية مصممة بدقة لثني أغشية الخلايا بطرق محكومة، لاحظوا أن αvβ5 يتجمع بقوة عند المناطق المنحنية، لكن فقط عندما يستطيع FCHo2 الارتباط بتسلسل قصير جداً—وهو موتيف HDRRE—داخل الخلية على ذيل β5. عندما يتعرض هذا الموتيف للاضطراب، يظل الإنتغرين فعالاً في الالتصاقات البؤرية لكنه لم يعد قادراً على تكوين الالتصاقات المنحنية. تثبيط FCHo2 يترك الالتصاقات البؤرية الكلاسيكية سليمة إلى حد كبير لكنه يقضي على الالتصاقات المنحنية، بينما يضعف إزالة تالين الالتصاقات البؤرية بشدة ويترك الالتصاقات المنحنية إلى حد كبير دون تأثير.
مفتاح حمض أميني واحد كمحدد للشكل
أحد الألغاز كان لماذا لا يمكن لإنتغرين قريب النسب، αvβ3، تكوين الالتصاقات المنحنية رغم تشابه ذيله الداخلي مع ذيل β5. عن طريق مبادلة المجالات بين الإنتغرينين وإدخال طفرات نقطية، حدد المؤلفون موضعاً محورياً واحداً قرب موقع ارتباط تالين: معظم إنتغرينات β تحمل حمض التربتوفان (W)، لكن β5 فريدة بوجود التيروسين (Y766). عندما استُبدل تيروسين β5 بتربتوفان، فقد الإنتغرين قدرته على المشاركة في الالتصاقات المنحنية وتصرف أكثر مثل β3، مفضّلاً الالتصاقات البؤرية فقط. التغيير المعاكس—وضع التيروسين في الكيميرا الشبيهة بـβ3—أعاد حساسية الانحناء. تجارب إضافية مع متغيرات تحاكي حالات الفسفرة أو عدم الفسفرة لهذا التيروسين تشير إلى أن التعديل الكيميائي لهذا الموقع يمكن أن يوجه الإنتغرين نحو الالتصاقات المسطحة عالية القوة أو الالتصاقات المنحنية منخفضة القوة.
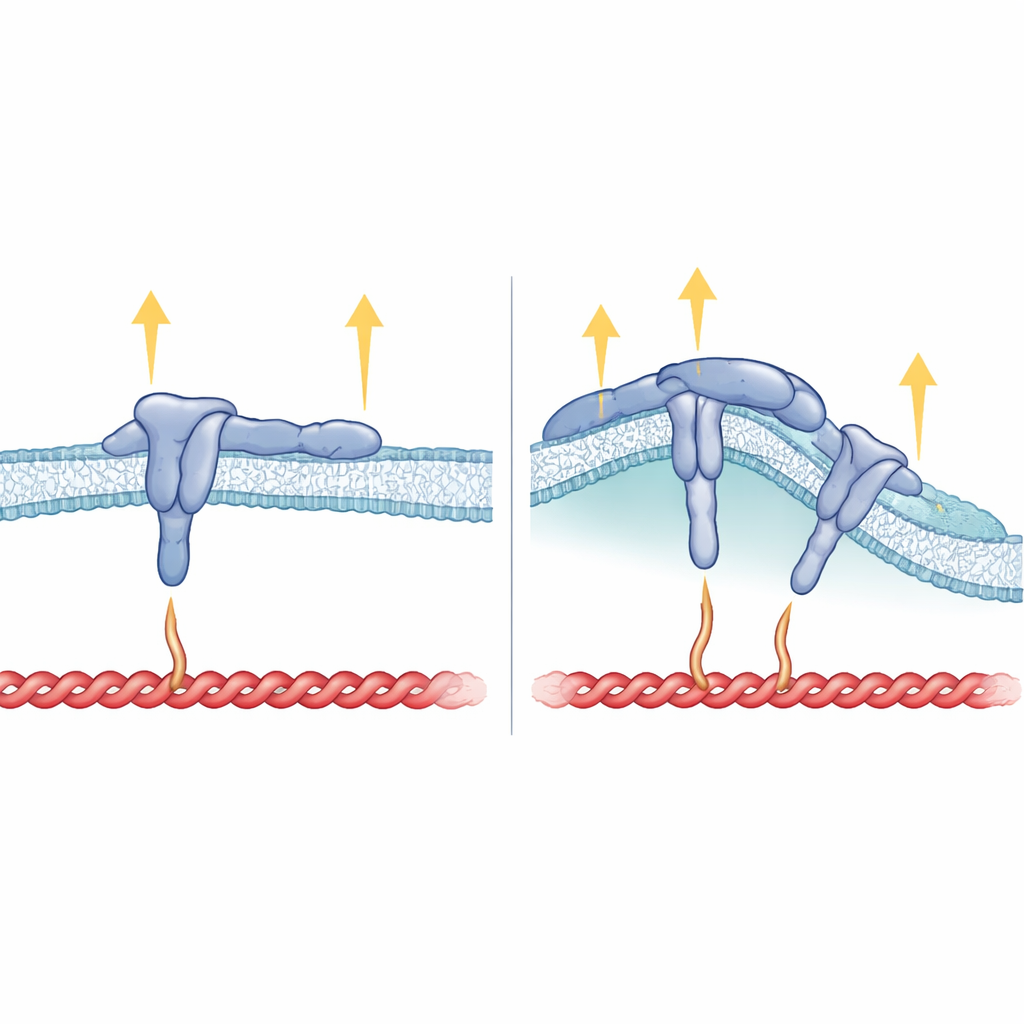
كيف يتوافق شكل الغشاء وبنية الإنتغرين والقوة معاً
بعيداً عن الذيل الداخلي، تبين أن جزء β5 الذي يعبر الغشاء كان حاسماً أيضاً. عندما استبدل الباحثون المقاطع العابرة للغشاء في β5 بمثيلها من β3، ظل الإنتغرين الناتج قادراً على تكوين الالتصاقات البؤرية لكنه لم يعد يفضل المواقع المنحنية ولا يتتبع FCHo2. يشير هذا إلى أن كيفية جلوس الإنتغرين في الغشاء تساعد في توجيه موتيف HDRRE بحيث يمكن لـFCHo2 الالتحام به في المناطق المنحنية وتثبيت αvβ5 المرتبط بالليجاند والنشط. في الالتصاقات المنحنية، يبدو أن تالين يلامس فقط جزءاً أبعد من ذيل الإنتغرين ولا يتحمل توتراً عالياً، وهو ما يفسر غياب عناصر أخرى محبة للقوة مثل فينكولين وتنسين وكاندلين هناك. في المقابل، في الالتصاقات البؤرية، يمسك تالين مواقع قريبة وبعيدة على الذيل والغشاء، داعماً قوى سحب قوية لكنه يمنع FCHo2 من الوصول إلى نفس المنطقة.
ما يعنيه هذا لسلوك الخلايا
للمراقب العادي، رسالة هذا العمل هي أن الخلايا تحمل وضعَي "ممسك" منفصلين للالتصاق بمحيطها. على المناطق المسطحة والصلبة تستخدم الالتصاقات البؤرية المدفوعة بتالين المبنية للسحب القوي. على البنى الليفية اللينة والمنحنية تتحول إلى الالتصاقات المنحنية المدفوعة بـFCHo2 التي تُمَكّن αvβ5 بنفوذ قوة أقل بكثير. تغيير طفيف في تسلسل الإنتغرين—وما إذا كان هذا الموقع مُعدَّلاً كيميائياً—يساعد على تقرير الوضع المستخدم. هذا النظام المزدوج يمكّن الخلايا من تفسير كل من الصلابة والشكل في بيئات ثلاثية الأبعاد، مما يؤثر على كيفية هجرة الخلايا وتنظيم الأنسجة، وربما على كيف تغزو أثناء المرض.
الاستشهاد: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
الكلمات المفتاحية: الإنتغرينات, الالتصاق الخلوي, انحناء الغشاء, FCHo2, الهيكل الخلوي