Clear Sky Science · ar
تشكّل الإندازول المحفَّز بالنترو ريدوكتاز
تحويل مكونات بسيطة إلى أدوية قيمة
تعتمد العديد من الأدوية الحديثة على عدد قليل من «الأُطر» الجزيئية الشائعة التي تناسب أهداف الجسم بشكل جيد. أحد هذه الأُطر، المسمى إندازول، يظهر في أدوية تُستخدم ضد السرطان والغثيان الشديد. حتى الآن، كان إنتاج الإندازولات يتطلب عادة مواد كيميائية قاسية، ودرجات حرارة مرتفعة، ومعادن غير صديقة للبيئة. تُظهر هذه الدراسة كيف يمكن للعلماء حثّ الإنزيمات الطبيعية على بناء الإندازولات بلطف في الماء، مما يفتح الباب أمام طرق أكثر خضرة لإنتاج الأدوية المهمة.
لماذا تهم هذه الجزيئات الحلقية
يعيد مصممو الأدوية استخدام هياكل حلقية معينة لأنّها تتفاعل بشكل موثوق مع البروتينات في الجسم. الإندازولات هي واحدة من هذه الهياكل المفضلة وتوجد في أدوية معتمدة لعلاج السرطان والغثيان الناتج عن العلاج الكيميائي. يعرف الكيميائيون بالفعل عدة طرق لصنع الإندازولات، لكن المسارات القياسية تعتمد على لبنات بناء تفاعلية، وقواعد أو أحماض قوية، ومحفزات معدنية مثل النحاس والبلاديوم. تعمل هذه الطرق، لكنها تولّد نفايات، وتستهلك طاقة، وتشكل مخاطر سلامة، وهو ما يتعارض مع السعي المتزايد للتصنيع المستدام في صناعة المستحضرات الصيدلانية.
الإنزيمات كعمّال بناء رقيقو المِؤَازَرَة
بدلاً من إجبار الذرات على الاتحاد بالحرارة والمواد القوية، لجأ الباحثون إلى التحفيز البيولوجي—استخدام الإنزيمات، المحفزات الطبيعية، لإجراء التفاعلات في الماء وفي درجة حرارة الغرفة. ركزوا على إنزيمات تُسمى نترو ريدوكتازات، التي تساعد الخلايا عادة على إزالة سمية المركبات الحاوية على مجموعات النترو عبر اختزال تدريجي. افترض الفريق أنه إذا أمكن تحرير وسيط معين في مسار الاختزال هذا في اللحظة المناسبة، فسينطوي على نفسه ويكوّن حلقة الإندازول المميزة تلقائياً. باستخدام اثنين من نترو ريدوكتازات مختلفتين، أظهروا أن مواد البداية البسيطة من نوع 2-نيتروبنزيل أمين تتحول بسلاسة إلى إندازولات بكفاءة ممتازة، غالباً بتَحَوُّل يفوق 99%، تحت ظروف مائية ولطيفة.
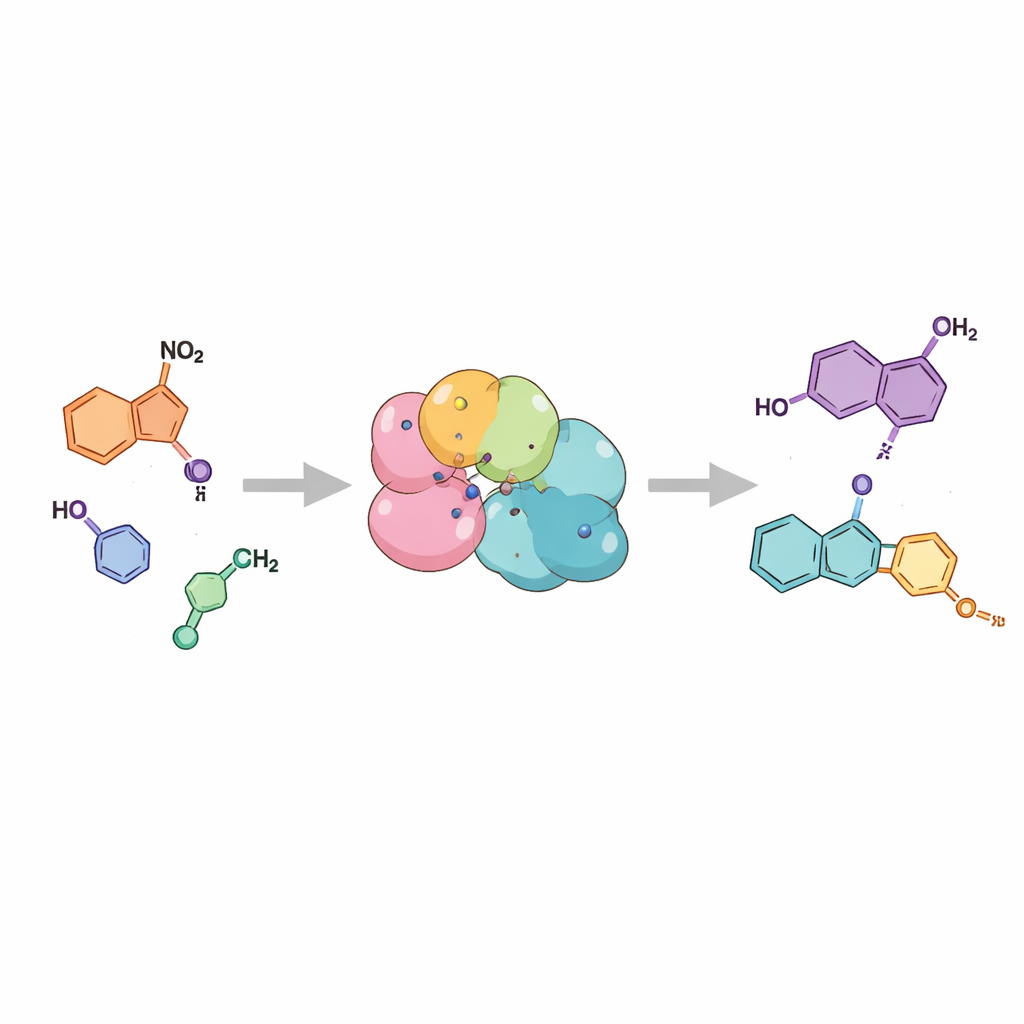
رسم خريطة لقدرات الإنزيمات
لاختبار مدى عمومية هذه الاستراتيجية، زوّد الباحثون الإنزيمات بمجموعة من مواد بداية ذات صلة تحمل مجموعات جانبية ومواقع مختلفة على الحلقة العطرية. وجدوا أن كلا الإنزيمين تحمل طيفاً واسعاً من التعديلات الكيميائية، من مجموعات صغيرة مثل الميثيل إلى أنظمة حلقية أكبر وعدة استبدالات بالكلور والبروم والميثوكسي. في كثير من الحالات، سارت التفاعلات بنقاء نحو الإندازول المطلوب، مع عوائد معزولة مرتفعة بما يكفي لتكون عملية. كما أن شكل الزخرفة على مادة البداية سيطر أيضاً على أي شكلين متقاربين من الإندازول يظهران، وهي ميزة مهمة لأن كلا الشكلين قد يكون لها أهمية في تصميم الأدوية. ويمكن تمديد نفس المبدأ لصنع قريب أكبر من الإندازولات، يُسمى السينولينات، مما يبرز مرونة المنهج.
بناء خط تجميع إنزيمي من خطوتين
الإندازولات في هذا العمل لا تُنتج مباشرة من مواد بداية متخصصة؛ بل بنى الفريق خط تجميع إنزيمي قصير يبدأ من لبنات بناء رخيصة. في الخطوة الأولى، فئة إنزيمية مختلفة، إنزيم اختزال الإيمين، تربط ألدهيد بسيطاً وأمينا لصنع 2-نيتروبنزيل أمين المطلوب. في الخطوة الثانية، يحول النترو ريدوكتاز هذا الوسيط إلى حلقة الإندازول. من خلال ضبط كميات الإنزيمات ونظام إعادة تدوير عواملهما المساعدة، شغّل المؤلفون هذا المسار المكوّن من إنزيمين على مقياس تحضيري، بدءاً من 50 ميليغراماً من الألدهيد في الماء. حصلوا على عدة منتجات إندازول بعوائد إجمالية جيدة، بما في ذلك أمثلة ذات سلاسل جانبية مختلفة يمكن تعديلها لاحقاً لأغراض اكتشاف الأدوية.
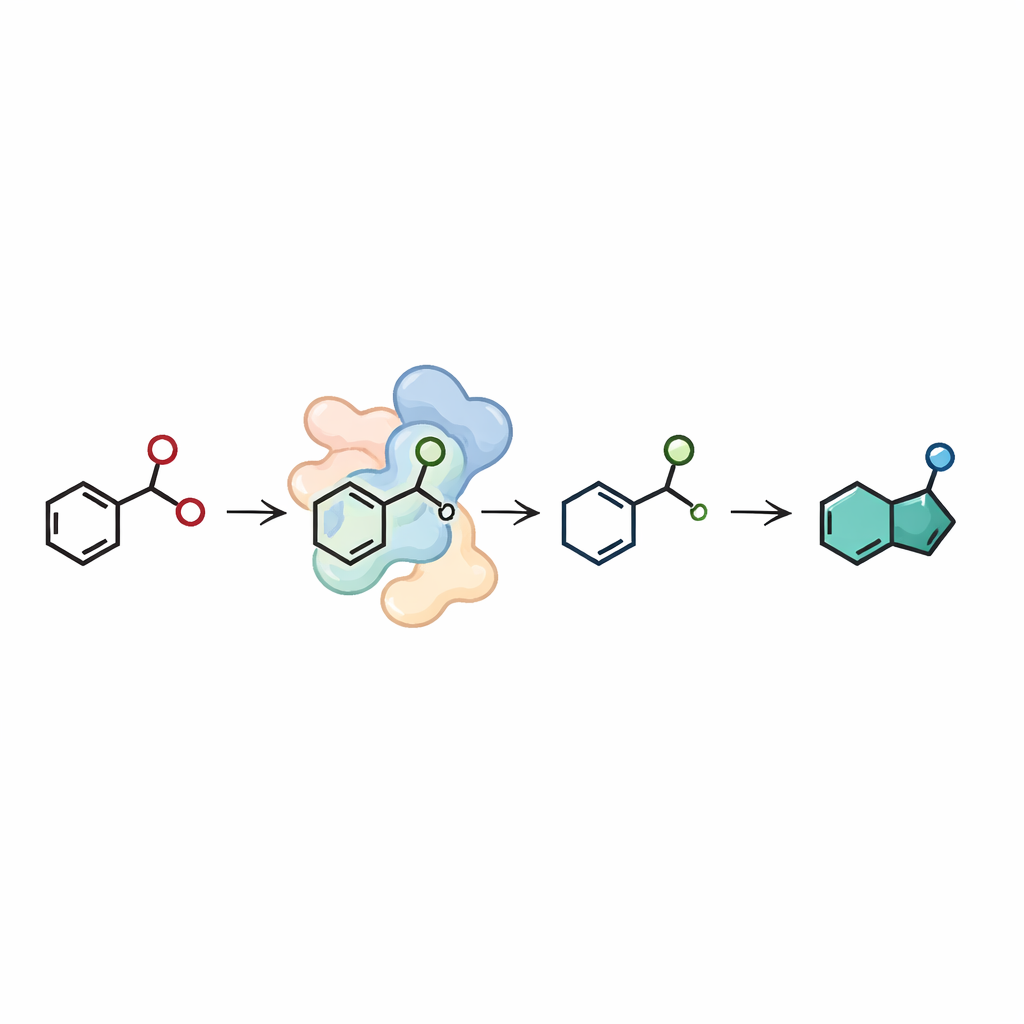
طريق أنظف لبِنَى دوائية معقدة
للقارئ العام، الرسالة الأساسية هي أن الباحثين علموا المحفزات الطبيعية تجميع حلقة مهمة طبياً بطريقة ألطف على العاملين والبيئة معاً. طريقهم المعتمد على الإنزيمات يتجنب المتفاعلات الضارة من نوع نيتروجين–نيتروجين والمحركات المعدنية النفيسة، ويعمل في الماء عند درجات حرارة معتدلة، ويمكن دمجه مع إنزيمات أخرى ليشكّل مصنعاً صغيراً وفعالاً. تضيف هذه العمل أداة قوية جديدة إلى صندوق أدوات الكيميائي، وتقرّب خطوة التصنيع المستدام، بينما تزود عالم الأدوية ببِنَى إندازول متعددة الاستخدامات للأدوية المستقبلية.
الاستشهاد: Terholsen, H., Medema, L., Chernyshova, E. et al. Nitroreductase-triggered indazole formation. Nat Commun 17, 2261 (2026). https://doi.org/10.1038/s41467-026-68926-y
الكلمات المفتاحية: التحفيز البيولوجي, تخليق الإندازول, نترو ريدوكتاز, كيمياء خضراء, سلاسل إنزيمية