Clear Sky Science · ar
التمدد النسلي لخلايا T القاتلة CD8⁺ في ARIA المرتبطة باليكانيماب
لماذا هذا مهم للأشخاص المصابين بالزهايمر
يُعد ليكانيماب واحدًا من أوائل الأدوية القادرة على إزالة الأميلويد من الدماغ وإبطاء فقدان الذاكرة بدرجة متواضعة لدى مرضى الزهايمر. ومع ذلك، يصاب بعض المرضى أثناء هذا العلاج بتورم دماغي أو نزيفات دماغية صغيرة، وهي تغييرات تُرى في صور الرنين المغناطيسي وتندرج تحت مصطلح شذوذات التصوير المتعلقة بالأميلويد (ARIA). تطرح هذه الدراسة سؤالًا حاسمًا للمرضى وعائلاتهم: ما الذي يحدث في الجهاز المناعي عند ظهور ARIA، وهل يمكن لاختبار دم بسيط يومًا ما أن يساعد في التنبؤ بمن هم الأكثر عرضة للخطر؟
وعد ومخاطر علاج جديد للزهايمر
ليكانيماب هو جسم مضاد يُعطى عن طريق التسريب ويستهدف تكتلات من بروتين يُدعى أميلويد-بيتا، وهو علامة مميزة لمرض الزهايمر. من خلال مساعدة الجسم على إزالة الأميلويد، يمكنه إبطاء التدهور المعرفي بشكل طفيف. لكن هذه الفائدة مصحوبة بمسألة سلامة: يصاب بعض الأشخاص بـ ARIA، والتي قد تشمل مناطق من التورم الدماغي أو نزيفات دقيقة. تتطلب هذه الآثار الجانبية مراقبة متكررة بالرنين المغناطيسي ويمكن أن تحد من الأشخاص المؤهلين لتلقي الدواء. ليس الجميع معرضًا للخطر بنفس القدر — حاملو متغير جيني يدعى APOE4 يكونون أكثر عرضة — لكن الجينات وحدها لا تفسر سبب حدوث ARIA، خاصة في المراحل المبكرة بعد بدء العلاج. وبما أن ليكانيماب يُعطى عبر مجرى الدم، افترض الباحثون أن فحص الخلايا المناعية في الدم عن قرب قد يكشف إشارات تحذيرية مبكرة أو حتى آليات تربط العلاج بإصابة الأوعية الدموية في الدماغ. 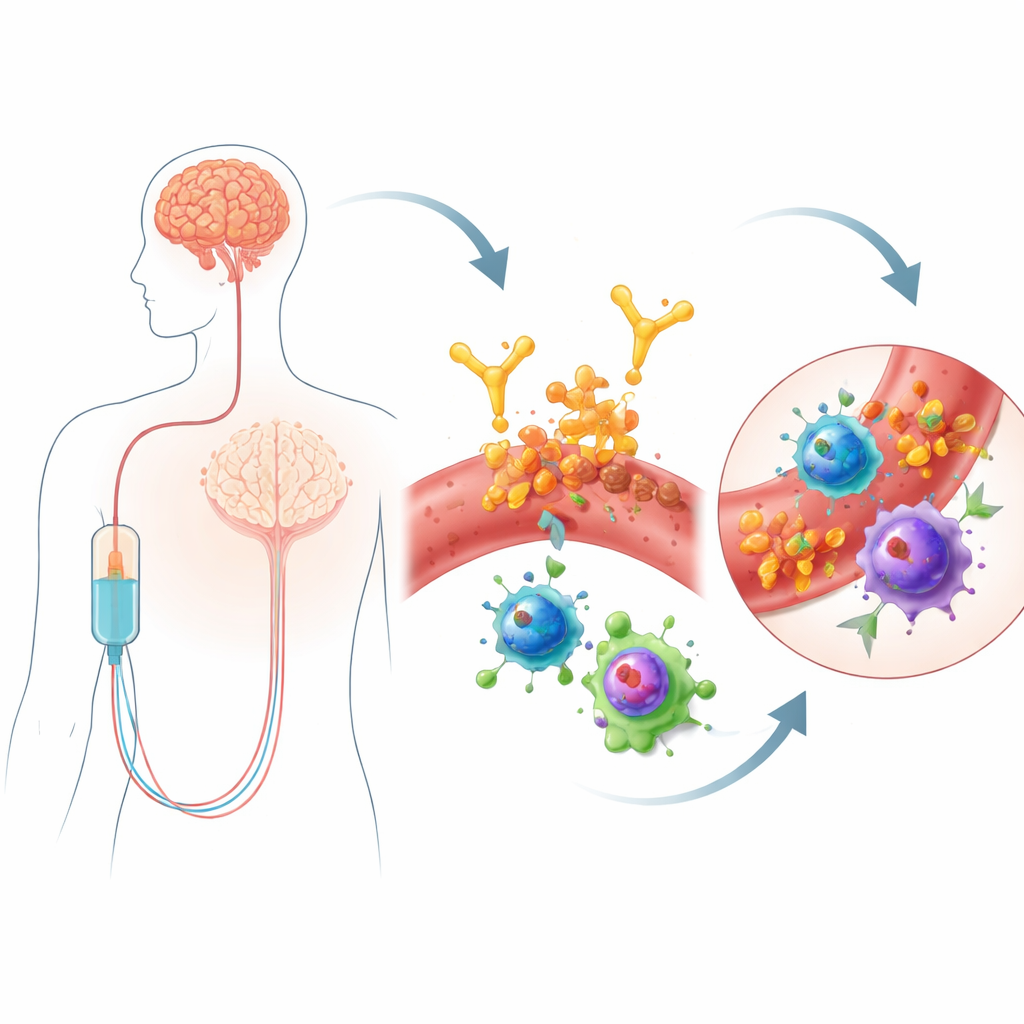
مراقبة الخلايا المناعية لدى مرضى طوّت لديهم ARIA والذين لم يطوّ
درس الباحثون ستة أشخاص مصابين بالزهايمر يتلقون ليكانيماب في عيادة ذاكرة إقليمية. أصيب ثلاثة منهم بأشكال مختلفة من ARIA، بينما لم تُظهر المجموعة المطابقة (متشابهة في العمر والجنس والنمط الجيني لـ APOE وعدد التسريبات) أي أعراض. سحبت عينات دم قبل التسريبات مباشرة، واستخدم الفريق نهجًا متعدد -أوميكيًا مكثفًا: تسلسل RNA الخلوي أحادي الخلية لقراءة أي الجينات مُفعلة في آلاف الخلايا المناعية المنفردة، وعلامات قائمة على الأجسام المضادة لتحديد أنواع الخلايا، وتسلسل مستقبلات الخلايا T لتتبع النسائل، وقياسات ميتابولومية مستهدفة لقياس مئات الجزيئات الصغيرة المشاركة في تمثيل الخلايا الغذائي. سمح ذلك لهم بأن يسألوا ليس فقط أي أنواع الخلايا كانت حاضرة، بل أيضًا مدى نشاطها، وما نوع الوقود الذي تستخدمه، وما إذا كانت عائلات محددة من خلايا T تتوسع استجابة لمثير ما.
تمدد خلايا T القاتلة عالية التسليح
ظهر نمط واضح لدى المرضى الذين أصيبوا بـ ARIA. مقارنةً بالضوابط، كان لديهم نسبة أعلى من خلايا CD8 "القاتلة" وقلة في خلايا CD4 المساعدة. داخل تجمع CD8، برزت مجموعتان فرعيتان: خلايا الذاكرة الفاعلة وخلايا متمايزة نهائيًا تُعرف بخلايا TEMRA. تشبه خلايا TEMRA الجنود المخضرمين — متخصصة للغاية للهجوم، مزودة بآلات قوية لقتل الخلايا المستهدفة. عند المرضى إيجابيي ARIA كانت خلايا TEMRA أكثر عددًا، وأكثر تمددًا نسليًا (بمعنى أن عائلات خلوية معينة تضاعفت)، وحملت برامج جينية مرتبطة بالسمية الخلوية والهجرة عبر الأوعية الدموية وعلامات التحفيز المزمن. لوحظت حالات خلوية مماثلة في الشيخوخة والعدوى المزمنة والتصلب المتعدد وفي السائل النخاعي لأشخاص مصابين بالزهايمر، حيث يمكن أن تتراكم قرب الأوعية الدموية وسطح الدماغ.
إعادة توصيل التمثيل الغذائي وتواصل مع خلايا مناعية أخرى
كما وجد الفريق أن خلايا CD8 الفاعلة أعادت توصيل استقلابها. بدلًا من الاعتماد بشكل رئيسي على إنتاج الطاقة الفعال في الميتوكوندريا، انتقلت إلى التحلل السكري، وهو طريق أسرع لكن أقل كفاءة لتوليد الطاقة يدعم نشاطًا عالي الشدة وقصير العمر. دعمت قياسات المستقلبات في خلايا الدم هذا الاستنتاج: ارتفعت مستويات اللاكتات والبيروفات، بينما انخفضت مكونات رئيسية لدورة حمض الستريك، نمط نموذجي للخلايا المناعية الالتهابية. أظهرت الخلايا الوحيدية (المونوسايت) — نوع آخر من خلايا الدم البيضاء — تغييرات مكملة. في المرضى إيجابيي ARIA، شغّلت الوحيديات جينات لعرض المستضدات والالتصاق بالخلايا وإنتاج الكيموكينات — إشارات كيميائية تجذب خلايا T. أشارت النمذجة الحاسوبية لأزواج الرابط-المستقبل إلى أن الوحيديات كانت ترسل إشارات أقوى للتنشيط والتموضع نحو خلايا CD8 الفاعلة، مكوّنة بيئة تشجّع هذه الخلايا القاتلة على التماس جدران الأوعية الدموية.
رموز العنوان التي توجّه خلايا T نحو أوعية الدماغ
نظرًا لأن هذه الدراسة أخذت عينات من الدم فقط، لجأ المؤلفون إلى مجموعة بيانات أحادية الخلية مستقلة مأخوذة من أدمغة مرضى عولجوا باليكانيماب ليروا ما إذا كانت نفس برامج خلايا T مرتبطة بجيوب وعائية في الدماغ. عندما عرضوا مجموعات CD8 الخاصة بهم على هذه الخريطة الدماغية، أظهرت خلايا TEMRA وخلايا الذاكرة الفاعلة من المرضى إيجابيي ARIA "رموز عنوان" نسخية — تركيبات من جزيئات التصاق ومستقبلات كيموكين — تطابقت مع خلايا بطانة الأوعية (الخلايا البطانية) في الدماغ المريض. تشير هذه البصمات إلى أن خلايا T القاتلة المتوسعة ليست فقط مسلحة بشدة ومفعّلة تمثيليًا، بل مستعدة أيضًا للتوجه والتفاعل مع أوعية دماغية متوترة في مواقع إزالة الأميلويد. 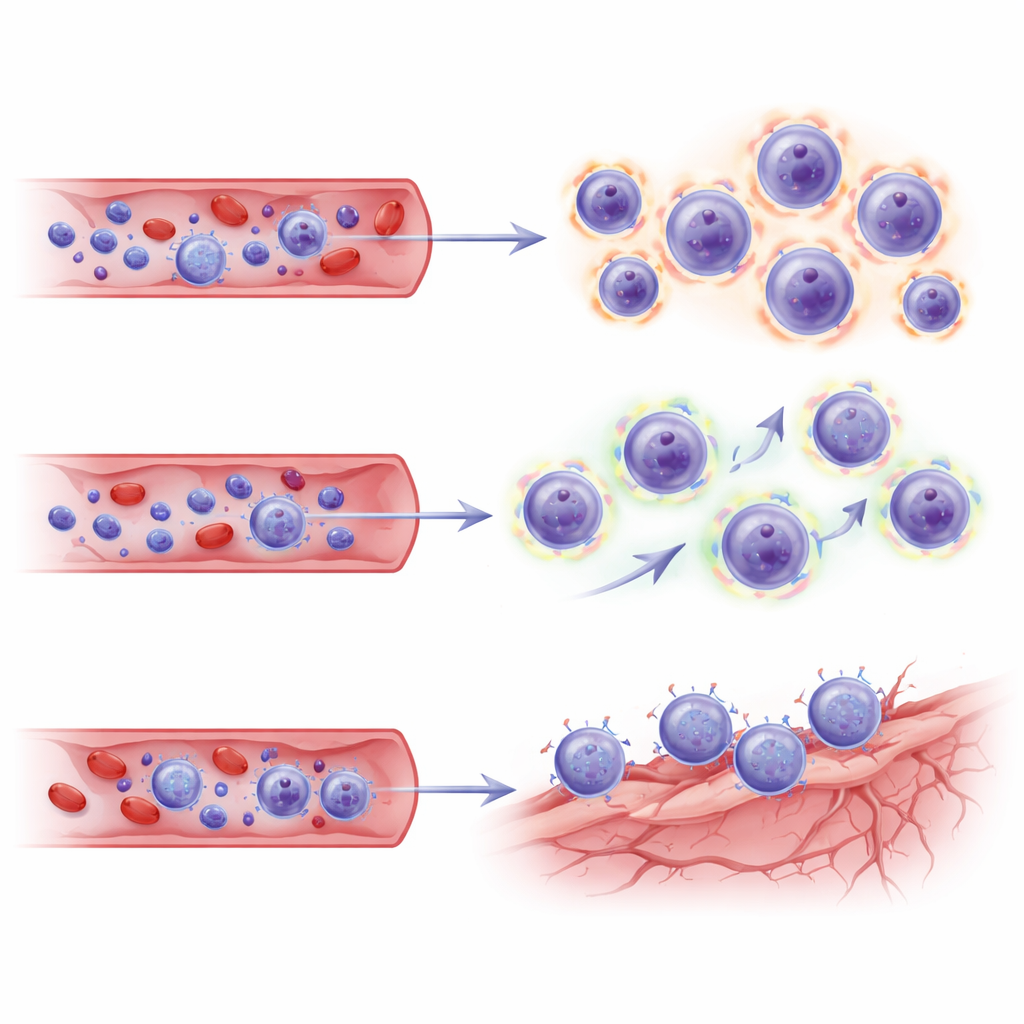
ما الذي قد يعنيه ذلك للمرضى والرعاية المستقبلية
معًا، ترسم هذه الدراسة الصغيرة لكن المفصلة صورةً عن ARIA كأمر يتجاوز كونه أثرًا جانبيًا سلبيًا لإزالة الأميلويد. بل يظهر أنه مرتبط باستجابة مناعية منسقة في الدم: تمدد وتنشيط تمثيلي لعناصر نسلية محددة من خلايا T القاتلة، تقوية الإشارات الصادرة من الوحيديات، وميزات جزيئية تُفضّل التفاعل مع أوعية الدماغ. العمل لا يثبت أن هذه الخلايا تسبب ARIA — فقد تكون التغيرات المناعية رد فعل على إصابة الأوعية بدلاً من مصدرها — لكنه يوفر فرضيات قابلة للاختبار ومخططًا لعلامات حيوية قائمة على الدم. مستقبلًا، قد يساعد قياس وفرة وحالة التمثيل الغذائي لخلايا CD8 TEMRA، إلى جانب جزيئات إشارات رئيسية، في تحديد المرضى الأكثر عرضة لخطر ARIA، وتوجيه جداول المراقبة، أو حتى إلهام استراتيجيات مستهدفة لتقليل هذه الاستجابة المناعية مؤقتًا مع الحفاظ على فوائد علاجات إزالة الأميلويد.
الاستشهاد: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
الكلمات المفتاحية: مرض الزهايمر, ليكانيماب, الخلايا المناعية, أوعية الدم في الدماغ, آثار جانبية للعلاج