Clear Sky Science · ar
بروتينات TMEM63 تعمل كمحولات للدهون منشّطة ميكانيكياً ومعدّلة بالكوليسترول تسهم في مقاومة الغشاء للقوى الميكانيكية
كيف تبقى الخلايا سليمة تحت الإجهاد الفيزيائي
خلايا أجسامنا تتعرض باستمرار للضغط والشد والاهتزاز، سواء في القلوب النابضة أو العضلات العاملة أو الأورام التي تدفع عبر النسيج. تكشف هذه الدراسة كيف تساعد عائلة من بروتينات الغشاء، تُسمى OSCA/TMEM63، الخلايا على النجاة من مثل هذه القوى الميكانيكية القاسية عبر إعادة ترتيب الدهون في غلافها الخارجي. فهم هذا النظام المدمج الماص للصدمات قد يفتح زوايا جديدة لفهم اضطرابات السمع وعزل الأعصاب وحتى انتشار السرطان.
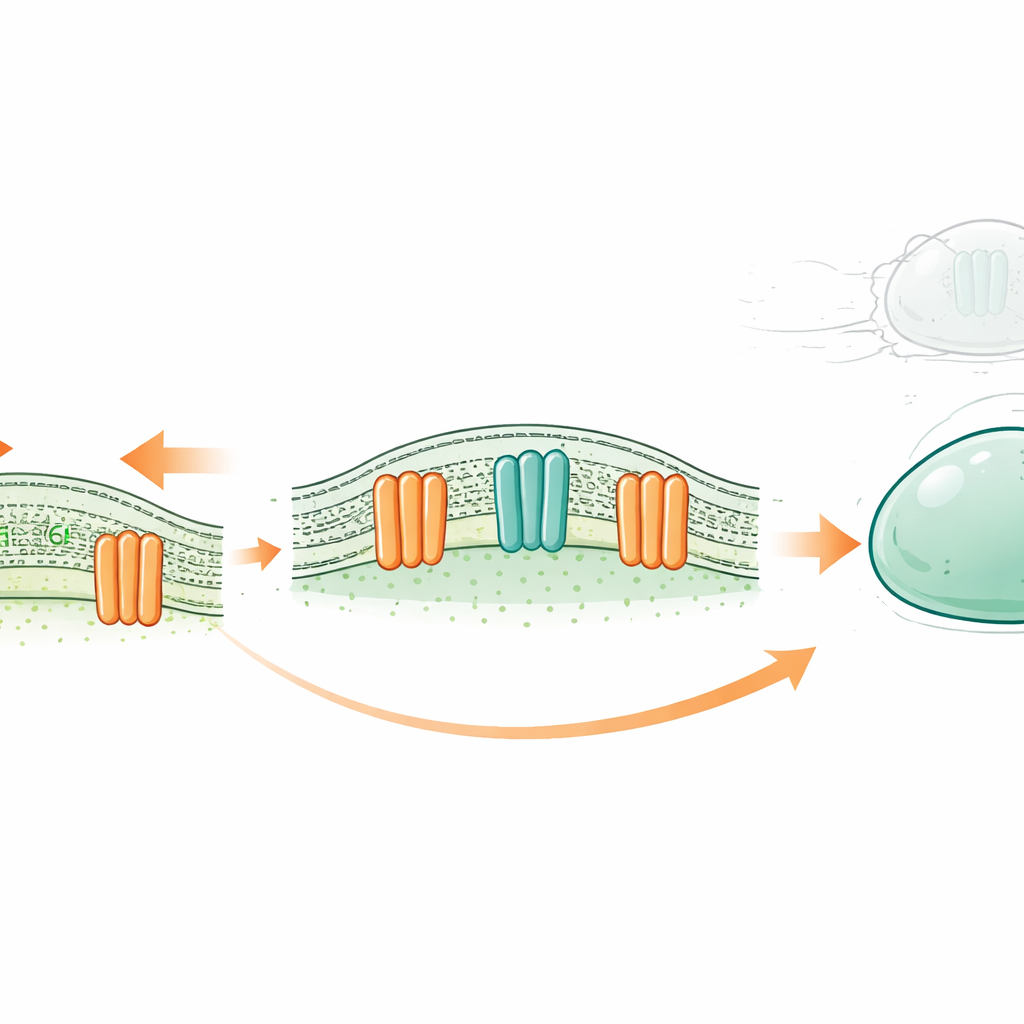
نوع جديد من ممتصات الصدمات الخلوية
كل خلية محاطة بغشاء زيتي رقيق مكوّن من طبقتين من جزيئات شبيهة بالدهون تُسمى الليبيدات. تقليدياً كان يُعتقد أن بعض بروتينات الغشاء تعمل فقط كقنوات أيونية — صمامات دقيقة تسمح بتدفق الجسيمات المشحونة استجابة لمنبهات مثل الشد. عُرف أن عائلة OSCA/TMEM63، الموجودة من النباتات إلى البشر، تنفتح استجابةً لتوتر الغشاء. أشارت أعمال بنيوية سابقة إلى أن مساماتها قد تكون مبطنة جزئياً بالليبيدات نفسها، مما أثار احتمالاً مثيراً: هل يمكن أن تعمل هذه القنوات أيضاً كمحوّلات للليبيدات (scramblases)، تُقلّب الليبيدات بين الطبقتين الداخلية والخارجية للغشاء عند تعرض الخلية لقوة؟
مراقبة تقليب الليبيدات عبر الغشاء
لاختبار هذه الفكرة، جمع الباحثون بين محاكاة حاسوبية وأنظمة مختبرية اختزالية مبنية من مكونات ممنوحة. في المحاكاة، وُضعت نسخ مفتوحة من عدة بروتينات OSCA وTMEM63 في أغشية نموذجية. تحرّكت جزيئات الليبيد تلقائياً عبر شقّ في هذه البروتينات من جانب واحد من ثنائي الطبقة إلى الجانب الآخر، مكوِّنة حزاماً يربط بين الورقتين في حين تركت مساراً مملوءاً بالماء للأيونات. في تجارب موازية، بنى الفريق "فقاعات" اصطناعية كبيرة (حويصلات) تحتوي على ليبيدات متألقة وبروتينات محددة. عندما قام عامل خارجي بإخماد الوجيه على السطح الخارجي، لم يكن أي انخفاض إضافي في الإشارة مبرراً إلا بتقليب الليبيدات من الطبقة الداخلية إلى الخارج. أظهرت الحويصلات التي تحتوي على OSCA1.1 أو OSCA1.2 أو OSCA2.2 أو TMEM63A/B هذا الفقد الإضافي في الفلورة، ما يشير إلى تقليب نشط، بينما القنوات الضابطة التي لا تقلب الليبيدات لم تُظهر ذلك.
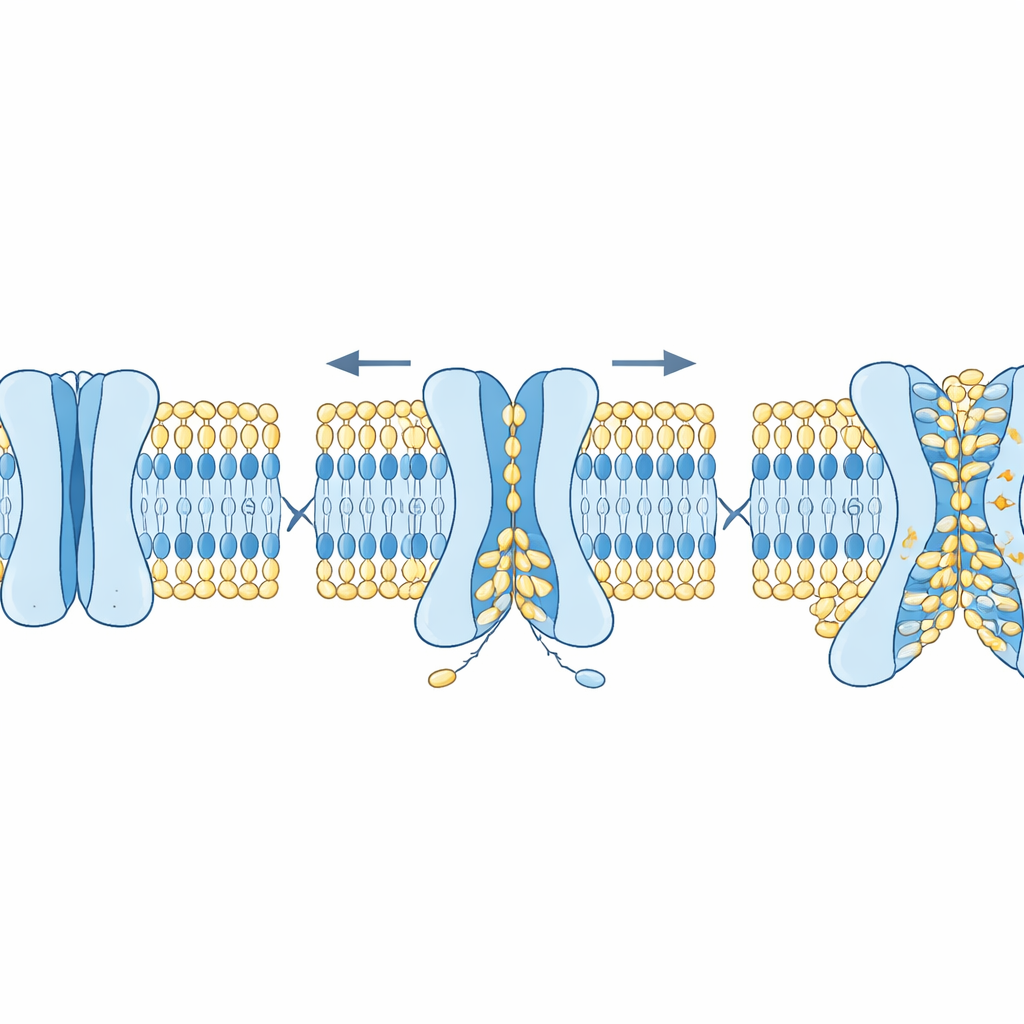
كيف تضبط البنية والكوليسترول العملية
سأل الباحثون بعد ذلك أي خصائص في بروتينات TMEM63 تتحكم في هذا السلوك المزدوج. باستخدام AlphaFold2، ولّدوا أشكالاً محتملة عديدة لبروتينات TMEM63 البشرية، تتراوح من مغلقة إلى مفتوحة تدريجياً. كشفت المحاكاة أن مجموعة قليلة من الأحماض الأمينية الضخمة تعمل كـ"عنق زجاجة" في الشق. قطعة واحدة تحدد بشكل رئيسي تدفق الأيونات، في حين أن أخرى تسد حركة الليبيدات. أدت طفرات في عنق الأيون إلى زيادة التوصيل الكهربائي دون تغيير كبير في تقليب الليبيدات، بينما سبّبت طفرات في بوابة الليبيد تقليب الليبيدات بسهولة أكبر وجعلت الخلايا تُظهر إشارات "كلِّني" على سطحها دون أي محفز إضافي. كان للكوليسترول أيضاً دور تنظيم رئيسي؛ فإضافة الكوليسترول إلى أغشية نموذجية أبطأت تقليب الليبيدات بشكل ملحوظ وثبتت حالة الإغلاق لبروتين TMEM63A، سواء في المحاكاة أو في هياكل المجهر الإلكتروني بالتجميد حيث ارتبط الكوليسترول بمواقع محددة على البروتين.
القوة الميكانيكية كمفتاح التشغيل
إذا كان الكوليسترول عادة يكبح التقليب داخل الخلايا، فما الذي يشغّله في اللحظة المناسبة؟ استخدم الفريق جزيئات سكر حلقيّة تسمى السايكلوديكسترينات لسحب الليبيدات انتقائياً من الأغشية وبالتالي زيادة التوتر دون إزالة الكوليسترول. في حويصلات بحجم خلية، فعّل إضافة السايكلوديكسترين تقليب الليبيدات بواسطة TMEM63A فقط عندما كان البروتين موجوداً، ما يبرهن أن الإجهاد الميكانيكي وحده قادر على تحفيز التقليب. أظهرت مقاربات مماثلة في خلايا حية أن إزالة كمية بسيطة من الكوليسترول بمفردها لم تكن كافية؛ إذ كان مطلوباً تحدٍ ميكانيكي لاحق لرؤية تقليب قوي. عندما شُدّت خلايا معدّلة للتعبير عن TMEM63A مراراً، كشفت بسرعة عن بعض الليبيدات على سطحها الخارجي، وهو علامة مميزة للتقليب، بينما أظهرت الخلايا التي تفتقد هذه البروتينات تغيّرات أقل بكثير.
حماية الخلايا من التمزق
بعيداً عن تقليب الليبيدات فقط، غيّر التقليب المنشّط ميكانيكياً سلوك الأغشية الفيزيائي تحت ضغط شديد. في الحويصلات الاصطناعية المعرضة لقوة كبيرة، كانت الحويصلات التي تفتقر إلى المحوّلات تميل إلى الانفجار، بينما الحويصلات التي تحتوي على TMEM63A أو على محوّل معروف تقلّصت وتكوّنت أنابيب رفيعة وبقيت سليمة إلى حد كبير. في سلالة خلوية لسرطان الدماغ البشري التي تعبر طبيعياً عن TMEM63A وTMEM63B، جعل تقليل مستوى أي من البروتينين الخلايا أكثر عرضة للتمزق عند تعرضها لإجهاد ميكانيكي قوي. تدعم هذه النتائج معاً نموذجاً ترى فيه أن بروتينات OSCA/TMEM63 تعمل كصمامات تفتح تحت التوتر وتطمس مؤقتاً الاختلاف المعتاد بين السطحتين الداخلية والخارجية للغشاء. من خلال السماح لليبيدات بإعادة التوزيع بسرعة، تساعد على موازنة الإجهاد ومنع التمزق الكارثي.
ما الذي يعنيه هذا للصحة والمرض
بعبارة بسيطة، تُظهر هذه الأعمال أن بعض القنوات الحساسة للشد تقوم بأكثر من نقل الإشارات الكهربائية: فهي أيضاً تعيد تنظيم الجلد الخارجي للخلايا لمساعدتها على النجاة من الضغط. تبرز بروتينات TMEM63 كمحوّلات ليبيدية منشّطة ميكانيكياً تُضبط نشاطها بدقة بواسطة تركيب الغشاء، وبخاصة الكوليسترول. قد تكون آلية مقاومة الميكانيك هذه مهمة أينما تتعرض الخلايا لقوى كبيرة، من ألياف العصب المعزولة وخلايا الاستشعار الصوتي في الأذن إلى خلايا السرطان التي تتنقل عبر أنسجة ضيقة. قد يفتح فهم هذه الوظيفة المزدوجة كقناة أيونية ومحوّل لليبيدات دروباً جديدة لحماية أنسجة معرضة للخطر — أو، على العكس، لجعل خلايا السرطان شديدة التحمل أكثر هشاشة.
الاستشهاد: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
الكلمات المفتاحية: قنوات أيونية حساسة للميكانيك, تقليب الدهون, ميكانيكا غشاء الخلية, تنظيم بالكوليسترول, بروتينات TMEM63 وOSCA