Clear Sky Science · ar
ببتيد تشفيري سام ناتج عن طيّ مموه لـPKN1 معتمد على TDP-43
تهديدات خفية داخل خلايا الدماغ
تشترك العديد من أمراض الدماغ، بما في ذلك التصلب الجانبي الضموري (ALS) ومرض ألزهايمر، في تراكم قطع بروتينية تُدعى TDP-43. يعرف العلماء أنه عندما يتعطل هذا البروتين، تفقد الخلايا العصبية رسائل حيوية وفي النهاية تموت. تكشف هذه الدراسة عن تطور أكثر إثارة للدهشة: يمكن لفشل TDP-43 أيضاً أن يسبّب إنتاج خلايا الدماغ لببتيد صغير سام لم يُعرف سابقاً، وهو ما يلحق بدوره أضراراً بدوائر الذاكرة. قد تفتح معرفة هذا الفاعل الخفي سبلًا جديدة للتشخيص والعلاج في حالات الخَرَف المدمرة.
كيف يحافظ مُصحّح الخلايا على انتظام RNA
داخل الخلايا العصبية، يعمل TDP-43 كمصحح لغوي للـRNA، الرسائل الوسيطة التي تقع بين الحمض النووي والبروتينات. يرتبط بتسلسلات قصيرة محددة ويمنع إدراج «قطع إضافية» ضالة في هذه الرسائل. عندما يفقد TDP-43 أو يختلط موضعه، كما يحدث في ALS والعديد من حالات ألزهايمر، قد تنزلق هذه القطع الإضافية—المسماة الإكسونات المموهة—إلى داخل RNA. حتى الآن، كانت معظم الإكسونات المموهة المعروفة تسبّب فقدان البروتين الطبيعي ببساطة عن طريق جعل الرسالة غير مستقرة وتُدمر سريعاً. لم يتضح ما إذا كانت مثل هذه الأحداث يمكن أن تولّد أيضاً بروتينات جديدة ضارة.
طي مموه ينتج شظية سامة
ركز الباحثون على جين اسمه PKN1، الذي يساعد في الحفاظ على السقالات الداخلية وتدفق الإشارات في الخلايا العصبية. باستخدام نماذج خلوية قللوا فيها من TDP-43، اكتشفوا إكسوناً مموهاً غير معترف به سابقاً، أطلقوا عليه اسم PKN1‑5a1، مُدرَجاً بين مقطعين طبيعيين من RNA الخاص بـPKN1. يضيف هذا الإدراج إشارة وقف مبكرة، فتصنع RNA مقصّراً. ولافت أن جزءاً من هذه الرسالة المعيبة يفلت من نظام الرقابة النوعية داخل الخلية ويُترجَم إلى شظية ثابتة من بروتين PKN1 تحتوي فقط على أول 207 أحماض أمينية. أطلق الفريق على هذا الناتج المختصر اسم PKN207. أظهروا أن TDP-43 عادةً ما يمنع هذا الخطأ عبر الارتباط بعدة مناطق غنية بـUG تحيط بالإكسون المموه؛ عندما يضيع ذلك الارتباط، يُقصّ الإكسون ويُنتَج PKN207.
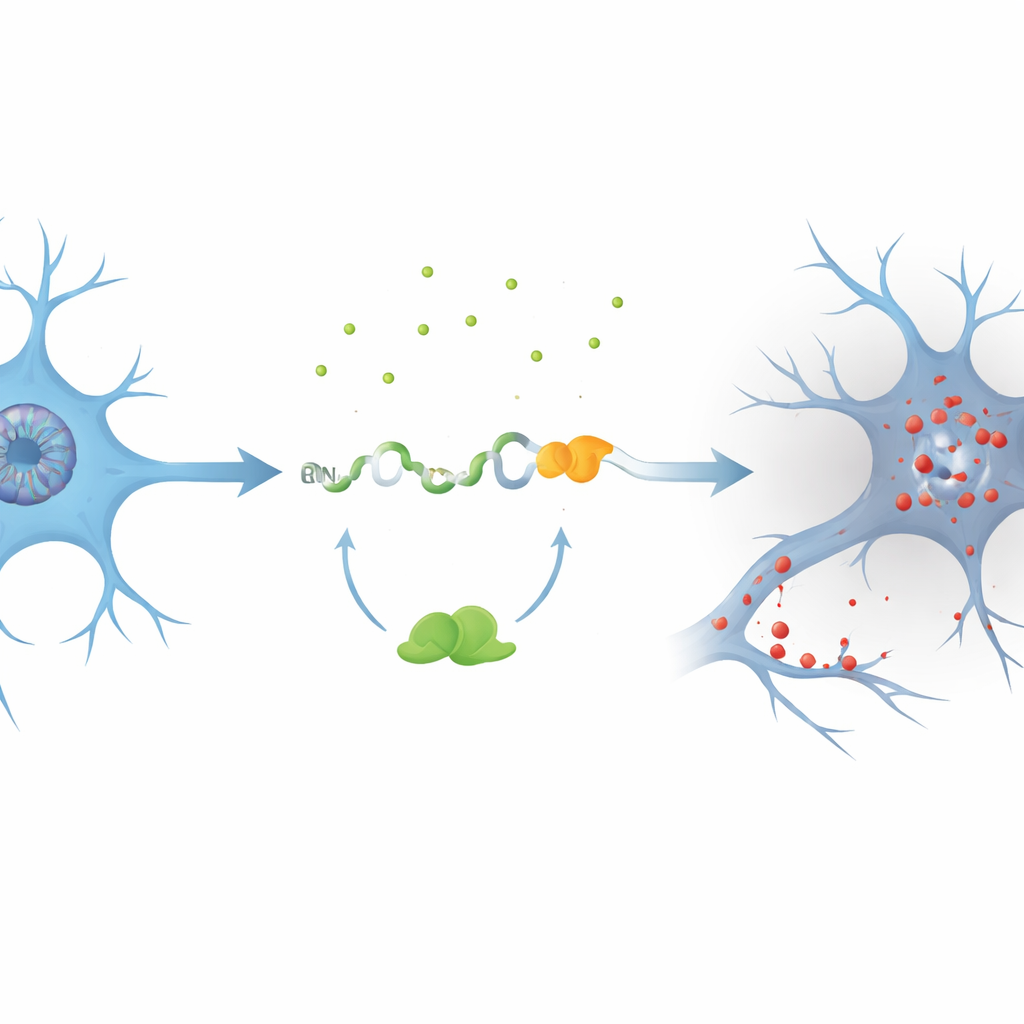
دلائل من أدمغة المرضى ومجموعات بيانات كبيرة
لاختبار ما إذا كان هذا الحدث يحدث في البشر المرضى، بحث الباحثون في بيانات تسلسل RNA المأخوذة من مئات عينات دماغ وحبل شوكي لمرضى ALS. وجدوا تنشيطاً واسع النطاق لإكسون PKN1‑5a1 المموه في مناطق معروفة بتأثرها بمرضية TDP-43، مثل القشرة الحركية والحبل الشوكي، لكن ليس في المخيخ الذي يبقى محتمياً نسبياً. ثم طوروا أجساما مضادة شديدة التخصص تتعرف فقط على الذيل الفريد لـPKN207، وليس على بروتين PKN1 الكامل. في نسيج الحُصين من مرضى ألزهايمر الذين ظهر لديهم أيضاً TDP-43 مفروض فسفره بشكل شاذ، كشفت هذه الأجسام المضادة عن نطاق مميز يتوافق مع PKN207، بينما كان هذا النطاق غائباً في أدمغة الشواهد. أكدت مجموعات بيانات ألزهايمر الإضافية أن الإكسون المموه يُشغَّل حتى في مراحل مبكرة من المرض، ما يشير إلى أن هذا الخطأ الجزيئي قد يبدأ قبل وقت طويل من بروز الأعراض.
ببتيد صغير بتأثير كبير على الذاكرة
أثار العثور على PKN207 في أدمغة بشرية مريضة السؤال الرئيسي: هل هو ضار؟ لاختبار ذلك، استخدم الفريق فيروسات لدفع إنتاج إما PKN1 الطبيعي أو PKN207 بشكل محدد في الحُصين—منطقة دماغية حاسمة للذاكرة—في فئران شابة. بعد أشهر، أظهر كلا المجموعتين من الفئران ضعفاً في التعلم في متاهة موريس المائية، حيث سبحوا وقتاً أطول للعثور على منصة مخفية. احتوى سائل الشوكي لديهم على مستويات أعلى من بروتين هيكلي، سلسلتها الخفيفة من الخيوط العصبية، وهو مؤشر على تلف المحوار. في الخلايا العصبية المستزرعة، أدّى تعزيز PKN207 إلى إصابة خلوية، قيس بتسرّب إنزيم يشير إلى تلف الغشاء. كشف تحليل تفصيلي لبروتينات الحُصين عن تغييرات واسعة في المسارات المرتبطة بقوة المشبك (التقوية طويلة الأمد) وأمراض التنكس العصبي المعروفة، مع تعطّل قوي بشكل خاص للجزيئات التي تدعم الإشارات الفعّالة وإطار الخلايا العصبية السليم.
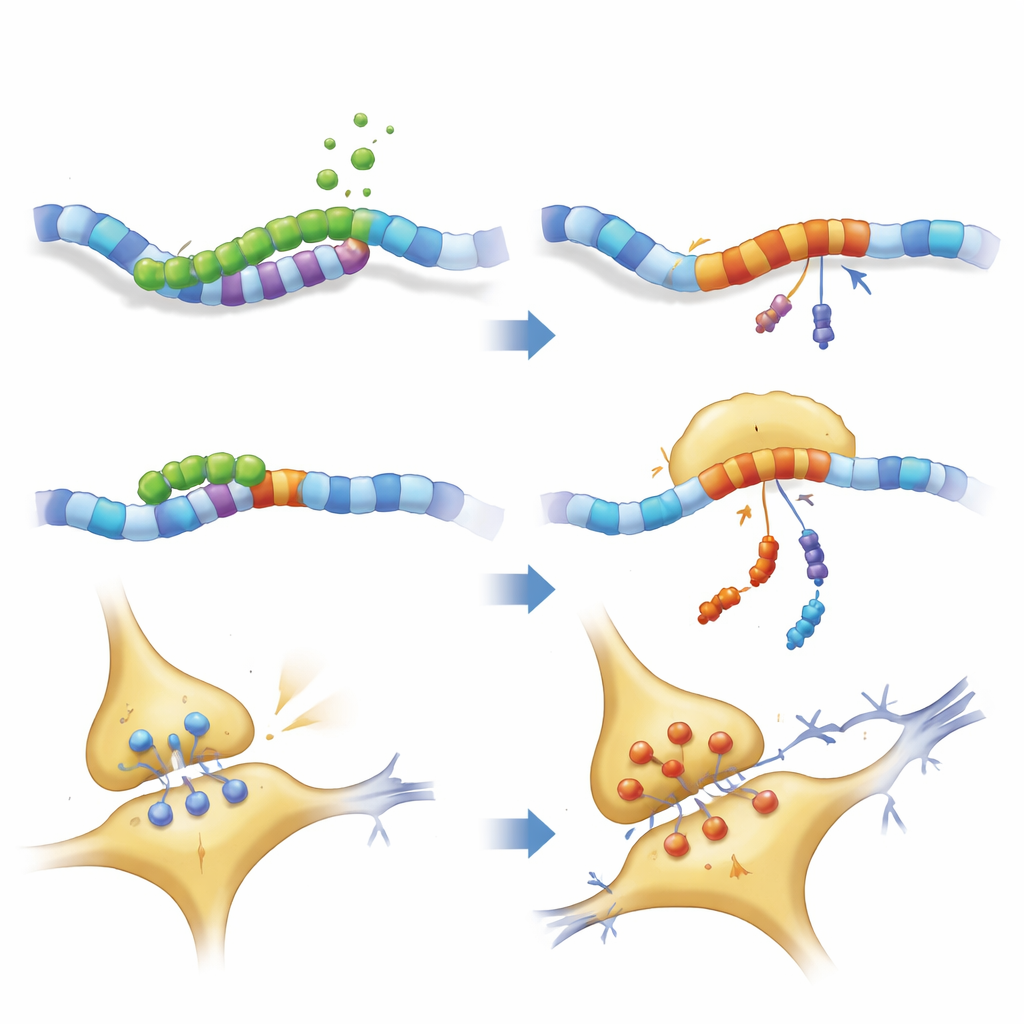
كيف تعطل الشظية شبكات الدماغ
أظهر الفحص الأدق لبنية الخلايا العصبية أن كل من PKN1 الكامل وPKN207 أزعجا شبكة الخيوط العصبية التي تمنح المحاور شكلها وتساعد على نقل البضائع. انخفضت بروتينات المحرك والهيكل الأساسية المهمة، بينما تراكمت بعض مكونات الخيوط العصبية، مما يوحي بزحام مروري واحتمال تكتل. أكدت القياسات الكهربائية من شرائح الحُصين أن الفئران المعبرة عن PKN207 عانت ضعفاً في التقوية طويلة الأمد—العملية التي تقوّي المشابك بعد نشاط متكرر وتُعتَبر أساساً خلوياً مقبولاً للتعلّم والذاكرة. رغم أن PKN207 يفتقر إلى المجال الإنزيمي لـPKN1، فإن وجوده كان كافياً لمحاكاة وأحياناً تجاوز التأثيرات المعيقة للبروتين الكامل، ما يوحي بأن النطاق المشترك من الطرف الن-يمكنه، بمفرده، أن يتدخل في توازن الخلايا العصبية.
لماذا تهم هذه النتيجة أمراض الدماغ
تضيف هذه الدراسة طبقة جديدة إلى فهمنا للاضطرابات المرتبطة بـTDP-43. فبدلاً من التسبب فقط في فقدان RNAs الأساسية، يمكن لفشل TDP-43 أن يولّد أيضاً ميكرو‑بروتين ثابتاً ساماً يقوّض المشابك والقدرات المعرفية. تبرز الآن إكسون PKN1‑5a1 المموه ومنتجه الببتيدي PKN207 كعلامات حيوية محتملة لخلل TDP-43 المبكر وكأهداف مرشحة لعلاجات تصحّح الطي أو تمنع الشظية الضارة. وعلى نطاق أوسع، تقترح الدراسة أن إكسونات مموهة أخرى قد تكون أيضاً مصدر بروتينات دافعة للمرض، ما يوجّه الباحثين نحو مشهد غني—وتم تجاهله سابقاً—من المشتبه بهم الجزيئيين في التنكس العصبي.
الاستشهاد: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
الكلمات المفتاحية: TDP-43, طي مموه, PKN1, الضمور العصبي, مرض ألزهايمر وALS