Clear Sky Science · ar
توسيع قدرة نواتقات الدي إن إيه الاصطناعية على التلف باستخدام كيمياء الكليك
بناء مقصات جزيئية أكثر ذكاءً
تعتمد بعض علاجات الكيمياء على إتلاف الحمض النووي للخلايا السرطانية، لكن الأدوية الحالية قد تكون أدوات خشنة تضر أيضاً بالأنسجة السليمة. تستعرض هذه الدراسة فئة جديدة من «المقصات الجزيئية» القابلة للبرمجة بدقة، المصنوعة من النحاس وقطع عضوية صغيرة تُجمع معاً بواسطة كيمياء الكليك. من خلال ضبط شكلها وطريقة تماسكها مع الحمض النووي، يهدف الباحثون إلى ابتكار عوامل تقطع المادة الوراثية بدقة أكبر، فاتحةً مسارات محتملة لعلاجات مضادة للسرطان ومضادة للبكتيريا في المستقبل.
تركيب قاطع ثلاثي الذراعين بتقنية الكليك
يستخدم الفريق كيمياء الكليك المحفّزة بالنحاس، وهي طريقة حازت على جائزة نوبل ومعروفة بموثوقيتها، لتجميع عائلة من الجزيئات تسمى ربطات تري-كليك (TC). كل جزيء TC هو محور ثلاثي الذراعين يمكن أن يحمل ثلاث أيونات نحاس في آن واحد، مكوّناً كتلة مدمجة قادرة على مهاجمة الحمض النووي. عبر استبدال مجموعات «المانح» الكيميائية في نهاية كل ذراع—المعتمدة على النيتروجين أو الأكسجين أو الكبريت—اختبر العلماء بشكل منهجي كيف تؤثر التغييرات البنية الدقيقة على ارتباط النحاس والتميّز مع الحمض النووي والنشاط الحيوي. من بين عدة تصاميم جديدة، برزت النماذج الحاملة لمجموعات نيتروجينية مسطحة حلزونية على أنها واعدة بشكل خاص لالتقاط الحمض النووي بإحكام.
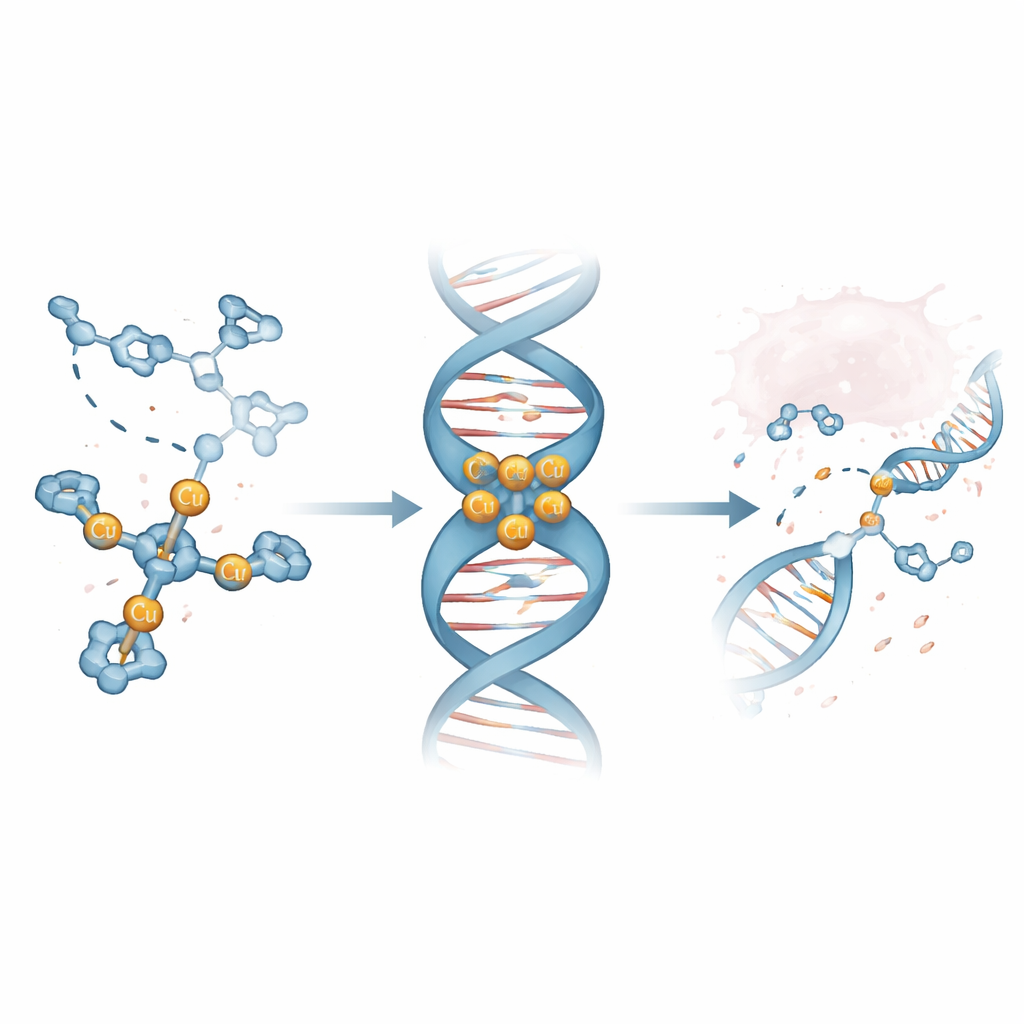
اكتشاف جزيء رائد يفضّل أخاديد الحمض النووي
أظهر الباحثون باستخدام مطيافية الكتلة وطرق بصرية أن مركباً واحداً يُدعى Cu3-TC-Py يشكل بثبات مجموعة مكونة من ثلاثة أيونات نحاس مستقرة في المحلول. كشفت تجارب التنافس مع أصباغ فلورية مرتبطة بـDNA من ثم الجِرْف العجالي أن Cu3-TC-Py يزيح هذه الأصباغ عند تركيزات منخفضة جداً، ما يدل على ارتباط قوي بالحمض النووي. أظهرت اختبارات لاحقة على قطع قصيرة من الحمض النووي ذات شكل دبوسي أن هذا المركب يفضّل الاستقرار داخل الأخدود الصغير—الوادي الأضيق الذي يلتف حول اللولب المزدوج—وبصفة خاصة يفضّل تسلسلات غنية بالزوجين G وC. دعمت المحاكاة الحاسوبية عالية الدقة هذه الصورة، مُظهِرة المركب الثلاثي الذراعين جالساً في الأخدود، وشحناته الموجبة تلتف حول الحمض النووي السالب، مع ضغط طفيف لللولب.
من الارتباط القوي إلى انكسار وتفكك الحمض النووي
على مستوى الجزيء الواحد، راقب الفريق خيوط دي إن إيه طويلة محصورة في قنوات نانومترية أثناء تفاعلها مع Cu3-TC-Py. عند جرعات منخفضة، نافس المركب صبغة الشد وبدّلها أثناء ارتباطه في الأخاديد. عند جرعات أعلى، بدأ الحمض النووي بالانكماش ثم تكاثف بالكامل، متسقاً مع جذب كهرستاتيكي قوي بين مجموعة النحاس وعمود الحمض النووي الفقري. عندما تعرّض الحمض النووي البلازميدي للمركب في وجود عامل مخفّض، تحوّلت الخيوط من شكلها الملفوف الأصلي إلى أشكال مرتخية ثم إلى أشكال خطية كاملة، وهو نمط يشير إلى تكوّن كسور أحادية وثنائية الشريط. أشارت اختبارات إضافية باستخدام مانعات الجذور الحرة إلى أن أنواع أكسجين قصيرة العمر—مثل الأكسيد الفائق، والأكسجين المفرد، وجذور الهيدروكسيل—هي الأدوات الحقيقية للقطع المتولدة بالقرب من المركب المرتبط.
مهاجمة الحمض النووي في الخلايا السرطانية والبكتيرية
تجاوز الباحثون دراسات الحمض النووي المنقى وفحصوا كيف يتصرف Cu3-TC-Py داخل الخلايا الحية. في مجموعات خلايا سرطانية، أظهرت الربطات الحرة التي تحتوي على مجموعات عطرية غنية بالنيتروجين تثبيط نمو أقوى بكثير مقارنةً بالتصاميم السابقة، وكان المركب النحاسي الكامل أكثر فاعلية، حيث قتل خطوط خلايا سرطانية متعددة عند تراكيز ميكرومولارية. كشفت قياسات النحاس داخل الخلايا أن Cu3-TC-Py ينقل النحاس بكفاءة إلى داخل الخلايا ويحفز تراكم الحمض النووي التالف، كما تم الكشف عنه بتقنية تصوير مدعومة بالتصليح التي تحدد الشوائب على خيوط الجينوم المشدودة. في البكتيريا، أظهرت الميكروسكوبية أن المعالجة أدت سريعاً إلى تعطيل الكروموسوم البكتيري المضغوط، مبعثرة الحمض النووي في جميع أنحاء الخلية ومماثلة للتفتت الشديد الذي تسببه مضاد حيوي قوي مُتلف للحمض النووي، متسقة مع دمار وراثي واسع النطاق.
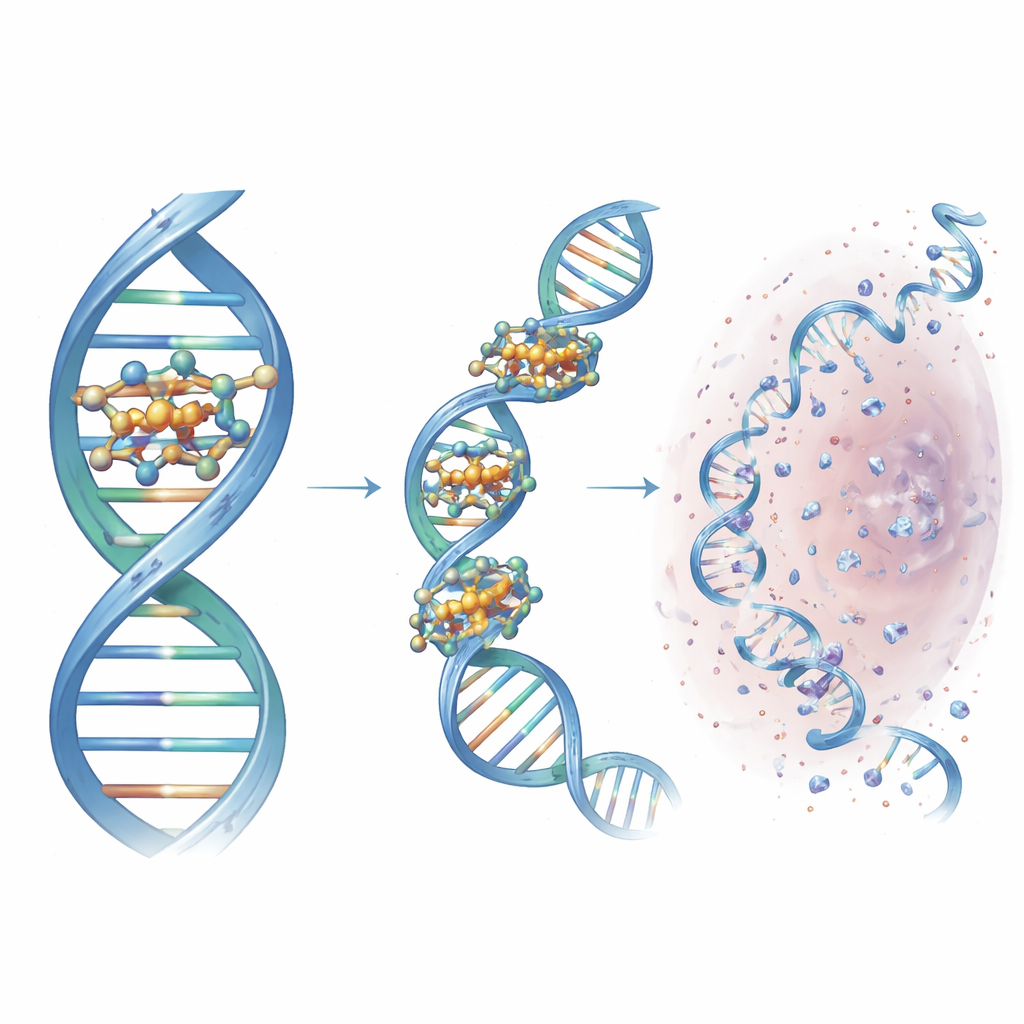
لماذا تهم هذه المقصات المصممة
لغير المتخصص، الرسالة الأساسية أن الباحثين حولوا قالباً بسيطاً وحدودياً من كيمياء الكليك إلى آلة قطع للحمض النووي مضبوطة بعناية. باختيار مجموعات نيتروجين حلقية مناسبة، أنشأوا مجموعة نحاسية مدمجة ترسو في أخدود محدد من الحمض النووي، تسحب الخيوط معاً وتولّد محلياً أنواع أكسجين تفاعلية تقطع اللولب المزدوج. هذا المركب الرائد، Cu3-TC-Py، يتلف الحمض النووي بكفاءة في كل من الخلايا السرطانية والبكتيرية ويظهر كيف يمكن للتصميم العقلاني أن يشحذ فعالية الأدوية القائمة على المعادن. ومع بقاء الكثير من العمل قبل الاستخدام السريري، ترسم الدراسة قواعد تصميم لمقصات جزيئية من الجيل القادم التي قد تقدم يوماً علاجات سرطانية أكثر استهدافاً واستراتيجيات مضادة للميكروبات مبتكرة.
الاستشهاد: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
الكلمات المفتاحية: كيمياء الكليك, تلف الحمض النووي, معقّدات النحاس, عوامل مضادة للسرطان, نيوكليازات اصطناعية