Clear Sky Science · ar
إعادة توظيف تطورية لمركب ثيولاز متعدِّد الأجزاء تمكّن تخليق مضاد حيوي
كيف تعيد الميكروبات اليومية اختراع كيميائها
العديد من المضادات الحيوية والأدوية التي نعتمد عليها تُصنَع بهدوء بواسطة البكتيريا. تستخدم هذه الكيميائيّات الصغيرة إنزيمات — آلات جزيئية — لبناء مركبات دفاعية معقَّدة. تكشف هذه الدراسة كيف أن إنزيمًا مركزيًا في الأيض، كان يُستخدم سابقًا لأعمال صيانة خلوية أساسية، أُعيد تأسيسه تطوريًا في بكتيريا الفم لصنع مضاد حيوي قوي. لا يقتصر فَهم هذا التحوّل على إظهار كيف تخترع الطبيعة كيمياء جديدة فحسب، بل يوفّر أيضًا دلائل لتصميم أدوية ومحفزات حيوية متقدِّمة.
من الأيض الأساسي إلى الأسلحة الكيميائية
تعتمد كل الخلايا الحية على مجموعة من الإنزيمات المحفوظة التي تُشغّل أيضها المركزي، مثل تحطيم الدهون وبناء الجزيئات الأساسية. إحدى هذه المجموعات، المسماة سوبرعائلة الثيولاز، تُساعد عادةً في التعامل مع جزيئات غنية بالطاقة مثل أسيتيل-كوإنزيم A وتدعم مسارات حيوية لصنع الدهون ومكوّنات خلوية أخرى. اكتشف المؤلفون أنه في عدة أنواع من ستربتوكوكس الفم، فقد مركّب ثلاثي الأجزاء القائم على الثيولاز — المكوَّن من بروتينات ذات صلة بـ HMGS وACAT وبروتين مساعد ثالث — دوره الأيضي الأسلفي. وبدلًا من ذلك، يكمل هذا المركب الآن تخليق مضاد حيوي يُدعى ريوترايكلين A، الذي يساعد هذه البكتيريا على التنافس في بيئة الفم المزدحمة.
نوع جديد من التفاعل الإنزيمي على هيكل مضاد حيوي
بإعادة بناء مركب الستربتوكوكس في المختبر وتزويده بمقدمة كيميائية مصنَّعة للريوترايكلين A، أظهر الباحثون أن المركب يؤدي تفاعلًا غير عادي لتكوين رابطة كربون–كربون معروفًا باسم ألكلة فرايدل–كرافتس C-ألكلة. بدلًا من ربط مجموعة الأسيتيل إلى الأكسجين كما تفعل العديد من الإنزيمات، يثبت المجموعة مباشرة على ذرة كربون في حلقة بيروليدين-2,4-ديون — جزء مهم من هيكل الريوترايكلين. يقبل المركب مانحَات أسيتيل طبيعية مثل أسيتيل-كوإنزيم A وعدة مانحات اصطناعية، ثم يمكنه حتى تشغيل التفاعل بالعكس، مفككًا الرابطة التي أنشأها. توسع هذه المرونة السجل المعروف لأسيليترات الأحياء وتلمّح إلى كيف يمكن تكييف مثل هذه الإنزيمات لبناء منتجات كيميائية متنوعة.
إعادة توظيف قالب بروتيني محفوظ
باستخدام مجهر إلكتروني بارد عالي الدقة، حَلَّ الفريق البنية ثلاثية الأبعاد لمركب الستربتوكوكس، المسمى SmaATase. على الرغم من وظيفته الجديدة، يحتفظ SmaATase بشبه معماري لافت لمركب ذي صلة في العتائق يشارك في طريق الميفالونات لتكوين ليبيدات الإيزوبرين. كلاهما تجمّعات متعددة الوحدات كبيرة مبنية من وحدات متكررة وتتميّز بتجويف مشترك حيث يمكن للكوإنزيم A أن يرتبط ويتحرك بين مواقع النشاط. ومع ذلك، فإن بقايا تحفيزية رئيسية كانت أساسية للتفاعل الأيضي الأصلي مفقودة أو مُعدَّلة في النسخة البكتيرية. وتؤكد الاختبارات الكيميائية الحيوية أن SmaATase لم يعد قادرًا على صنع المنتج الأسلفي HMG-CoA وبدلًا من ذلك يستخدم أسيتيل-كوإنزيم A كمانح فقط لركائزه الجزيئية الصغيرة الجديدة.
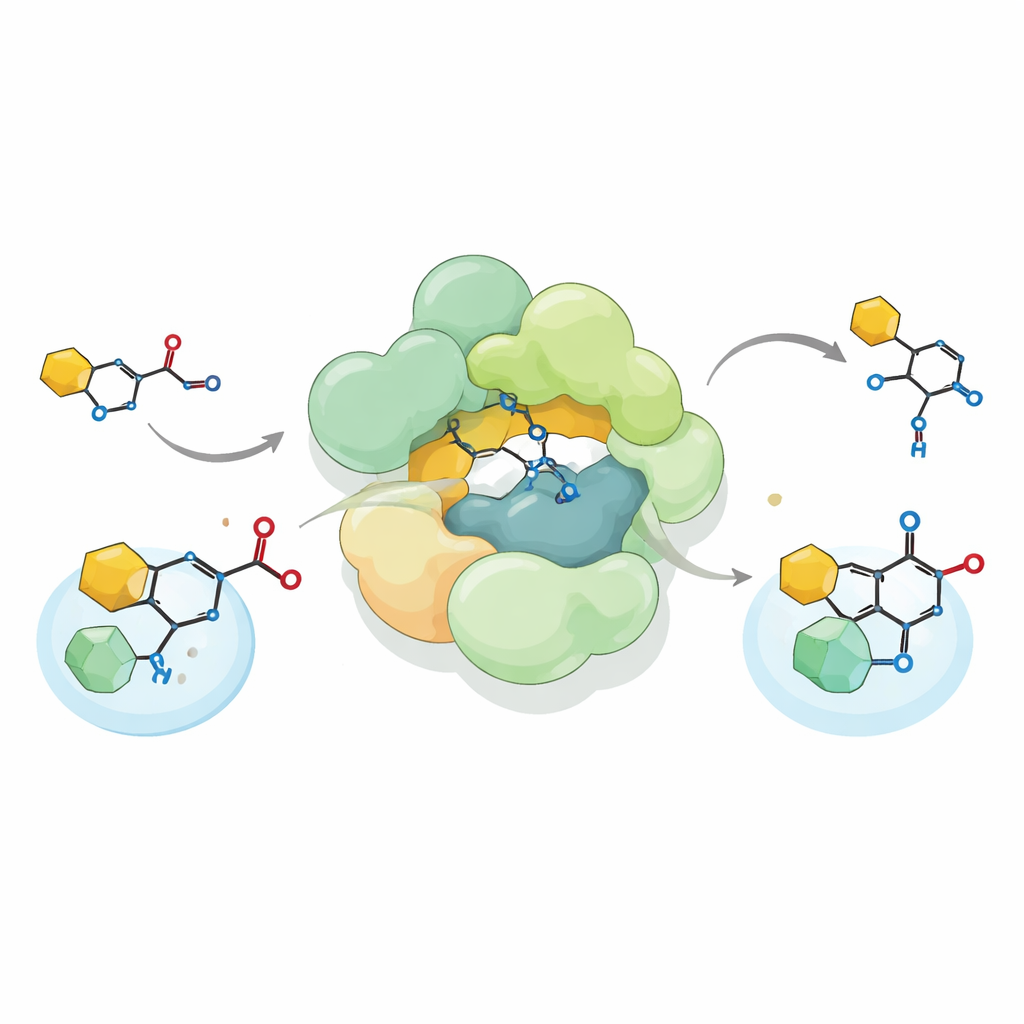
درب تطوري من الأيض إلى المضادات الحيوية
لفهم كيف قد تكون العملية التطورية قد تبلورت، قارن المؤلفون تسلسلات وأنشطة مركبات ذات صلة عبر العديد من البكتيريا والعتائق. حدّدوا أكثر من ألف عنقود جيني يحتوي على نفس الثلاثي من أنواع الإنزيمات. بعضها لا يزال يدعم الكيمياء التقليدية للثيولاز؛ أما أخرى، مثل تلك في الزائفية، فتغذي تخليق مضادات حيوية صغيرة مختلفة. يبدو أن مركبًا ممثلًا من Pseudomonas fluorescens يقف في منتصف هذا المسار التطوري: مجال HMGS الشبيه به مُعطّل، لكن وحدة ACAT الشبيهة به ما تزال تؤدي تفاعلًا أكثر تقليدية على ركائز مرتبطة بالكوإنزيم A. في SmaATase ونظيره في Pseudomonas الذي يصنع المركب الواقي للمحاصيل DAPG، أدت تغييرات إضافية حول موقع النشاط إلى تكييف الإنزيمات للتعرّف على مستقبلات غير قياسية مثل الحلقات العطرية أو نُوى حمض التترا مِيك.
لماذا تُحدِث مجموعة أسيتيل الصغيرة فرقًا كبيرًا
في النهاية، العائد البيولوجي لهذا التحول الجزيئي واضح. عندما اختبر الفريق المضادات الحيوية المؤستلة ريوترايكلين A وDAPG مقابل لوحة من البكتيريا موجبة الغرام، أظهرت هذه الجزيئات نشاط قتل قويًا، في حين أن سوابقها غير المؤستلة كانت أضعف بكثير أو شبه غير فعّالة. تلك المجموعة الأسيتيلية الصغيرة، الموضوعة في الموضع الصحيح تمامًا بواسطة المركب الإنزيمي المعاد توظيفه، تحوّل هيكلًا متواضعًا إلى سلاح قوي، مما يمكّن ستربتوكوكس في الفم أو زائفية حول جذور النباتات من التفوّق على جيرانهم. تبرز هذه العمل كيف يمكن للتطوّر إعادة تدوير أُطر إنزيمية قائمة مع طفرات طفيفة لكنها استراتيجية، محوِّلًا الآلات الأيضية الروتينية إلى أدوات متخصصة للدفاع الكيميائي — ومقدِّمًا مخططًا لمهندسين يأملون تصميم محفزات جديدة لتكوين روابط كربون–كربون لاكتشاف الأدوية والبيولوجيا التخليقية.
الاستشهاد: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
الكلمات المفتاحية: تطوُّر الإنزيمات, تخليق المنتجات الطبيعية, كيمياء المضادات الحيوية, إعادة توظيف استقلابية, ألكلة فرايدل-كرافتس