Clear Sky Science · ar
نماذج مستندة إلى الخلايا الجذعية المحوَّلة البشرية لالتهاب الرئوي التليفِي تكشف أن تثبيط p300/CBP يثبط حالة الخلايا الحويصلية الانتقالية
لماذا يهم تندب الرئتين الجميع
التليف الرئوي مجهول السبب (IPF) مرض قاسٍ تتحول فيه أنسجة الرئة تدريجيًا إلى نسيج ندبي، مما يجعل كل نفس أصعب. الأدوية الحالية يمكنها فقط إبطاء هذه العملية وغالبًا ما تسبب آثارًا جانبية مزعجة. تستخدم هذه الدراسة أدوات متقدمة في الخلايا الجذعية والجينومية لإعادة إنشاء رئات متندبة في المختبر، وتطرح سؤالًا بسيطًا لكنه حيوي: هل يمكننا إيجاد مفتاح يوجه الخلايا الرئوية المتضررة بعيدًا عن حالة ضارة وإلى طريق الشفاء؟
نافذة مزروعة بالمختبر على رئة متندبة
لدراسة IPF، بنى الباحثون رئات مصغرة من خلايا جذعية بشرية مُحوَّلة (iPSCs). تم توجيه هذه الخلايا لتصبح خلايا حويصلية—الخلايا التي تبطن الحويصلات الهوائية الصغيرة حيث يدخل الأكسجين إلى الدم—ونمت معًا مع الخلايا الليفية الرئوية، خلايا النسيج الضام التي تشكل الندبة. مغروسة في مادة هلامية لينة، عملت هذه "الأورغانويدات الحويصلية" بشكل مشابه لأنسجة الرئة الحقيقية. عند تعريضها لمادة البليوميسين الكيميائية—التي تُعرف كمحفز لإصابة الرئة—انكمش الهلام نتيجة شد الخلايا الليفية عليه، مقلدًا انكماش الأنسجة الذي يُرى في التليف.
باستخدام هذا النظام، فحص الفريق مكتبة مؤلفة من 264 جزيءًا صغيرًا وقاسوا تلقائيًا مدى منع كل مركب لانكماش الهلام، مع أداة تحليل صور مدعومة بتعلّم عميق لضمان قراءات موضوعية. لم يكن لمعظم المركبات أي تأثير، لكن عائلة واحدة برزت بوضوح: مثبطات بروتينَي p300 وCBP، اللذان يساعدان في التحكم بكيفية تغليف الحمض النووي وما هي الجينات النشطة. جميع المركبات الثمانية المستهدفة لـ p300/CBP في المكتبة خفّضت الانكماش بجرعات منخفضة، مما يبرز هذا المسار كمقبض واعد للتأثير على التليف. 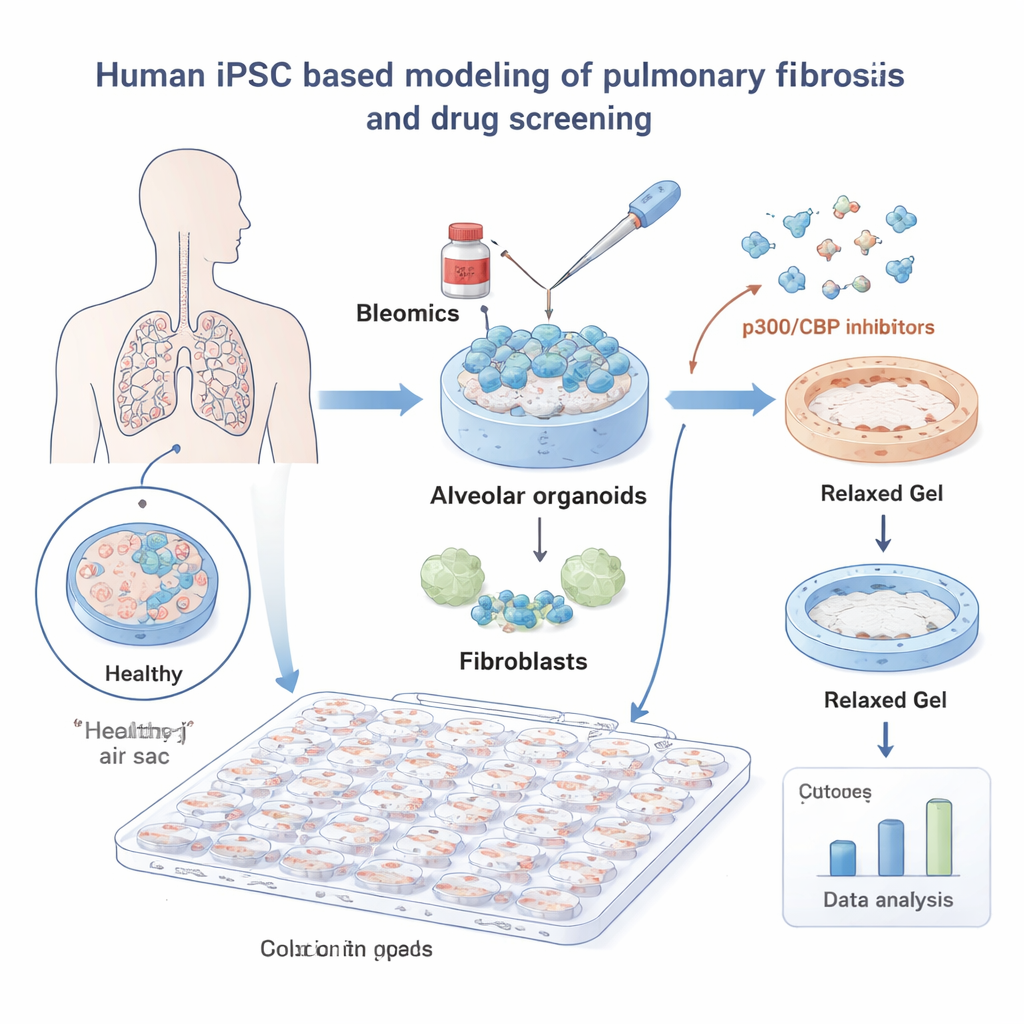
المسببون: الخلايا الرئوية الانتقالية
كشفت أعمال حديثة عن نوع خلوي مشكل في الرئات المريضة يُسمى حالة الخلايا الحويصلية الانتقالية. عادةً، تتحول الخلايا الداعمة المعروفة باسم خلايا AT2 إلى خلايا AT1 رفيعة جدًا تغطي الحويصلات وتمكّن تبادل الغازات. في IPF، تتعطل خلايا AT2 غالبًا في هذه الحالة الانتقالية، معبرةً عن جينات الإجهاد والإصلاح بينما تفشل في إكمال التحول إلى خلايا AT1 وظيفية تمامًا. تتجمع هذه الخلايا الانتقالية في المناطق المتليفَة وتتواصل بقوة مع الخلايا الليفية، لكن لم يكن واضحًا ما إذا كانت مجرد نتيجة جانبية للضرر أم محركات نشطة للتندب.
من خلال تسلسل الرنا وتوصيف الكروماتين المفتوح في أورغانويداتهم، أظهر المؤلفون أن الخلايا الانتقالية الناشئة في نموذجهم طابقت عن كثب تلك الموجودة في رئات مرضى IPF. عرضت هذه الخلايا الانتقالية المحفَّزة توقيعات جينية للإجهاد والالتهاب وإعادة تشكيل المصفوفة، وقامت بتنشيط الخلايا الليفية الرئوية المتشاركة بقوة. والأهم، عندما تم حجب p300/CBP، تراجعت علامات الحالة الانتقالية، حافظت هوية AT2 على نفسها بشكل أفضل، وتراجع تنشيط الخلايا الليفية. بعبارة أخرى، لم تكن الأدوية سامة للخلايا بشكل عام؛ بل منعت بشكل انتقائي خلايا AT2 من الوقوع في هذا المأزق الضار.
فك شيفرة مفاتيح الجزيئات
لفهم كيف يؤثر p300/CBP على قرار المصير هذا، فحص الفريق العلامات الكيميائية على الهستونات—البروتينات التي تساعد في تغليف الحمض النووي. علامة معينة، أسيتلة H3K27، عادةً ما يضعها p300/CBP عند المحسّنات والمروّجات النشطة. في الخلايا الانتقالية، حملت المناطق القريبة من جينات الاستجابة للإجهاد والجينات المؤيدة للتليف أسيتلة H3K27 قوية وكانت غنية بمواقع ربط لعوامل النسخ مثل AP‑1 وHNF1B. عند معالجة الخلايا بمثبطات p300/CBP، تضاءلت هذه العلامات الأسيتيلية في تلك المواقع، وانخفض التعبير عن العديد من الجينات المؤيدة للتليف. كذلك، أدى حجب AP‑1 مباشرة أو خفض AP‑1 وHNF1B بواسطة RNA صغيرة متداخلة إلى تقليص البرنامج الانتقالي وانكماش الأورغانويد، راسخًا صِلة هذا الثلاثي—p300/CBP وAP‑1 وHNF1B—بالمحرك الذي يغذي إعادة تشكيل النسيج التليفي.
خارج الصحن، اختبرت الدراسة أحد المثبطات، CBP30، في فئران تعرضت لإصابة رئوية ناجمة عن البليوميسين. أظهرت الحيوانات المعالجة بـ CBP30 خلايا ظهارية انتقالية أقل، وتنشيطًا أقل للمايوفبروبلاستات المكونة للندبة، وتعبيرًا مخففًا لعلامات التليف. يعزز هذا التحقق المتقاطع بين نماذج الخلايا الجذعية البشرية والنموذج الحيواني الحجة القائلة بأن p300/CBP ليس مجرد أثر مختبري بل منظم حقيقي لتندب الرئة. 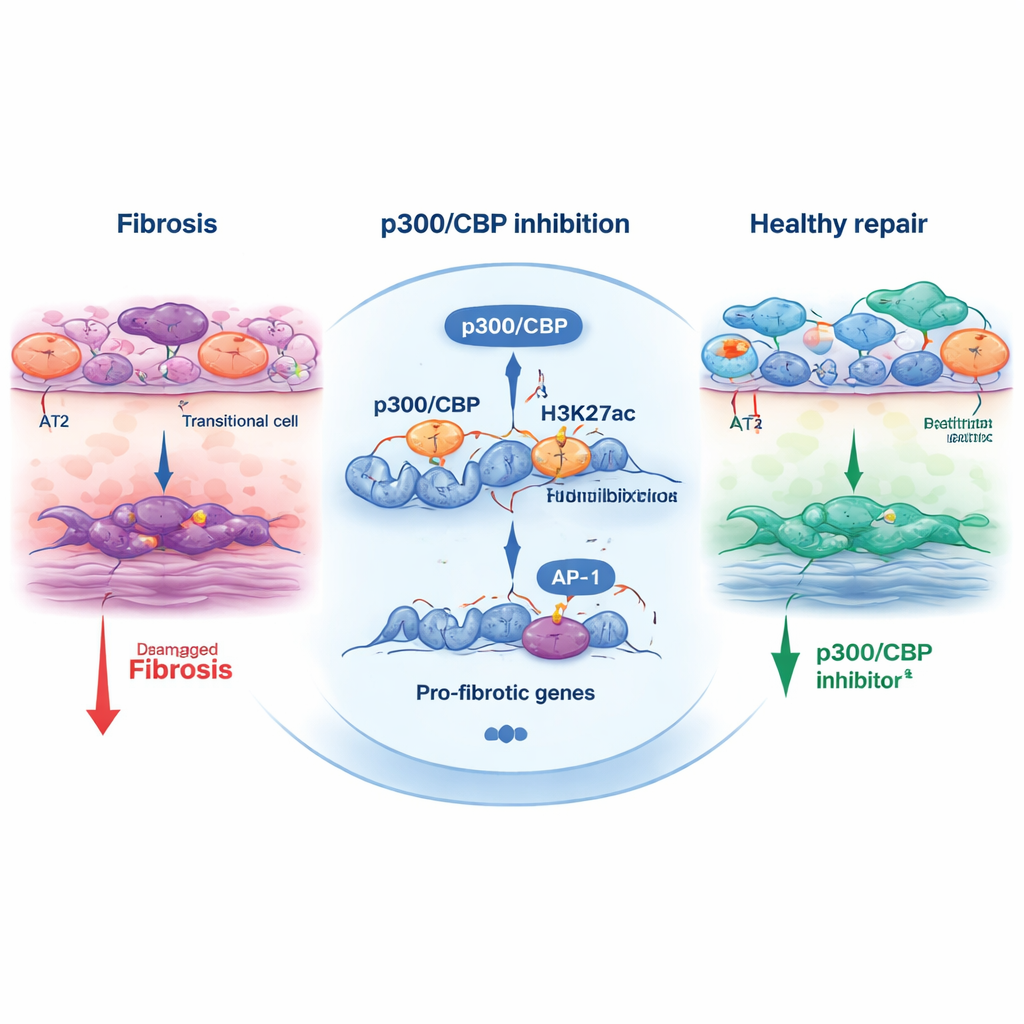
ماذا يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الخلاصة الأساسية هي أن الباحثين بنوا نموذجًا بشريًا واقعيًا للرئات المتليفة واستخدموه لتسليط الضوء على هدف دوائي جديد. تشير نتائجهم إلى أن تندب الرئة يقوده جزئيًا حالة خلوية انتقالية قابلة للعكس ومحفَّزة بالإجهاد تُضلّل النسيج المحيط. عن طريق تخفيف نشاط p300/CBP، قد يكون من الممكن تهدئة هذه الحالة، والحفاظ على تطور الخلايا الحويصلية في مساره الصحي، وتقليل الإشارات التي تدفع الخلايا الليفية إلى فرط النشاط. وبينما لا تزال مثبطات p300/CBP بحاجة إلى تحسين للسلامة واختبار سريري، تشير هذه الدراسة إلى علاجات تعالج سوء التواصل الخلوي الجذري في IPF بدلًا من مجرد إبطاء عواقبه.
الاستشهاد: Tsutsui, Y., Masui, A., Konishi, S. et al. Human iPSC-based Modeling of Pulmonary Fibrosis Reveals p300/CBP Inhibition Suppresses Alveolar Transitional Cell State. Nat Commun 17, 1214 (2026). https://doi.org/10.1038/s41467-026-68909-z
الكلمات المفتاحية: التليف الرئوي مجهول السبب, أورغانويدات الحويصلات الرئوية, مثبطات p300/CBP, الخلايا الظهارية الانتقالية, خلايا جذعية رئوية