Clear Sky Science · ar
هندسة البلازميدات مع أصول تكرار تركيبية
لماذا يهم إعادة كتابة DNA الميكروبات
تعتمد العديد من أدوات التكنولوجيا الحيوية الحديثة، من إنتاج الإنسولين إلى دوائر الجينات المتقدمة، على حلقات صغيرة من الحمض النووي تُدعى البلازميدات. تعمل هذه العناصر الجينية كحاملات لنقل الجينات المعدّلة إلى البكتيريا، لكن تصميمها الأساسي لم يتغير تقريبًا منذ عقود. تُظهر هذه الدراسة أن جوهر البلازميدات نفسه — التسلسلات التي تخبر الخلايا متى وبأي تكرار يجب أن تنسخها — يمكن إعادة تصوُّره بالكامل. من خلال إعادة بناء "محرك النسخ" هذا من الصفر، يبتكر الباحثون بلازميدات أسهل في الضبط والدمج والبرمجة، ما يفتح الباب أمام تشخيصات أكثر مرونة وتصنيعًا حيويًا مطوَّرًا وتطبيقات في علم الأحياء التركيبي.
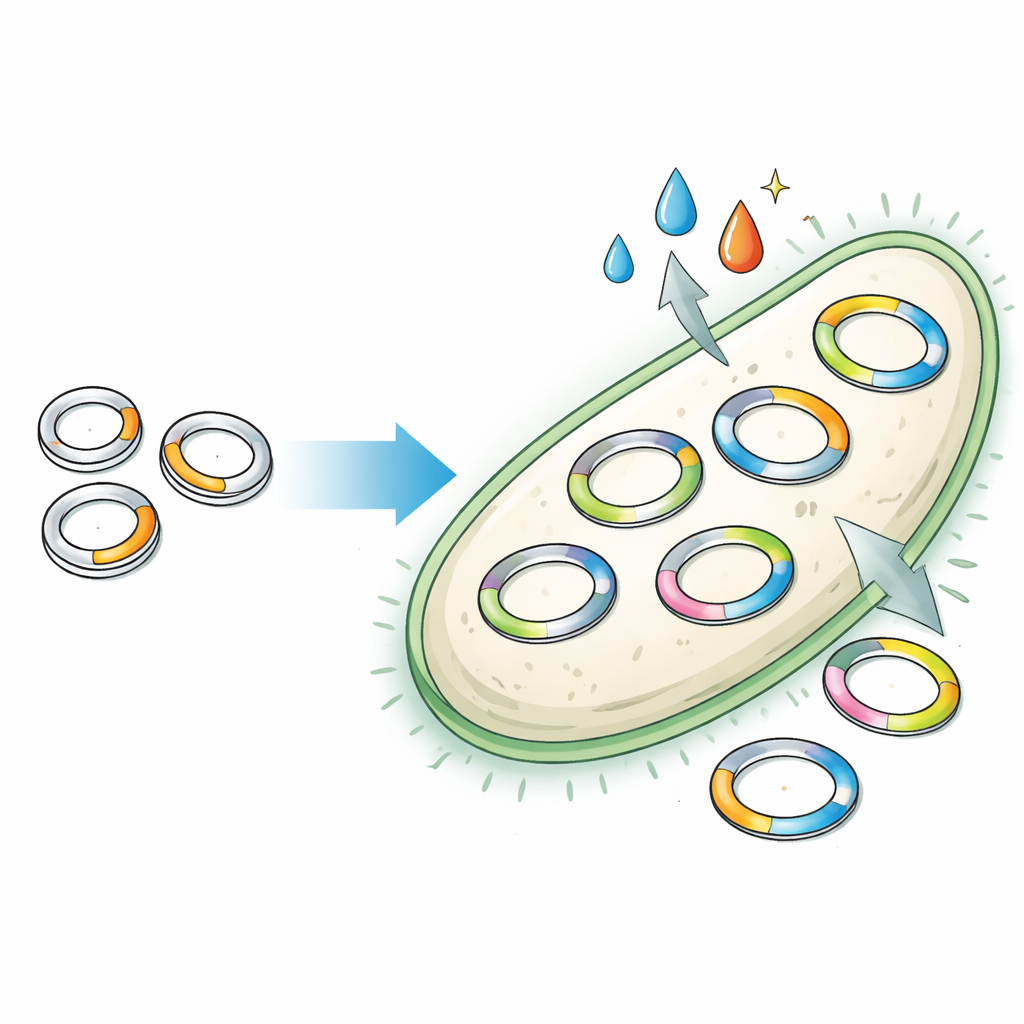
أدوات قديمة بحدود خفية
تطورت البلازميدات طبيعيًا كحمض نووي متنقل يساعد البكتيريا على تبادل صفات مثل مقاومة المضادات الحيوية أو طرق جديدة لهضم مصادر الغذاء. في المختبر، يستعير المهندسون هذه البلازميدات لحمل جينات مفيدة، لكن معظمها يعتمد على تصاميم كلاسيكية قليلة اكتشفت في ثمانينيات القرن الماضي. تخفي هذه التصاميم القديمة تشابكًا من الأجزاء الجينية المتداخلة التي تتحكم في عدد نسخ البلازميد داخل كل خلية وما إذا كانت البلازميدات المختلفة يمكن أن تتعايش بسلام. وبما أن هذه الأجزاء ملتحمة، فإن تغيير ميزة واحدة قد يكسر أخرى بشكل غير متوقع. ونتيجة لذلك، يقتصر العلماء على قائمة قصيرة من البلازميدات ذات أعداد نسخ ثابتة وتوافق محدود، ما يقيّد مدى تعقيد الأنظمة المهندسة.
إعادة بناء محرك النسخ من الصفر
ركز الباحثون على منشأ نسخ مستخدم على نطاق واسع من عائلة بلازميدات pMB1. في صورتها الطبيعية، يستخدم هذا المنشأ حوارًا متوازنًا بين اثنين من جزيئات الحمض النووي الريبوزي — واحد يبدأ نسخ الحمض النووي وآخر يوقفه — للحفاظ على عدد نسخ البلازميد ضمن الحدود. بدأ الفريق أولًا بـ"إعادة تنظيم" هذا النظام: فصلوا الجينات المتداخلة، عطّلوا محفزًا مدفونًا، ووضعوا القطع الرئيسية على خرائط جينية منفصلة ونظيفة. هذا وحده أظهر أن مهمة المنشأ الجوهرية يمكن الحفاظ عليها مع تبسيط التخطيط، محولًا جزءًا معقّدًا مشكّلًا بفعل التطور إلى شيء أقرب إلى آلة معيارية بمكونات يسهل الوصول إليها.
استبدالها بمقابض تحكم تركيبية
بما أن منطق التحكم الأصلي أصبح مكشوفًا، استبدله المؤلفون بمنظمات تركيبية بالكامل. ربطوا مُمهِّد النسخ بمفاتيح RNA هندسية تعمل كأذرع تعتيم: يمكن لـ RNAات التحكم الصغيرة قلب هذه المفاتيح للسماح أو منع إنتاج الممهِّد وبالتالي التحكم في نسخ البلازميد. من خلال اختيار متغيرات مفاتيح مختلفة وإقرانها بمحفزات بقوى متفاوتة، ضبطوا عدد نسخ البلازميد عبر أكثر من درجتين من الحجم (أكثر من مئتي ضعف). كما استكشفوا ترتيبات فيزيائية مختلفة لكاسِتات التحكم على الحمض النووي، فاكتشفوا ترتيبات حسّنت الاستقرار وأتاحت لهم تقليص منطقة التكرار إلى نواة عملية مدمجة أثناء إضافة أنظمة مساعدة طبيعية تمنع تشابك البلازميدات المعيب.
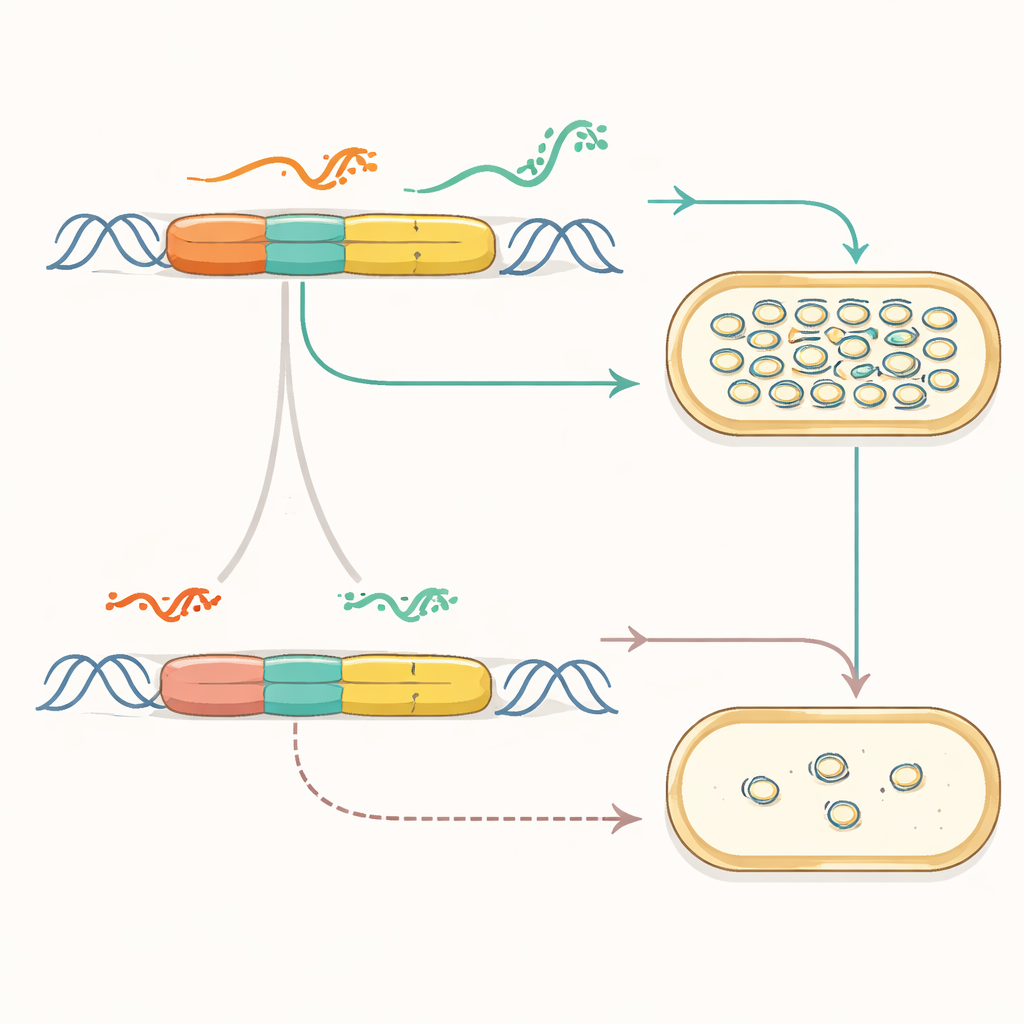
تحويل الإشارات الكيميائية إلى أعداد DNA
بمجرد أن أصبح محرك النسخ معياريًا، أظهر الفريق أنه يمكن توصيله للاستشعار من العالم الخارجي. ربطوا المنشأ التركيبي بمحفزات قابلة للتحفيز وهياكل RNA تسمى ريبوسويتشات، التي تغير شكلها استجابة لجزيئات صغيرة. في هذه البلازميدات الجديدة، أدى إضافة مادة كيميائية مثل IPTG أو الكوميت إلى ارتفاع أو انخفاض عدد نسخ البلازميد — وبالتالي إشارة تقريرية. يمكن دمج إشارات متعددة بحيث يدفع مادة كيميائية عملية النسخ بينما تكبح أخرى إيقافها. بنى الباحثون حتى أزواجًا من البلازميدات، كل منها يستجيب لمادة كيميائية مختلفة، وتتبعوا أعداد نسخها المتغيرة في نفس الخلية باستخدام تسلسل الحمض النووي، فحوّلوا فعليًا أعداد البلازميدات إلى شيفرة شريطية لتاريخ التعرض البيئي.
العديد من البلازميدات المخصصة في خلية واحدة
كان اختبارًا مهمًا لهذا النهج هو ما إذا كان من الممكن أن تتعايش عدة بلازميدات تتحكم فيها أنظمة مستقلة. بالاستعانة بمكتبة من منظمات RNA متعامدة، بنى الفريق ستة بلازميدات مختلفة، كل واحد بمنشاه التركيبي ومؤشر مقاومة مختلف للمضاد الحيوي، وأدخلوها جميعًا معًا إلى E. coli. أكدت عمليات تسلسل البلازميد الكامل على مدى عدة أيام بقاء الستة جميعها حاضرَة، رغم أن توزعاتها النسبية تغيّرت. فشلت المحاولات للقيام بالشيء نفسه مع ستة بلازميدات تقليدية، مما يبرز كيف أن التصميم المعاد تنظيمه وأنظمة الاستقرار المضافة تجعل البلازميدات الجديدة أكثر توافقًا ومتانة عند اكتظاظها معًا داخل خلية واحدة.
ما الذي يعنيه هذا لمستقبل التكنولوجيا الحيوية
لغير المتخصصين، الخلاصة واضحة: حوّل المؤلفون البلازميدات من أدوات جامدة بمقاس واحد تناسب الجميع إلى منصة قابلة للتخصيص. تعمل أصول النسخ التركيبية لديهم كمحركات قابلة للتوصيل والتشغيل يمكن اختيار سرعتها وحساسيتها ومدخلاتها حسب الطلب. هذا يجعل من الممكن بناء بكتيريا تسجل التعرضات الكيميائية كتغيرات في عدد نسخ الحمض النووي، واختبار مسارات جينية عديدة بالتوازي عن طريق توزيعها عبر بلازميدات متعددة، أو موازنة النمو والإنتاج بدقة في سلالات صناعية. وعلى الرغم من بقاء بعض مقايضات الاستقرار، تُظهر هذه الدراسة أن آليات تكرار البلازميد الأساسية لم تعد محجوبة عن الهندسة، فاتحةً مجالًا جديدًا للابتكار في علم الأحياء التركيبي.
الاستشهاد: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
الكلمات المفتاحية: بلازميدات تركيبية, منشأ النسخ, منظمات الحمض النووي الريبوزي, ضبط عدد النسخ, علم الأحياء التركيبي