Clear Sky Science · ar
مستقبل حمض السكسينات 1 يقيّد التكوّن الدموي ويمنع تقدم اللوكيميا النخاعية الحادة
عندما ينحرف وقود الخلية
يُجدَّد دمنا باستمرار بواسطة مجموعة صغيرة من الخلايا الجذعية المخفية في نقي العظام. تستكشف هذه الدراسة كيف يعمل ناتج أيضي شائع، السكسينات، ومستقبله على غشاء الخلية كفرامل لهذا النظام التجديدي. عندما تتعطل هذه الفرملة، يمكن أن تنقلب المعادلة بين إنتاج دم سليم ونمو سرطاني نحو اللوكيميا النخاعية الحادة (AML)، سرطان دم عدواني. قد يؤدي فهم هذا المفتاح الخفي للضبط إلى علاجات أكثر دقة تكبح المرض عبر استعادة آليات الحماية الذاتية في الجسم.
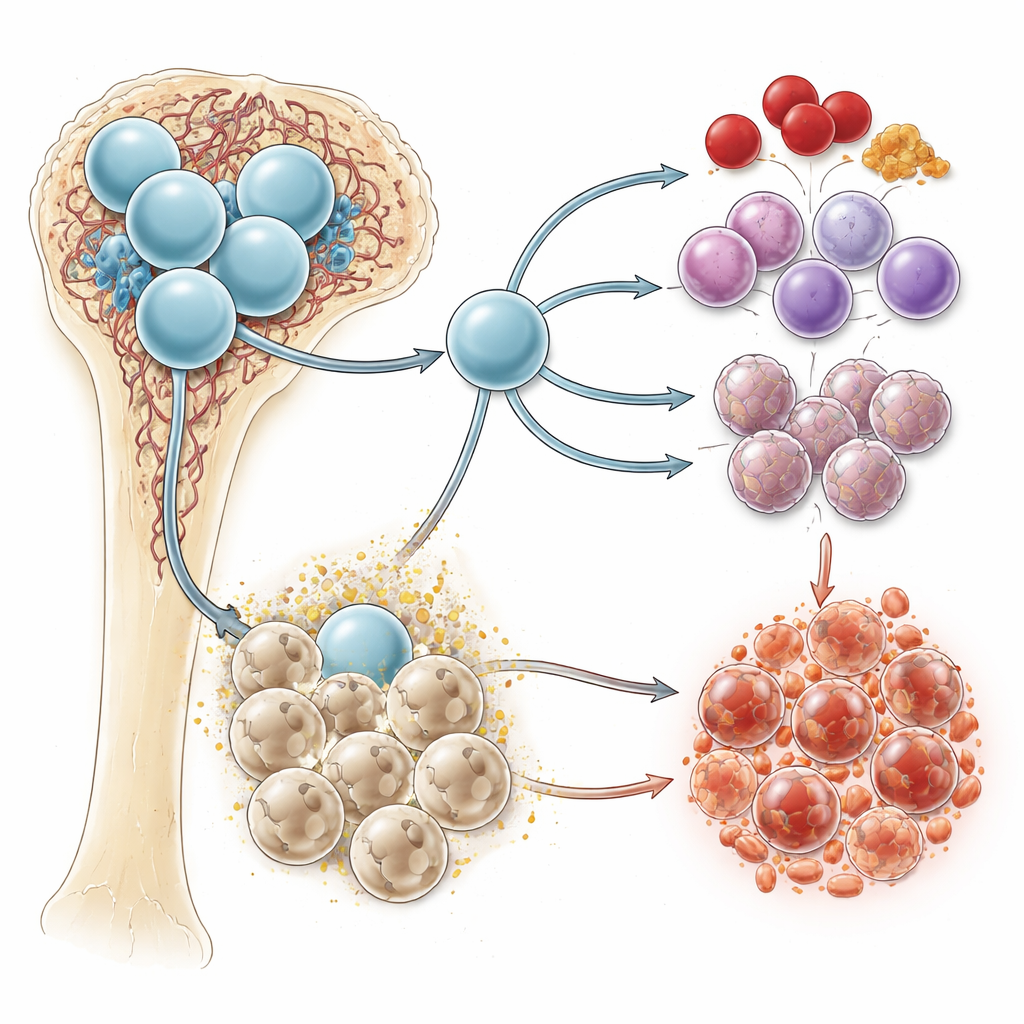
إشارة كيميائية ذات حياة مزدوجة
السكسينات هو ناتج جانبي روتيني لمدى احتراق الخلايا للوقود، لا سيما داخل الميتوكوندريا، محطات طاقة الخلية. في ظروف انخفاض الأكسجين — كما يحدث في نقي العظام — يميل السكسينات إلى التراكم. يمكن أن يعمل داخل الخلايا، مغيرًا الأيض والاستجابات الالتهابية، ويمكن أن يخرج أيضًا ليعمل كإشارة خارج الخلية. على سطح الخلية، يكتشف مستقبل يُدعى SUCNR1 وجود السكسينات وينقل الإشارة إلى الداخل. ربطت أعمال سابقة بين السكسينات وSUCNR1 والالتهاب والبيئات المواتية للسرطان، لكن دورهما المباشر في تكوّن الدم واللوكيميا لم يكن واضحًا.
علامة تحذّر لدى مرضى اللوكيميا
حلّل الباحثون بيانات التعبير الجيني لمئات مرضى AML واكتشفوا أن مستويات SUCNR1 تختلف اختلافًا واسعًا بين الأفراد. المرضى الذين كانت خلايا اللوكيميا لديهم تنتج كميات ضئيلة من SUCNR1 عاشوا مدة إجمالية وفترات خالية من التقدم أقصر، حتى بعد ضبط العوامل مثل العمر والجنس والأنواع السريرية القياسية. أظهرت بعض المجموعات الجينية للـ AML انخفاضًا ملحوظًا في SUCNR1. عندما زرع الفريق خلايا AML بشرية تفتقر إلى SUCNR1 في فئران ناقصة المناعة، ثم حقن الحيوانات بحمض السكسين (الذي يتحوّل إلى سكسينات في الجسم)، ازداد العبء اللوكيمي في نقي العظام. يشير ذلك إلى أنه في الأورام منخفضة SUCNR1 قد يساهم السكسينات الإضافي في تقدم المرض بدلًا من كبحه.
الفرملة الخفية على خلايا الدم الجذعية
لفهم كيفية عمل SUCNR1 في تكوّن الدم الطبيعي، لجأ العلماء إلى فئران معدلة وراثيًا. عندما حُذِف SUCNR1 إما في الحيوان ككل أو فقط في الخلايا المكوّنة للدم، صار نقي العظام مفرط النشاط. توسع عدد الخلايا الجذعية والنسليات، وزاد تعداد الخلايا النخاعية (مثل الوحيدات والعدلات) والخلايا البائية في الدم والطحال. نجت هذه الخلايا الشبيهة بالجذعية بشكل أفضل وشكلت مستعمرات أكثر في أطباق المختبر، رغم أنها كانت أقل قليلًا قدرة على إعادة تأسيس إنتاج الدم عند زرعها في منافسة مع خلايا طبيعية. أظهر خط فئران مراسل خاص أن مجموعة فرعية فقط من الخلايا الجذعية والنسلية تُعبّر فعلاً عن SUCNR1؛ وكانت هذه الخلايا الإيجابية لـ SUCNR1 ذات قدرة زرع محدودة بشكل خاص. عمومًا، عمل المستقبل كقيد على حجم ونشاط مستودع الخلايا الجذعية.
من دفاع متوازن إلى اندفاع التهابي مفرط
كشف تحليل مفصّل للتعبير الجيني في الخلايا الجذعية والنسلية التي تفتقد SUCNR1 تبدلًا واضحًا. خفتت بصمات الخلايا الجذعية الصامتة والبدائية، في حين ارتفعت جينات مرتبطة بالالتهاب وأنواع الأكسجين التفاعلية والخلايا الدموية الناضجة. برزت جزيئتان: S100A8 وS100A9، زوج من «المنبِّهات» التي تضخّم الإشارات الالتهابية. زادت هذه العوامل داخل حجرة الخلايا الجذعية وفي سائل نقي العظام المحيط. عندما عالج الفريق فئرانًا ناقصة SUCNR1 بعقار تاسكينيومود، وهو دواء يثبط إشارات S100A9، انقلب التوسع الزائد للخلايا الجذعية والنسلية وإفراط إنتاج الخلايا النخاعية والبائية إلى حد كبير. بعبارة أخرى، يمكن التراجع عن كثير من الأضرار المترتبة على فقدان SUCNR1 عبر قطع حلقة إنذار S100A8/S100A9.
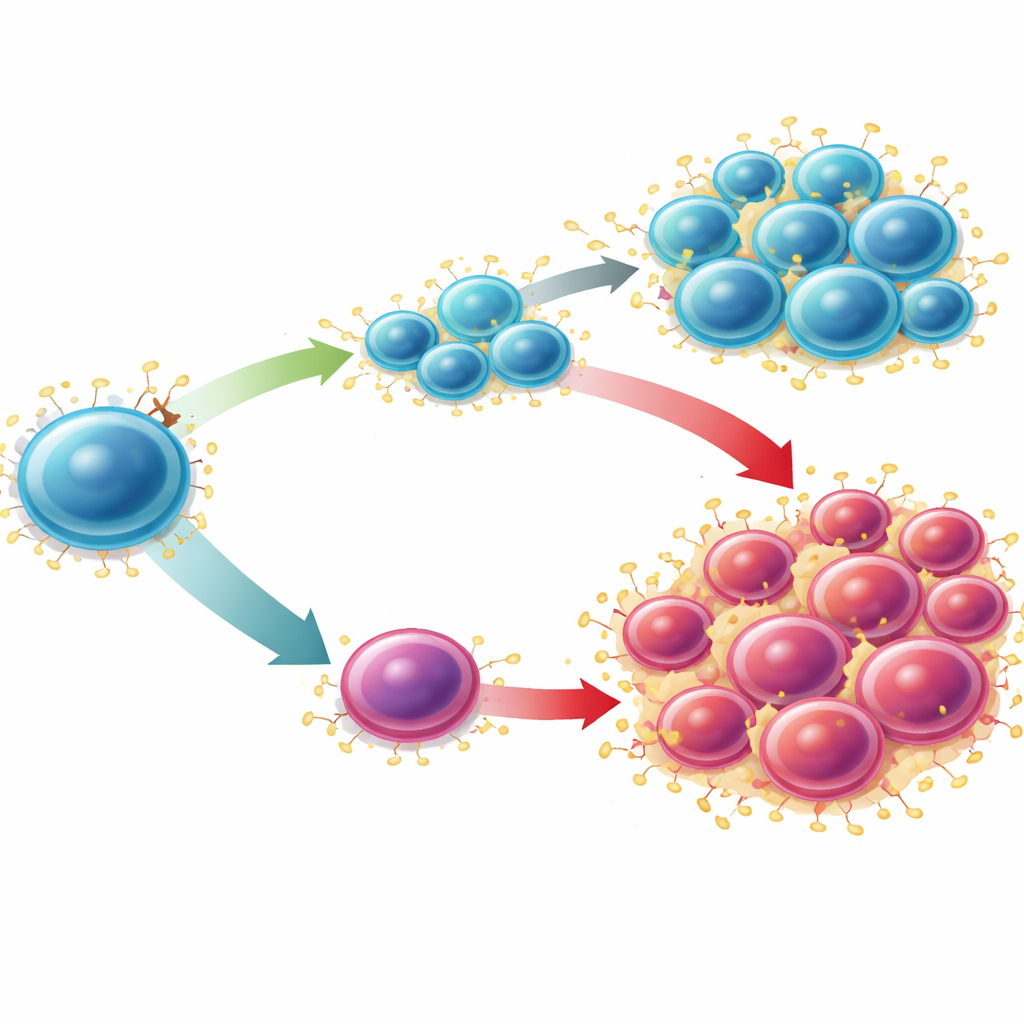
تحويل نقطة ضعف إلى استراتيجية علاجية
ثم تساءل العلماء عما إذا كان يمكن استغلال هذا المسار علاجيًا في AML. في نموذج اللوكيميا العدواني المدفوع طفرة MLL-AF9 — حيث تكون مستويات Sucnr1 منخفضة جدًا — أدى حجب S100A9 بتاسكينيومود، خاصة عند الجمع مع مركب منشط قوي لـ SUCNR1، إلى تقليل الخلايا الجذعية الشبيهة باللوكيميا وخفض عبء المرض في نقي العظام والطحال. أظهرت تحليلات بيانات RNA أحادية الخلية من نماذج AML البشرية المعالجة بعقار السيتارابين أن العناقيد المقاومة كانت غنية بـ S100A8 وS100A9، بينما كان SUCNR1 نادرًا ومرتبطًا بمجموعة أيضية نشطة تقلصت بعد العلاج. في خطوط خلايا اللوكيميا البشرية، زاد تفعيل SUCNR1 من موت الخلايا الناتج عن العلاج الكيميائي وكان قادرًا على تحريض الاستماتة بمفرده عند فرْط إنتاج SUCNR1. معًا تضع هذه النتائج انخفاض SUCNR1 ليس فقط كعلامة لتوقع سئ، بل أيضًا كضعف: خلايا اللوكيميا التي تخلّت عن هذه الفرملة قد تعتمد بشكل كبير على محور S100A8/S100A9 وتكون حساسة بشكل خاص للاستراتيجيات التي تعيد تفعيل إشارات SUCNR1 أو تحجب إنذارها اللاحق.
للقارئ العام، الرسالة المركزية هي أن ناتجًا أيضيًا يبدو عاديًا، السكسينات، ومستقبله SUCNR1 يشكّلان نظام أمان غير متوقع في تكوّن الدم. عندما يكون SUCNR1 موجودًا ونشطًا، يحافظ على ضبط الخلايا الجذعية ويمنع النمو المفرط. عندما يفقد SUCNR1 أو يكون منخفضًا — وهو شائع لدى بعض مرضى AML — يمكن أن يدفع السكسينات والمنبهات الالتهابية مثل S100A8 وS100A9 الخلايا الجذعية والنسلية نحو التوسع المفرط واللوكيميا. من خلال الجمع بين أدوية تُقلّل هذا الإنذار الالتهابي وعوامل تعيد أو تحاكي إشارات SUCNR1، قد يكون من الممكن إعادة النظام إلى حالة توازن إنتاج الدم وتحسين فعالية العلاجات الكيمياوية القائمة.
الاستشهاد: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, مستقبل السكسينات, خلايا جذعية مكونة للدم, الأيض والسرطان, إشارات الالتهاب