Clear Sky Science · ar
أكسيدازات كحول مهندَسة تحفّز التبادل الأسيتري في وسط مائي دون تحلل تنافسي
لماذا تهمّ هذه القصة الإنزيمية
تعتمد العديد من المنتجات اليومية، من الأدوية ونكهات الطعام إلى الديزل الحيوي، على نوع بسيط من الروابط الكيميائية يسمى الإستر. يعد تصنيع هذه الإسترات وتعديلها بكفاءة وتكلفة منخفضة وبطرق صديقة للبيئة هدفاً أساسياً في الكيمياء الخضراء. التحدّي هو أن الماء، الذي يُعَد المذيب المثالي من حيث السلامة والاستدامة، غالباً ما يخرب هذه التفاعلات بتفكيك الإسترات بسرعة تعادل أو تفوق سرعة تكوينها. تكشف هذه الدراسة عن إنزيم مهندَس قادر على بناء الإسترات في الماء مع تجاهل شبه كامل للماء المحيط به، ما يفتح مسارا لكيمياء صناعية أنظف.
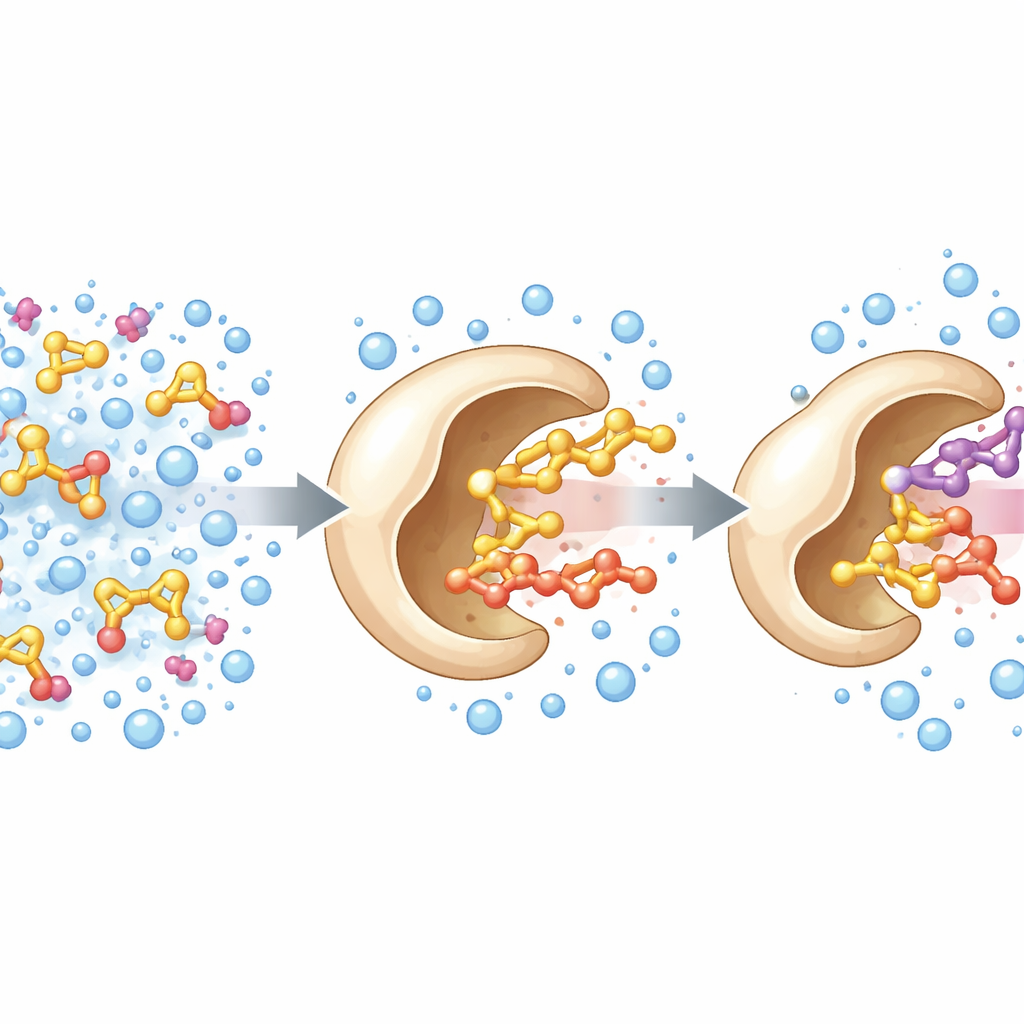
تحويل إنزيم معروف إلى وظيفة جديدة
انطلق الباحثون من إنزيم معروف، أكسيداز كحول مصدره فطر متحلل للخشب. في الطبيعة، يستخدم هذا الإنزيم عامل فلافين المساعد لسحب إلكترونات من كحولات صغيرة مثل الميثانول. سعى الفريق إلى توسيع نطاق نشاطه ليشمل كحولات أكثر ضخامة، ذات صلة أكبر بالمواد الكيميائية الرفيعة والنكهات. مستفيدين من البنية ثلاثية الأبعاد للإنزيم كخارطة طريق، ركزوا على ثلاثة أحماض أمينية تشكل ما يشبه بوابة دخول إلى الموقع الفعّال. من خلال تبديل عشوائي لهذه المواضع وفحص المتغيرات الناتجة، اكتشفوا طفرة ثلاثية سُميت PcAOx‑VPN تستطيع معالجة كحولات أكبر بكفاءة مثل البنزيل كحول مع فقدان كبير في نشاطها الأصلي تجاه كحولات صغيرة مثل الميثانول.
موهبة غير متوقعة: بناء الإسترات في الماء
أثناء اختبار PcAOx‑VPN في خليطات مصممة لإذابة ركائز زيوتية، لاحظ الفريق قمماً إضافية في قراءاتهم التحليلية. تبين أن هذه كانت منتجات أسيتيلية: كان الإنزيم ينقل مجموعة أسيل من مانح أسيل منشط إلى الكحولات، تفاعل يُعرف بالتبادل الأسيتري. والأمر اللافت أن هذا جرى في وسط مائي معتمد على المحلول العازل، وهو ما عادةً ما يؤدي إلى تحلل مائي تنافسي قوي حيث يهاجم الماء الإستر ويدمّره. هنا، جمع PcAOx‑VPN الكحولات ومانحي الأسيل مثل أسيتات الفينيل لتشكيل إسترات جديدة بكفاءة، غالباً بعوائد تفوق 80%، ومع تفاعلات جانبية متواضعة فقط. كما استطاع نفس الإنزيم العمل على مجموعة واسعة من الكحولات، بما في ذلك السلاسل المستقيمة والعطرية والمهتمية والسابحة بالكبريت، وأظهر تفضيلاً واضحاً لشكل مرايا على الآخر في عدة حالات.
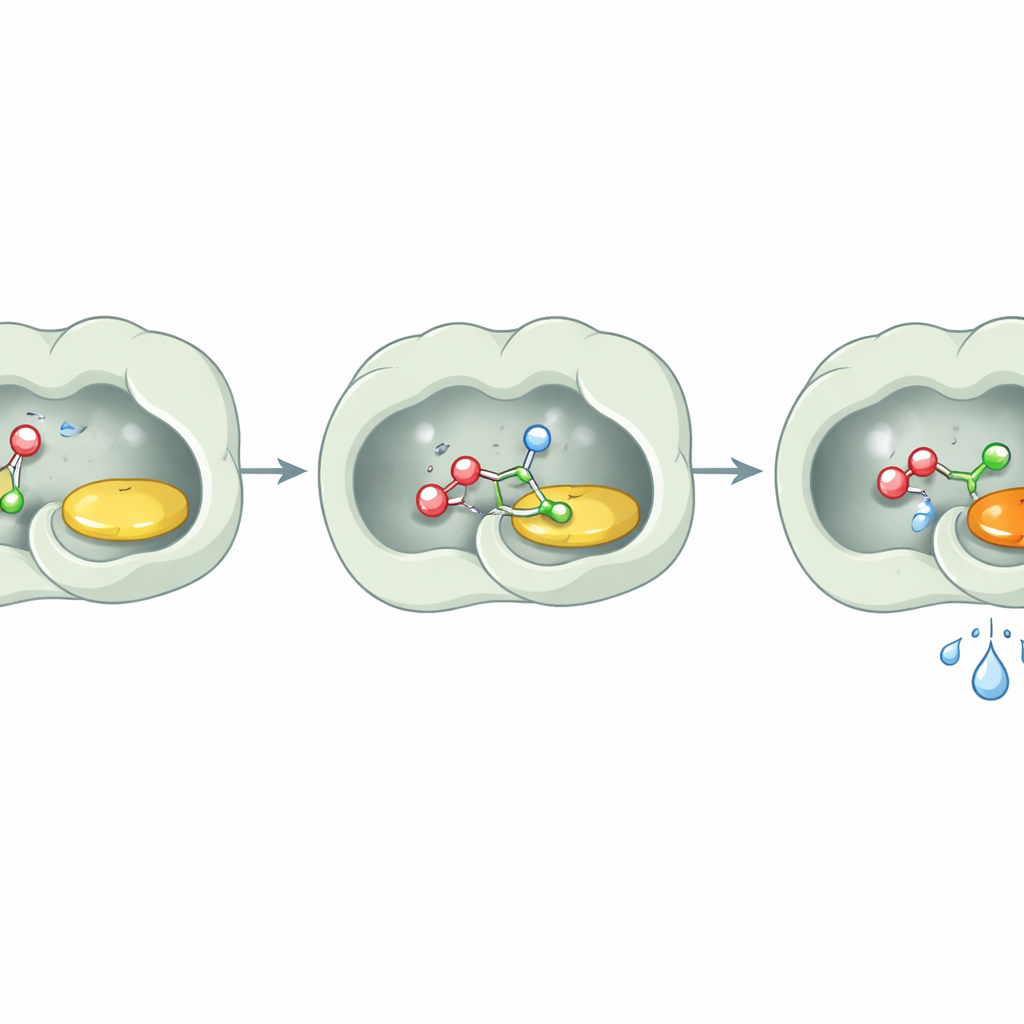
إبعاد الماء عن الطريق
المفاجأة الرئيسية كانت فيما لم يفعله الإنزيم: لم يلاحظ أنه يحلل الإسترات مائياً. حتى بعد حاضنات طويلة مع ركائز إستر وماء، ترك PcAOx‑VPN هذه الركائز سليمة جوهرياً ما لم يُزوَّد مانح أسيل إضافي. توفر الدراسات البنائية تفسيراً بسيطاً. يكسو الموقع الفعّال أحماض أمينية عطِرية وزيتية إلى حد كبير تخلق جيباً شديد الكارهة للماء. أظهر التحليل التفصيلي عدم وجود جزيئات ماء قريبة من عامل الفلافين، وأكّدت الأدوات الحاسوبية أن القناة المؤدية إلى الموقع الفعّال غير ملائمة للماء أيضاً. باختصار، يبني الإنزيم غرفة صغيرة جافة داخل عالم مائي. يمكن للكحولات والآسيات المنشطّة الدخول والتفاعل، لكن تُبقي جزيئات الماء في الجانب الآخر، فلا تتاح لها الفرصة لتفكيك المنتج.
كيف يعمل التفاعل على الأرجح داخلياً
كشفت التجارب الميكانيكية وتحليل الطفرات أن حمضين أمينيين، هستيدين وأسباراجين، مركزيان لكل من دور الأكسدة الطبيعي للإنزيم وموهبته الجديدة في التبادل الأسيتري. يعمل الهستيدين كقاعدة، مساعداً على نزع بروتون من الكحول الداخل وجعله أكثر تفاعلية، بينما يثبت الأسباراجين الحالة المشحونة الناتجة. معاً، يعززان هجوم الكحول على مانح الأسيل لتشكيل وسيط قصير العمر ينهار إلى الإستر المرغوب. كما أن الحالة المؤكسدة لعامل الفلافين مطلوبة: في ظروف خالية من الأكسجين، عندما يُختزل الفلافين، يتوقف تفاعل التبادل الأسيتري ويستأنف فقط عند إعادة إدخال الهواء. ومن اللافت أنه عندما وُضعت نفس الثلاثي من الطفرات في أكسيدازات ذات صلة من فطريات أخرى، اكتسبت تلك الإنزيمات أيضاً نشاط تبادل أسيل قوي، مما يوحي بأن هذا السلوك يمكن تعميمه.
ماذا يعني ذلك لكيمياء أكثر خضرة
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن المؤلفين علموا إنزيمًا معروفًا خدعة جديدة: بناء إسترات مفيدة مباشرة في الماء، مع تجاهل فعّال لميل الماء لفك الشغل. من خلال نحت جيب جاف وملائم للزيت داخل بروتين وضبط عدد قليل من الأحماض الأمينية الأساسية، صنعوا محفزاً يفضّل الكحولات على الماء كشركاء تفاعل. وبما أن مبدأ التصميم نفسه يعمل في إنزيمات ذات صلة، يمكن توسيع هذه المقاربة إلى عائلة من المحفزات لصناعة النكهات والعطور والمواد الكيميائية الرفيعة، وربما الوقود الحيوي، بعمليات أكثر أماناً واستدامة تعتمد أقل على المذيبات العضوية القاسية وأكثر على الماء.
الاستشهاد: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
الكلمات المفتاحية: هندسة الإنزيمات, التحفيز الحيوي, الكيمياء الخضراء, تخليق الإستر, بروتينات فلافين