Clear Sky Science · ar
جهاز نانوي قائم على الحمض النووي يستشعر الإشارات البورينية ويحفّز مفتاحًا مناعيًا لحل الالتهاب
خفض نظام الإنذار في الجسم
عندما تتعرض الأنسجة للإصابة، تتسرّب الخلايا دفعة من «إشارات الإنذار» الكيميائية التي تستدعي الخلايا المناعية لمكافحة العدوى وإزالة الحطام. هذا الاستجابة ضرورية، لكن إذا ظل الإنذار مرتفعًا جدًا أو لفترة طويلة، فقد يسبب التهابًا ضارًا في الرئتين والكليتين وأعضاء أخرى. تصف هذه الدراسة جهازًا نانويًا صغيرًا قابلًا للبرمجة، مصنوعًا من الحمض النووي، يستطيع استشعار متى يكون إشارة الإنذار مفرطة ويقللها بهدوء، مما يساعد الجهاز المناعي على الانتقال من وضع الهجوم إلى وضع الشفاء.
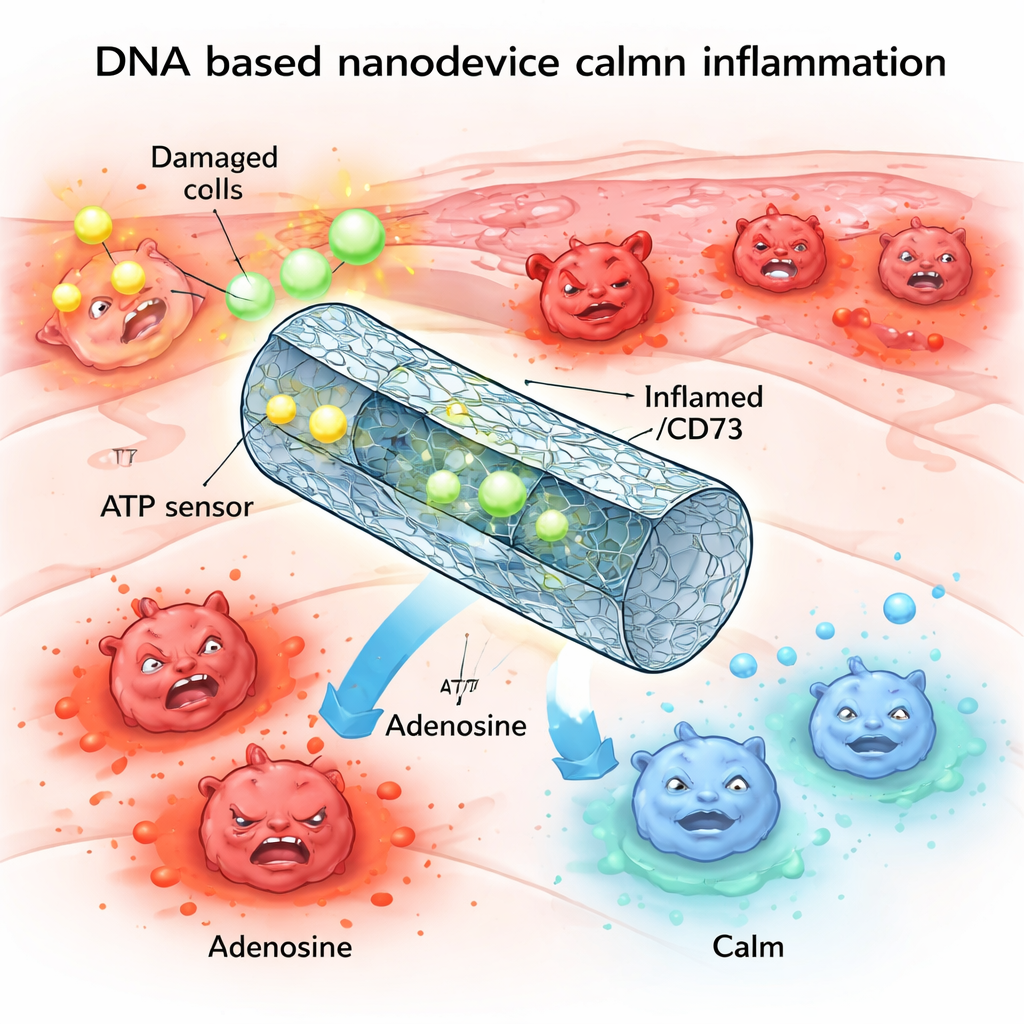
إنذار كيميائي قد يتجاوز الحد
أحد جزيئات الإنذار الرئيسية في الجسم هو ATP، المعروف أكثر بأنه «عملة الطاقة» داخل الخلايا. خلال الإصابة أو الإجهاد، يتسرّب كميات كبيرة من ATP من الخلايا المتضررة إلى الفراغ المحيط. هناك، يعمل ATP خارج الخلية كإشارة استغاثة، مرتبطة بمستقبلات على الخلايا المناعية وتدفعها نحو حالة التهابية شديدة. في الظروف الطبيعية، تقوم إنزيمات على أسطح الخلايا بسرعة بتفكيك فائض ATP إلى الأدينوزين، وهو جزيء ذي تأثير مهدئ ومضاد للالتهاب. لكن في العديد من الأمراض الالتهابية المزمنة أو الشديدة، يكون هذا الجهاز التفكيكي معطلاً، مما يترك مستويات ATP مرتفعة والأدينوزين منخفضًا، وتبقى الأنسجة في حلقة من الضرر.
بناء أنبوب DNA ذكي
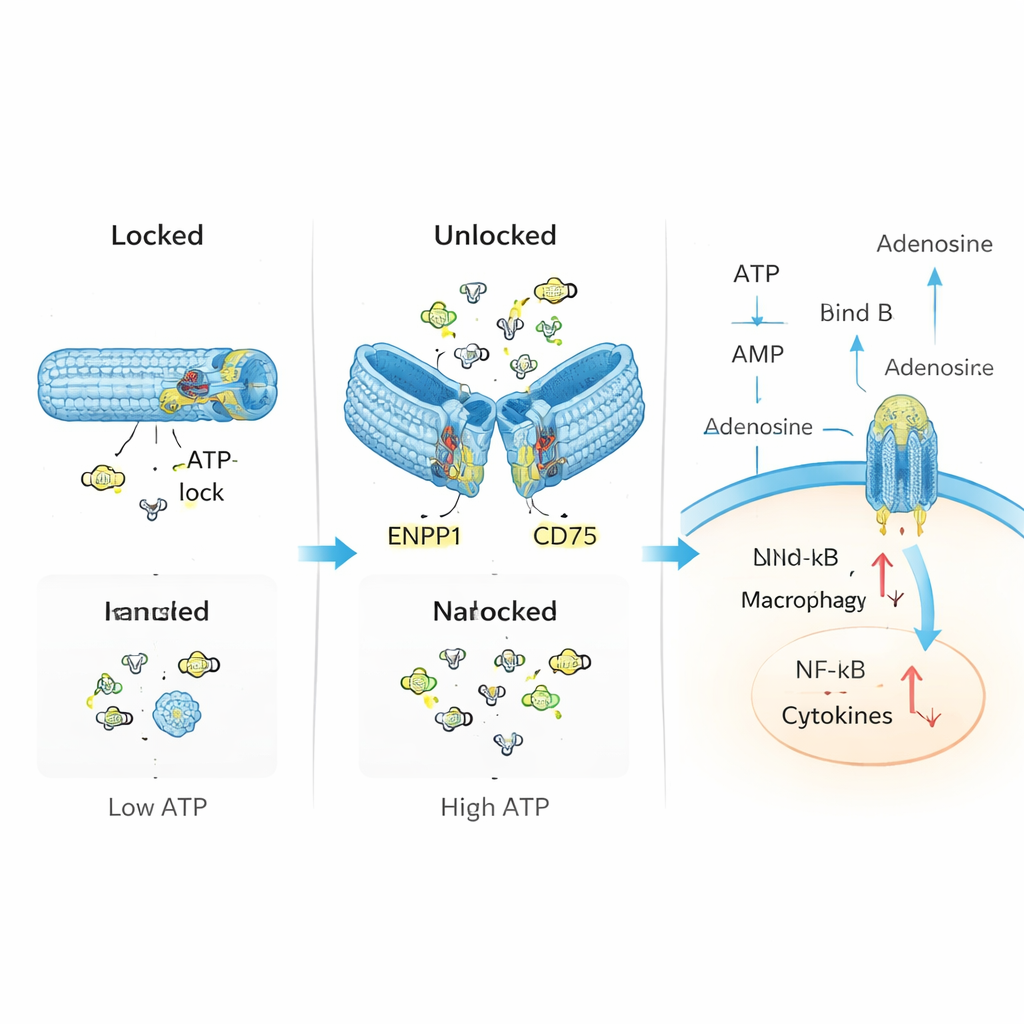
سعى الباحثون لتقليد وإصلاح هذا النظام الضابط الطبيعي باستخدام تكنولوجيا النانو القائمة على الحمض النووي. بنوا أنبوبًا مجوفًا من الحمض النووي، مطويًا بطريقة تشبه الأوريغامي، ومزوّدًا بمكوّنَين رئيسييْن: «مستشعرات» تتعرف على ATP، وإنزيمات تحول ATP إلى أدينوزين. في حالة الراحة، يكون الأنبوب مغلقًا بواسطة مقاطع قصيرة من الحمض النووي تعمل أيضًا كمستشعرات ATP. عندما ترتفع مستويات ATP فوق عتبة معينة نموذجية للأنسجة المصابة، يرتبط ATP بهذه المقاطع، ما يسبب فتح الأنبوب وكشف الإنزيمات ENPP1 وCD73 في الداخل. ثم تقوم هذه الإنزيمات بتفتيت فائض ATP وإنتاج الأدينوزين، مغيرةً التوازن الكيميائي المحلي بلطف من حالة الخطر إلى حالة الحل.
إثبات أن المفتاح يعمل
في تجارب مخبرية محكمة، أكد الفريق أن أنبوب الحمض النووي يبقى مغلقًا عند مستويات ATP المنخفضة لكنه يفتح بشكل موثوق عندما يصبح ATP وفيرًا، تمامًا مثل صمام طوارئ. بمجرد فتحه، يحول الجهاز ATP تدريجيًا إلى نواتج وسيطة ثم إلى الأدينوزين، دون الإضرار الملحوظ بنشاط الإنزيمات. في الخلايا المناعية المعرضة لمستويات عالية من ATP، خفّض هذا الجهاز النانوي النواتج السامة في الميتوكوندريا، وقلل تنشيط مسارات التهابية مثل NF-κB ومركب الالتهاب NLRP3، وعزّز الإشارات المرتبطة بتأثيرات الأدينوزين المهدئة. بعبارة أخرى، لم يكتفِ الجهاز بجمع ATP فحسب؛ بل أعاد برمجة سلوك الخلايا من حالة التهابية إلى حالة تنظيمية.
الركوب إلى مواقع الإصابة
تصميم مفتاح ذكي أمر واحد؛ وإيصاله إلى المكان الصحيح في الجسم أمر آخر. لحل مشكلة التوصيل هذه، ربط الباحثون أنابيب الحمض النووي بسطح الخلايا الوحيدة المتحركة (المونوسيتات)، وهي نوع من خلايا الدم البيضاء التي تتوجه طبيعيًا إلى الأنسجة الملتهبة. باستخدام مرساة من الحمض النووي مرتبطة بالكوليسترول، «أوقفوا» أعدادًا كبيرة من الأجهزة النانوية على غشاء كل خلية، حيث بقيت الأجهزة في الغالب على السطح بدلًا من أن تبتلعها الخلية. في نماذج فئران لإصابة حادة في الرئة والكلى، تراكمت هذه المونوسيتات المزينة في الأعضاء التالفة بكفاءة أكبر بكثير من الأجهزة الحرة، ولا تزال الأجهزة النانوية تستجيب بشكل محدد لمستويات ATP العالية في الأنسجة المصابة.
مساعدة الأنسجة على الشفاء
في الفئران المصابة بإصابة رئوية أو كلوية محفزة كيميائيًا، قلّل العلاج بالجهاز القائم على الحمض النووي من تلف الأنسجة، وتراكم الخلايا المناعية، وجزيئات الرسائل الالتهابية. نجحت نسخة الجهاز المحمولة على المونوسيتات أفضل، مقدمة حماية أقوى من الجهاز الحر أو الإنزيمات وحدها. أظهرت تحليلات جينية و أيضية أعمق لأنسجة الرئة أن هذا النهج لم يخفّض الجينات الالتهابية فحسب، بل ساعد أيضًا في استعادة استقلاب الطاقة الاضطراري في الخلايا. والأهم من ذلك، أظهرت الأجهزة سمية منخفضة ولم تفعّل ردودًا مناعية ضارة في الحيوانات السليمة.
لماذا هذا مهم للعلاجات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن هذا العمل يبرهن على «ثرموستات» جزيئي قابل للبرمجة للالتهاب. مصنوع من الحمض النووي وإنزيمات طبيعية، يستشعر الجهاز النانوي متى تكون إشارة الخطر مفرطة ويحوّلها تلقائيًا إلى إشارة مهدئة، مما يساعد الخلايا المناعية على التراجع وتسهيل إصلاح الأنسجة. ورغم أنه لا يزال في مرحلة تجريبية مبكرة، يشير هذا النهج إلى فئة جديدة من العلاجات التي لا تكتفي ببساطة بحظر المسارات المناعية في كل مكان، بل تعيد التوازن محليًا للإشارات الكيميائية في مواقع الإصابة، ما قد يوفر تحكمًا دقيقًا بالالتهاب الضار في أمراض متعددة.
الاستشهاد: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
الكلمات المفتاحية: جهاز نانوي من الحمض النووي, ATP خارج الخلية, الالتهاب, إشارات الأدينوزين, النانومدينة