Clear Sky Science · ar
العلاج المناعي المضاد لـ TLR2 يغير انتقال α-سينوكلين من الخلايا العصبية إلى الخلايا الدبقية قليلة التغصن في نماذج فأرية وبشرية
لماذا يهم هذا البحث
ضمور الجهاز المتعدد (MSA) هو اضطراب دماغي نادر لكنه سريع التقدّم يجمع بين مشاكل حركية شبيهة بمرض باركنسون وفشل التوازن والوظائف اللاإرادية، مثل هبوط ضغط الدم. يمكن للأطباء تخفيف الأعراض، لكنهم لا يستطيعون حالياً إبطاء تقدم المرض نفسه. يكشف هذا البحث كيفية انتشار بروتين مشوه الشكل بين خلايا الدماغ لإتلاف «عزل الأسلاك» العصبية، ويظهر أن علاجاً بالأجسام المضادة الموجّهة يمكن أن يوقف هذه العملية في نماذج حيوانية وخلوية. تشير النتائج إلى استراتيجية دوائية ملموسة قد تغير مسار MSA في المستقبل بدل الاكتفاء بعلاج الأعراض فقط.
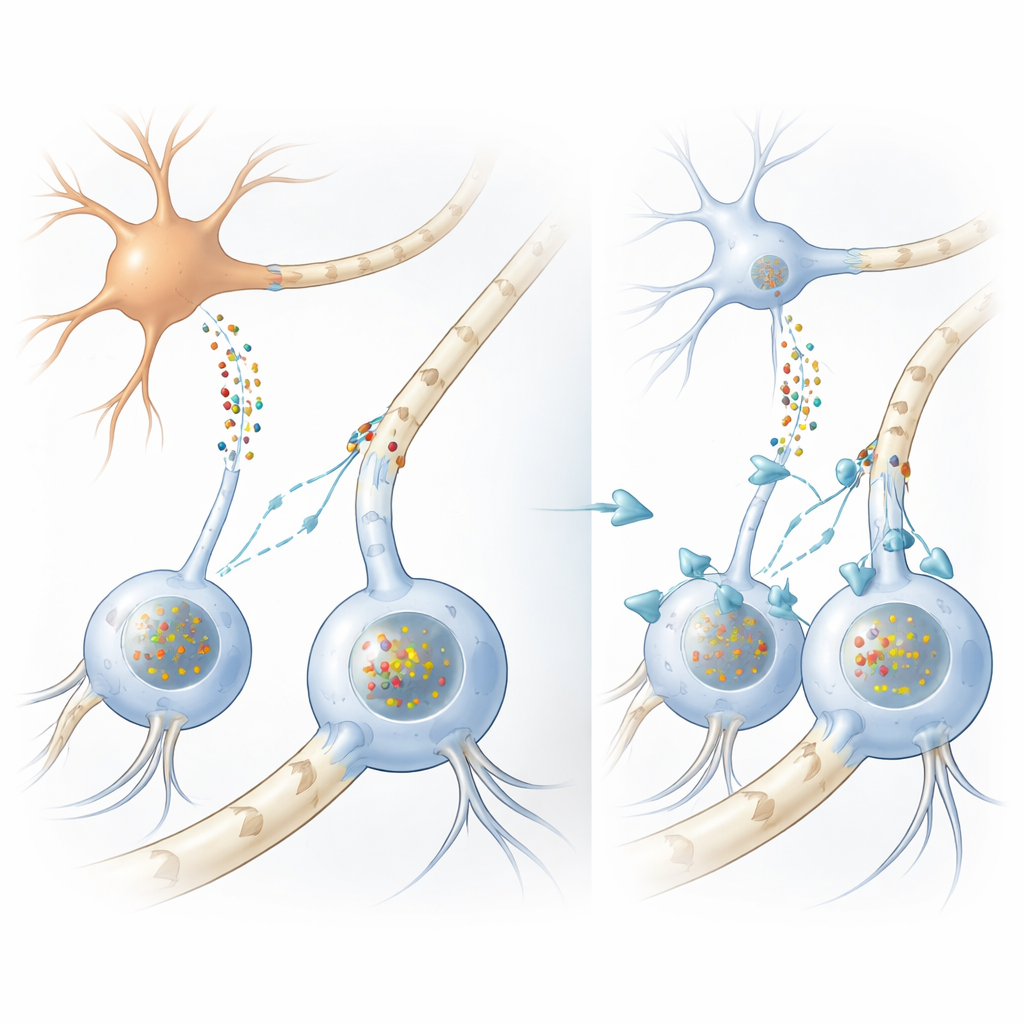
كيف يخطئ توصيل الدماغ
في كثير من اضطرابات الحركة، بما في ذلك داء باركنسون، تتراكم كتل من بروتين يسمى ألفا-سينوكلين داخل الخلايا العصبية. في MSA، مع ذلك، تكون أكثر التراكمات وضوحاً داخل خلايا الدعم المسماة الخلايا الدبقية قليلة التغصن، التي تغلف المحاور العصبية عادة بغلاف دهني يُسمّى المايلين لتسريع الإشارات الكهربائية. من الغريب أن الخلايا الدبقية قليلة التغصن تصنع كمية ضئيلة جداً من ألفا-سينوكلين بنفسها، مما يترك لغزاً قائماً منذ زمن طويل: من أين تأتي الرواسب البروتينية الضخمة في هذه الخلايا؟ أكد الباحثون أولاً، باستخدام عينات دماغية بشرية وتحليلات RNA واسعة النطاق، أن الخلايا الدبقية قليلة التغصن بالفعل تنتج قدرًا أقل بكثير من ألفا-سينوكلين مقارنة بالخلايا العصبية، ما يعزز فكرة أن البروتين الضار يجب أن يصل من الخارج.
انتقال البروتين من الخلية العصبية إلى خلية الدعم
لاختبار ذلك، بنى الفريق عدة نماذج مكملة. في أطباق زراعة الخلايا، أنشأوا خلايا شبيهة بالدبقية قليلة التغصن من خلايا جذعية عصبية ووضعوها في سائل مُجمع من خلايا شبيهة بالعصبونات تم تعديلها لإفراز كميات كبيرة من ألفا-سينوكلين. امتلكت خلايا الدعم هذا البروتين وكونت تكتلات تشبه عن كثب التضمّنات الدبقية المرصودة في أدمغة مرضى MSA، مترافقة مع نفس الوسوم الكيميائية والبروتينات المساعدة. عند فحصهم لسلالة فأرية تُنتج ألفا-سينوكلين البشري الطافر في الخلايا العصبية فقط، وجدوا مرة أخرى تكتلات من البروتين البشري داخل الخلايا الدبقية قليلة التغصن في المادة البيضاء، رغم أن هذه الخلايا لم تكن تُعبّر عن الجين البشري. توضح هذه التجارب معاً أن ألفا-سينوكلين يمكن أن ينتقل من الخلايا العصبية إلى الخلايا الدبقية قليلة التغصن ويشكّل تضمّنات شبيهة بالمرض هناك.
البوابة على سطح الخلية
سأل العلماء بعد ذلك كيف يدخل البروتين إلى الخلايا الدبقية قليلة التغصن. أظهر عمل سابق أن جهاز الاستشعار المناعي مستقبل شبيه التول Toll-like receptor 2 (TLR2) على أسطح الخلايا يعمل كموقع لالتحام ألفا-سينوكلين في الخلايا العصبية والميكروغليا. من خلال التنقيب في مجموعات بيانات التعبير الجيني من أدمغة مرضى MSA، وجد الفريق أن الخلايا الدبقية قليلة التغصن لدى المرضى حملت مستويات مرتفعة بصورة غير عادية من TLR2 مقارنة بالمجموعات الضابطة، وأن ارتفاع TLR2 ارتبط بانخفاض مستويات جينات مرتبطة بالمايلين مثل بروتين المايلين الأساسي. لم يظهر هذا الارتباط في عدة مجموعات بيانات مستقلة لباركنسون، مما يوحي بأن حساسية الخلايا الدبقية لألفا-سينوكلين عبر TLR2 هي سمة مميزة لـ MSA وليست سمة عامة لجميع اضطرابات السينوكلين.
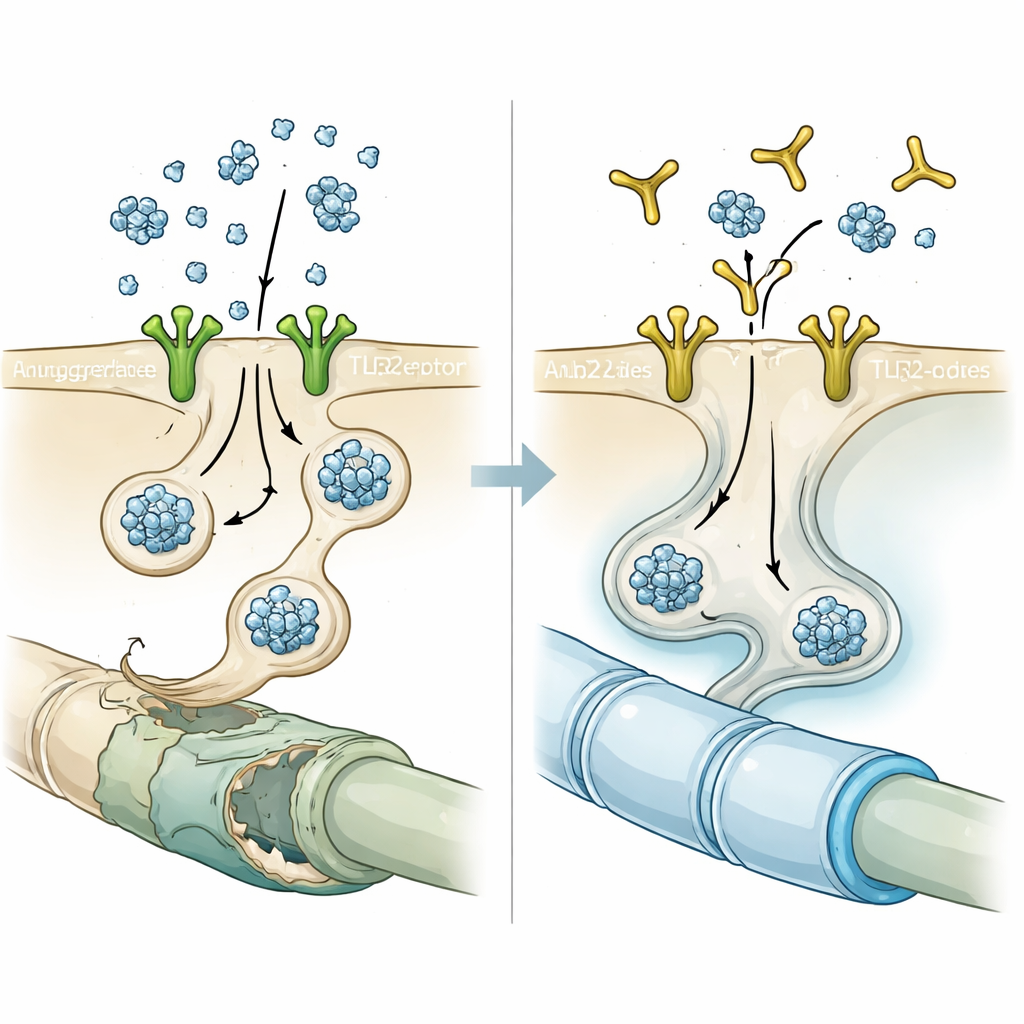
حجب البوابة بواسطة جسم مضاد
مسلحين بهذه الدلالة، اختبر الباحثون NM-101، وهو جسم مضاد مصمم للارتباط بـ TLR2 ومنع تنشيطه. في مزارع الخلايا، أدت المعالجة القصيرة المسبقة للخلايا الدبقية قليلة التغصن بـ NM-101 قبل إضافة ألفا-سينوكلين المستمد من الخلايا العصبية إلى خفض حاد في عدد وحدة وشدة التكتلات الشبيهة بالتضمّن. في الفئران التي إما أنتجت فائضاً من ألفا-سينوكلين العصبي أو تلقت حقنًا بألياف ألفا-سينوكلين مُشكّلة مسبقًا، أدت التسريب الأسبوعي لـ NM-101 إلى خفض كمية البروتين المتجمع في المادة البيضاء، وتهدئة الاستجابات الالتهابية من الميكروغليا والخلايا النجمية، وتقليل تنشيط إنزيم التهابية يُدعى كاسبيز-1 داخل الخلايا الدبقية. عاشت الحيوانات المعالجة لفترة أطول وأظهرت أداءً أفضل في اختبارات الحركة، ما يشير إلى أن التأثيرات الوقائية للجسم المضاد كانت ذات معنى وظيفي، وليس مجرد ملاحظات مجهرية.
إنقاذ العزل التالف
بما أن الخلايا الدبقية قليلة التغصن تصنع المايلين في الدماغ، فحص الفريق ما إذا كان نقل ألفا-سينوكلين يضر المايلين، وما إذا كان حجب TLR2 يمكن أن يساعد. كشف تسلسل RNA على مستوى الخلية المفردة لخلايا دبقية مشتقة من بشر وتعرضت لألفا-سينوكلين منقّاة من الخلايا العصبية تحولات واسعة بعيدًا عن حالة ناضجة منتجة للمايلين واتجاهًا إلى حالة أكثر بدائية شبيهة بالخلايا السلفية، مع خفض العديد من جينات المايلين الأساسية. وأظهرت دراسات التعبير الجيني الموازية على خلايا دبقية ملتقطة بالليزر من مرضى MSA ومن نموذج الفأر توقيعًا مشتركًا: انخفاض تعبير الجينات المشاركة في تشكيل المايلين والحفاظ عليه. وتحت المجهر الإلكتروني، عرضت المادة البيضاء في فئران ألفا-سينوكلين أغلفة مايلين أرق وأقل تنظيماً. عكست معالجة NM-101 العديد من هذه التغيرات، إذ سَمّكت المايلين وأعادت مستويات بروتينات المايلين وطبيعت التعبير عن الجينات اللازمة لنضوج الخلايا الدبقية.
ما يعنيه كل هذا للعلاجات المستقبلية
يدعم هذا البحث سيناريو واضحًا: في MSA، يمكن لألفا-سينوكلين المنتج عن طريق الخلايا العصبية أن ينتشر إلى الخلايا الدبقية قليلة التغصن عبر TLR2 على سطحها، حيث يتراكم، ويُحرّض الالتهاب، ويعطل برنامج نضوج الخلايا، ويقوّض غلاف المايلين الذي يعزل توصيلات الدماغ. من خلال حجب TLR2 بواسطة جسم مضاد موجه، استطاع الباحثون مقاطعة سلسلة الأحداث هذه في الفئران ونماذج الخلايا البشرية، مما قلّل التضمّنات السامة وهدّأ الالتهاب وأصلح المايلين وحسّن البقاء والحركة. وبينما يحتاج NM-101 نفسه إلى اختبارات صارمة على البشر، يثبت العمل أن نقل البروتين المعتمد على TLR2 هو محرك مركزي لاعتلالات شبيهة بـ MSA ويبرز العلاج المناعي المضاد لـ TLR2 كاستراتيجية واعدة لإبطاء أو منع هذا المرض المدمر.
الاستشهاد: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
الكلمات المفتاحية: ضمور الجهاز المتعدد, ألفا-سينوكلين, الخلايا الدبقية قليلة التغصن, ضرر المايلين, العلاج المناعي