Clear Sky Science · ar
تخليق NAD/H السيتوبلازمي عبر NRK1 ينظم القدرة الالتهابية ويعزز بقاء خلايا CD4+ T
الحفاظ على توازن الخلايا المناعية
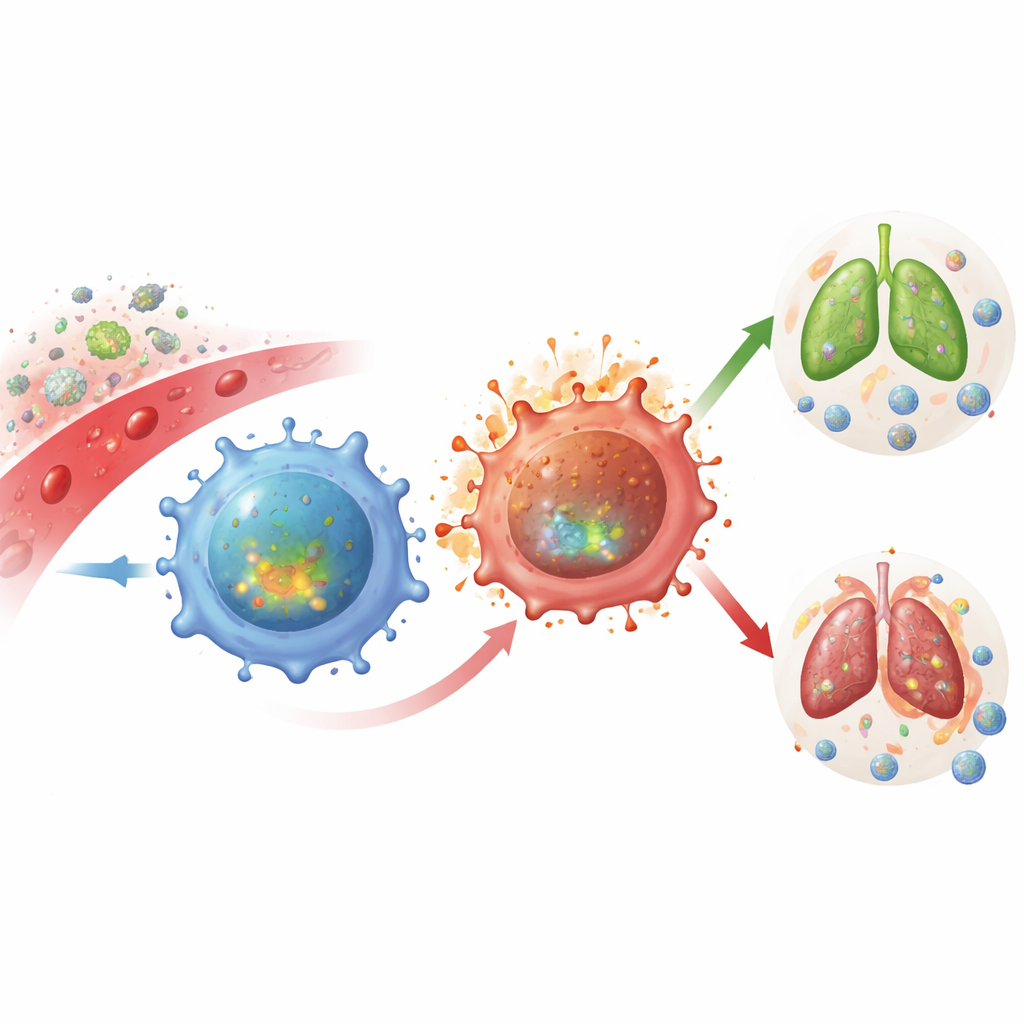
عندما تواجه أجسامنا عدوى، تتدخل أنواع معينة من خلايا الدم البيضاء تُدعى خلايا CD4+ T لتنسق الاستجابة المناعية. لكن إذا أصبحت هذه الخلايا مفرطة النشاط قد تتلف أنسجتنا؛ وإذا كانت ضعيفة للغاية تستغل العدوى الفرصة. تستكشف هذه الدراسة كيف يقرر مفتاح أيضي صغير داخل الخلايا، يدور حول جزيء يُدعى NAD وإنزيم يُسمى NRK1، ما إذا كانت هذه الخلايا ستستجيب بطريقة مُحكمة أم تنقلب إلى فرط نشاط ضار.
وقود للخلايا المناعية المشغولة
عند تنشيط خلايا CD4+ T أثناء العدوى، ترتفع متطلباتها من الطاقة بشكل كبير. تحرق المزيد من السكر، تزداد نشاط الميتوكوندريا، وتولد دفعات من أنواع الأكسجين التفاعلية (ROS)—جزيئات تفاعلية جدًا قد تعمل كإشارات لكنها قد تسبب أيضًا تلفًا. كل هذا يعتمد على NAD، عامل مساعد صغير ينقل الإلكترونات ويُستخدم ويُعاد تدويره باستمرار. وجد الباحثون أنه في خلايا CD4+ T البشرية والجرذية على حد سواء، يؤدي التنشيط إلى زيادة قوية في مستويات الإنزيم NRK1، الذي يساعد على إعادة بناء NAD الخلوي من جزيئات سابقة. إضافة سلف لـ NAD يُدعى نيكوتيناميد ريبوزيد (NR) زادت مستويات NAD في الخلايا البشرية، لكن بشكل غير متوقع جعلتها أقل تنشيطًا وأقل ميلاً لإطلاق بروتينات مراسلة التهابية.
قوة نارية أكبر لكن عمر أقصر
لفهم دور NRK1 داخل الخلايا بشكل أعمق، لجأ الفريق إلى فئران مُعدلة جينيًا تفتقر إلى NRK1. احتوت خلايا CD4+ T لديهم على NAD أقل عمومًا ولم تعد تستجيب لـ NR. عند تحفيز هذه الخلايا، أنتجت في الواقع المزيد من السيتوكينات الالتهابية مثل إنترفيرون-غاما وجزيئات إشارات أخرى، مما يشير إلى أنها أصبحت مفرطة النشاط. ومع ذلك، كان هناك ثمن: هذه الخلايا الخالية من NRK1 ماتت بسهولة أكبر أثناء التنشيط المطوّل. بعبارة أخرى، أدى فقدان NRK1 إلى تحوّل الخلايا نحو استجابة أكثر انفجارًا وأقل استدامة، مع نشاط أقوى على المدى القصير لكن بقاء أقل على المدى الطويل.
صمام أمان أكسدة-اختزال داخل الخلية
ثم تساءل الباحثون لماذا يغير تعديل NRK1 سلوك الخلايا T بهذا الشكل الدراماتيكي. اكتشفوا أن NRK1 مهم بشكل خاص لتوليد ليس NAD فحسب، بل أيضًا قريبه الفوسفاتيدي NADP وصيغته المختزلة NADPH داخل السيتوبلازم، السائل الداخلي للخلية. يعد NADPH لاعبًا رئيسيًا في أنظمة مضادات الأكسدة التي تعيد تدوير الجلوتاثيون، أحد الدفاعات الأساسية ضد ROS. في الخلايا الخالية من NRK1، انخفضت مستويات NADP/NADPH بشكل أبلغ من NAD نفسه، ضعفت دفاعات الجلوتاثيون، ارتفعت مستويات ROS، وأصبح عامل النسخ NFAT أكثر ميلاً للانتقال إلى النواة وتشغيل الجينات الالتهابية. وأدى حجب إنزيم منفصل يصنع NADPH إلى تكرار هذه الزيادة في ROS وإنتاج السيتوكينات، بينما عكس علاج الخلايا بمضاد أكسدة الحالة المفرطة الالتهاب. في الخلايا البشرية، أدى تزويدها بـ NR إلى زيادة NADPH، وتعزيز قدرة مضادات الأكسدة، وتقليل ROS، ومنع NFAT من دخول النواة، مما خفّض الالتهاب مرة أخرى.
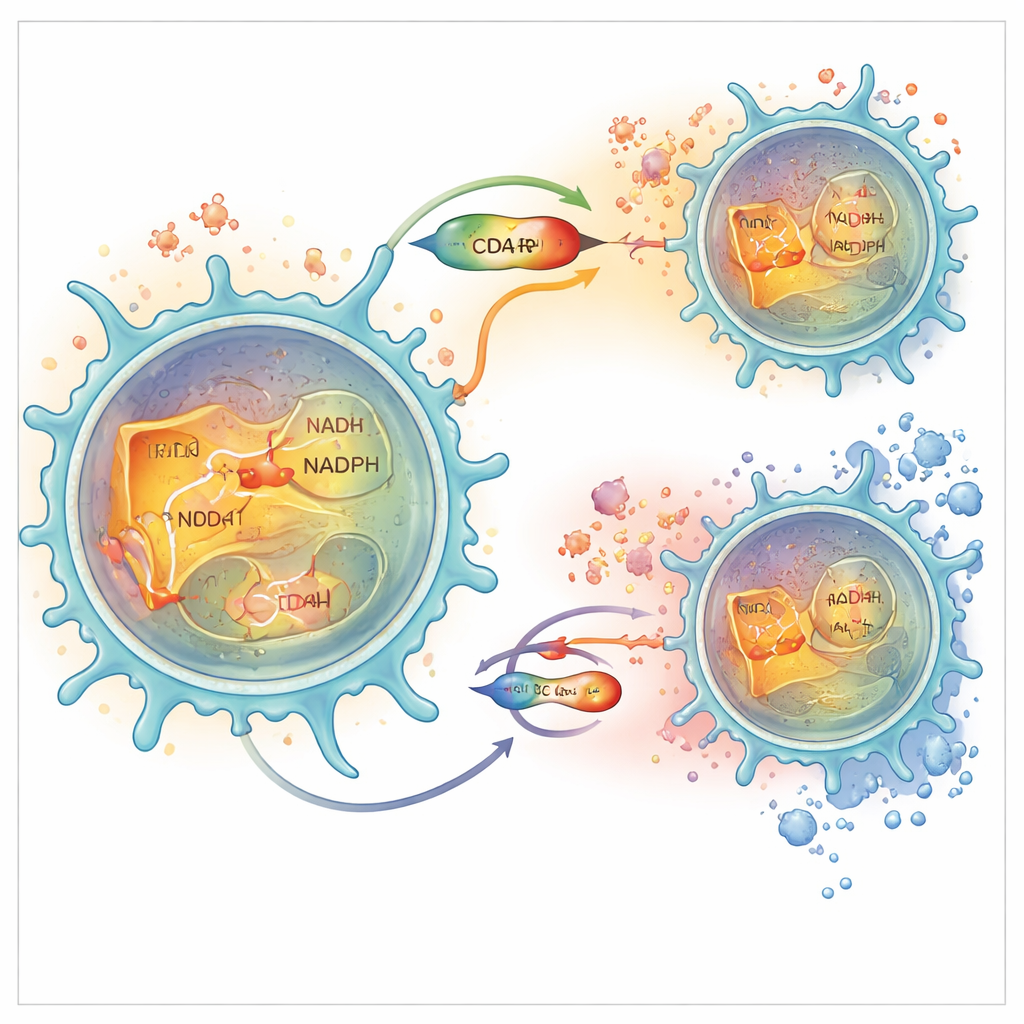
تحكم محلي في داخل الخلية T
بتعمق أكبر، أظهر الفريق أن مستويات NRK1 ترتفع أساسًا في السيتوبلازم للخلايا CD4+ T المنشطة، وليس في ميتوكوندرياتها، وأن إنزيمات الشريك هناك مُكيّفة لتحويل وسائط مشتقة من NR إلى NAD ثم إلى NADP/NADPH. باستخدام موائمات حيوية فلورية وتقسيم كيميائي حيوي للكسور الخلوية، تحققوا أن نشاط NRK1 يعزّز محليًا NAD وNADPH بشكل خاص في هذا الحيز. يرتبط هذا "الجيب الأيضي" المحلي ارتباطًا وثيقًا بالتحلل السكري (تحلل الجلوكوز) في السيتوبلازم وبمعالجة ROS. بدون NRK1، تحولت الخلايا بعيدًا عن التحلل السكري نحو استخدام أكبر للأكسدة الميتوكوندرية لكن دون فشل طاقي شامل، ما يشير إلى أن النتيجة الرئيسية لفقدان NRK1 هي اضطراب توازن الأكسدة-الاختزال والإشارات أكثر من إيقاف استقلاب الخلية بأكمله.
اختبارات واقعية أثناء العدوى
لمعرفة كيف يتجلى هذا الآلية في الحيوانات الحية، درس الباحثون فئرانًا تفتقر خلايا T فيها إلى NRK1 أثناء عدوى خطيرة بفطر رئوي (Cryptococcus neoformans) وفيروس الإنفلونزا. في كلتا الحالتين، ظهرت على خلايا CD4+ T الخالية من NRK1 دلائل على تلف DNA أكبر—من المحتمل نتيجة ROS غير المنضبط—وكانت أقل قدرة على البقاء كخلايا فعالة وظيفيًا في مواقع حاسمة مثل الدماغ أثناء العدوى الفطرية والعقد الليمفاوية المصرفية للرئتين المصابة بالإنفلونزا. كان لدى الفئران ذات خلايا T الخالية من NRK1 أحمال فطرية أعلى في الدماغ ودرجات مرض أسوأ أثناء الإنفلونزا، مما يربط المسار الكيميائي الحيوي مباشرةً بقدرة الجسم على السيطرة على الممرضات.
ما دلالة هذا لاختبارات علاجية مستقبلية
بشكل عام، تكشف الدراسة أن NRK1 يعمل كوسط مُعدّل داخلي حاسم لخلايا CD4+ T، يشكّل مدى التهابية هذه الخلايا ومدة بقائها. عبر توجيه الإنتاج السيتوبلازمي لـ NAD وNADPH، يدعم NRK1 دفاعات مضادات الأكسدة، ويقيد الإشارات الالتهابية المفرطة، ويساعد في الحفاظ على أعداد فعالة من الخلايا أثناء العدوى. للقراء غير المتخصصين، الرسالة أن قدرة الجهاز المناعي ودقته تعتمد ليس فقط على نوع الخلايا الموجودة، بل أيضًا على دوائر أيضية صغيرة داخل تلك الخلايا. قد تتيح تعديل المسارات المرتبطة بـ NAD—مثل المكملات كنيكوتيناميد ريبوزيد أو أدوية تستهدف NRK1 وشركاءه—سبلًا جديدة في المستقبل لتهدئة الالتهاب الضار أو تعزيز الدفاع المناعي، بحسب الحاجة السريرية.
الاستشهاد: Stavrou, V., Ali, M., Gudgeon, N. et al. Cytoplasmic NAD/H synthesis via NRK1 regulates inflammatory capacity and promotes survival of CD4+ T cells. Nat Commun 17, 2349 (2026). https://doi.org/10.1038/s41467-026-68863-w
الكلمات المفتاحية: خلايا CD4 T, استقلاب NAD, الإجهاد التأكسدي, تنظيم المناعة, نيكوتيناميد ريبوزيد