Clear Sky Science · ar
تفاعلات cGAS-IFN-I عبر استخراج الحمض النووي النووي من الخلايا الميتة عبر النيوكليوسيتوز
كيف يقرأ جهازنا المناعي الحمض النووي من الخلايا الميتة
عندما تموت خلايانا أثناء العدوى أو السرطان أو بسبب التآكل اليومي، يجب تنظيف بقاياها دون استثارة التهاب مفرط. تكشف هذه الورقة عن طريقة مفاجئة يمكن للخلايا المناعية أن تختزل بها إلى نوى الخلايا الميتة، وتستخرج حمضها النووي، وتستخدمه كإشارة خطر. قد يغير فهم هذا النظام المخفي للتنظيف والإنذار نظرتنا إلى الأدوية المضادة للفيروسات، والأمراض المناعية الذاتية، وعلاجات السرطان، وتأثيرات الأدوية الجانبية.
إنذار حمض نووي مخفي داخل الخلايا المناعية
تحتوي خلايانا على جهاز استشعار يُدعى cGAS يكتشف الحمض النووي في مكان غير صحيح — طافياً في سائِل الخلية بدلاً من أن يكون مغلفاً بأمان في النواة أو الميتوكوندريا. عندما يصادف cGAS مثل هذا الحمض النووي، يفعّل برنامج إنذار قوي ينتج الإنترفيرونات من النوع الأول، وهي بروتينات محورية لمكافحة الفيروسات وتنظيم المناعة. علم العلماء أن الفيروسات يمكنها إدخال مادتها الوراثية إلى الخلايا لتحفيز هذا المسار، وأن أجزاء من حمضنا النووي قد تتسرب أحياناً وتسبب أمراضاً مناعية ذاتية. لكن ظل لغز أساسي: كيف تصل كميات كبيرة من حمضنا النووي، خصوصاً من الخلايا الميتة، إلى cGAS دون أن تُهضم ببساطة في “معدة” الخلية المتمثلة في الجسيمات الحالّة (الليزوزومات)؟
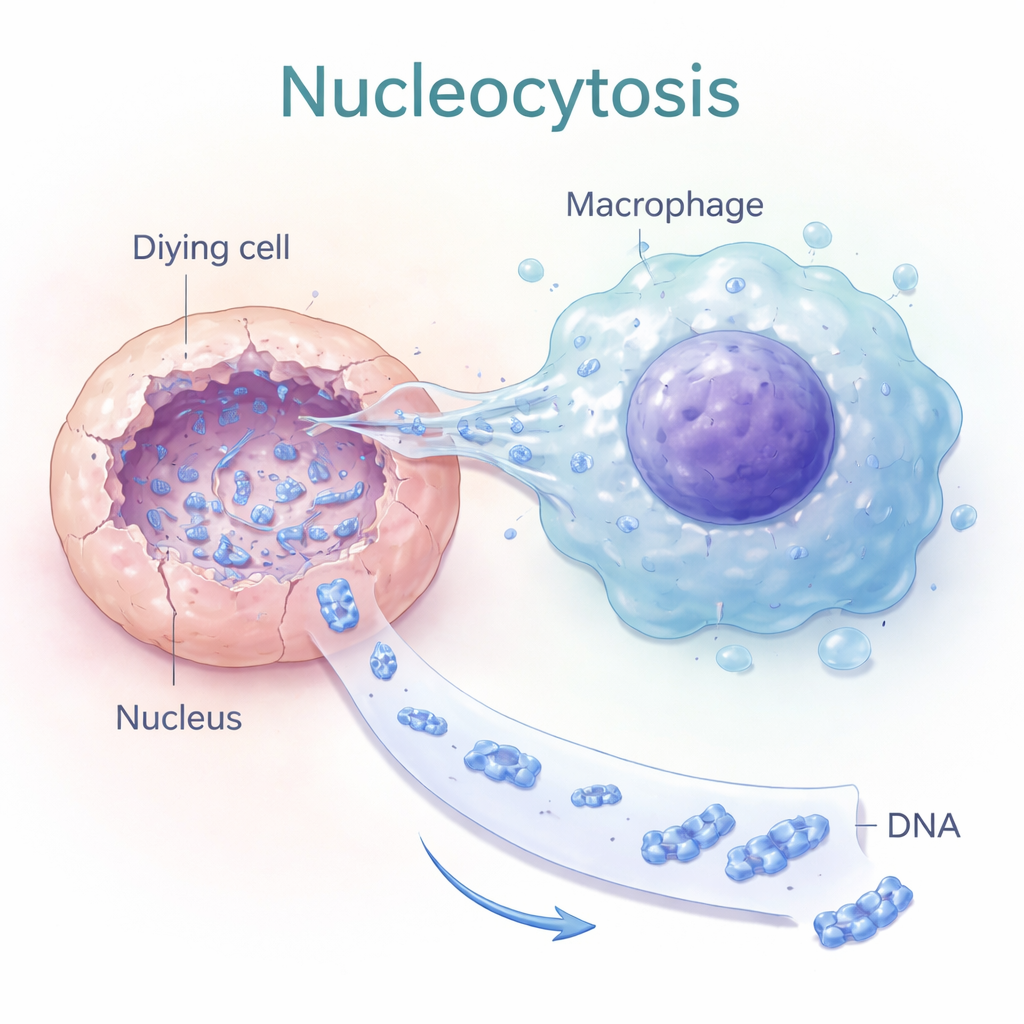
النيوكليوسيتوز: نفق إلى أنوية الخلايا الميتة
اكتشف المؤلفون عملية أطلقوا عليها "النيوكليوسيتوز"، حيث تقوم بلعميات معينة — خلايا مناعية عادةً تبلع الحطام — بسلوك أكثر تحديداً. بدلاً من ابتلاع خلية ميتة كاملة، تمد هذه الخلايا نتوءات رفيعة تشبه الأصابع مباشرة إلى نواة الخلية المحتضرة. أظهرت صور الخلايا الحية انخفاض كثافة الحمض النووي داخل نواة الخلية الميتة بينما زادت داخل البلعمي الملتصق، مما يشير إلى استخراج نشط للحمض النووي النووي. اعتمد هذا النقل على هيكل الخلية الداخلي (الأكتين) وعلى جزيئات إشارات تتحكم في شكل الخلية، ما يوحي بأن النيوكليوسيتوز سلوك ميكانيكي هادف، لا تسرباً سلبياً.
عندما تُفعل أدوية مضادة للفيروسات إنذار الحمض النووي
خلال جائحة كوفيد-19، جُرّبت أدوية مثل الهيدروكسي كلوروكين على نطاق واسع كمضادات فيروسية، ومع ذلك ظلت آلياتها الدقيقة في الجسم مبهمة. وجد الباحثون أن الهيدروكسي كلوروكين وعدداً من الأدوية الشبيهة "المحبة للأيونات" يمكن أن تنشط بقوة مسار cGAS–STING–الإنترفيرون — لكن فقط في شريحة فرعية من البلعميات. تزعزع هذه الأدوية الليزوزومات برفع حموضتها وبحجب إنزيم يسمى PPT1، الذي يساعد في تكسير الوشوم الدهنية على البروتينات. يدفع التأثير المشترك بعض الخلايا إلى شكل خاص من الموت يتراكم فيه بروتين يسمى الكالريتكولين في النواة. ثم تمتد البلعميات تفضيلياً نحو هذه الأنوية الغنية بالكالريتكولين، وتستخرج الحمض النووي عبر النيوكليوسيتوز، وتفجر إنتاج إنترفيرون قوي في عدد قليل من الخلايا — بما يكفي لإحداث إشارة مضادة للفيروسات محلية قوية دون أن تُسيطر على الجسم بأكمله.
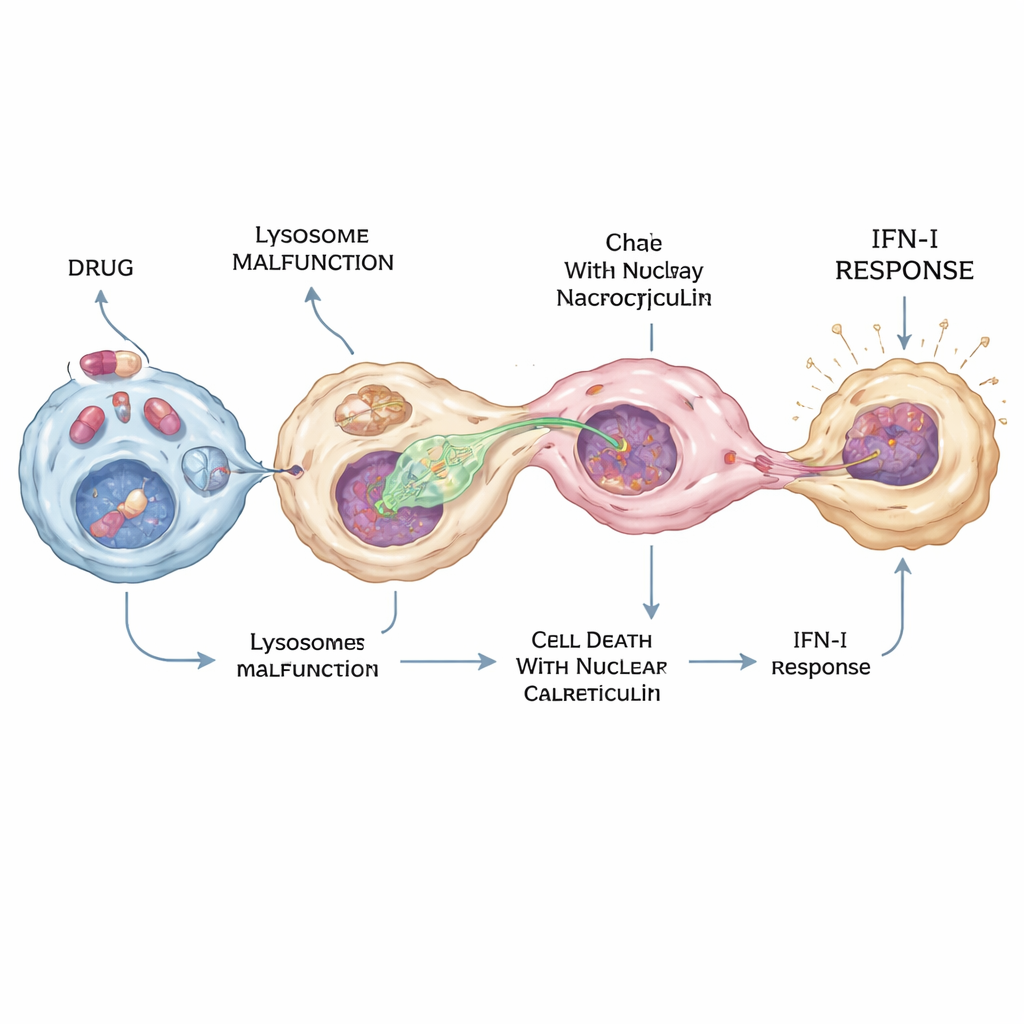
من الدفاع المحلي إلى المرض والتأثيرات الجانبية
من خلال دراسة كل من مزروعات الخلايا ورئات الفئران، أظهر الفريق أن البلعميات المعالجة بالأدوية يمكن أن تشعل استجابة إنترفيرون معتمدة على STING تبقى في الغالب محلية — على سبيل المثال في الرئة — بدلاً من أن تصبح جهازية. يساعد هذا في تفسير سبب إمكانية ظهور فوائد مضادة للفيروسات أو مضادة للأورام لأدوية مثل الهيدروكسي كلوروكين في أنسجة معينة، وأيضاً لماذا قد تسبب آثاراً جانبية محددة للأعضاء مثل سمية العين أو القلب عند استخدامها طويل الأمد. قد يساهم نفس مسار النيوكليوسيتوز بشكل معقول في الأمراض المناعية الذاتية أو الالتهابية كلما تزامنت الخلايا الميتة مع إجهاد الليزوزومات، لأنه يوفر طريقاً مباشراً لحمض نووي ذاتي لتفعيل إنذار cGAS.
لماذا يهم هذا للأدوية المستقبلية
للغير متخصص، الرسالة الأساسية هي أن الخلايا المناعية لا تكتفي بابتلاع الخلايا الميتة سلبياً؛ إذ يمكنها فعلياً استخراج الحمض النووي من أنويتها واستخدامه كإشارة لطلب المساعدة. يشرح هذا المسار كيف يمكن لحمضنا النووي أن ينشط دفاعات مضادة للفيروسات قوية بطريقة مركزة ومحلية، بينما يبرز أيضاً كيف قد تؤدي الأدوية التي تزعزع الليزوزومات أو PPT1 إلى تشغيل هذا المفتاح عن غير قصد. بتمكين ضبط النيوكليوسيتوز صعوداً أو هبوطاً — إما بتصميم مضادات فيروسية وعلاجات سرطانية أكثر ذكاءً أو بتجنب إشارات الحمض النووي الذاتي غير المرغوب فيها في الأمراض المناعية الذاتية — يأمل الباحثون في استغلال هذه الآلية المكتشفة حديثاً لعلاجات أكثر أماناً ودقة.
الاستشهاد: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
الكلمات المفتاحية: النيوكليوسيتوز, cGAS-STING, هيدروكسي كلوروكين, الإنترفيرون من النوع الأول, البلعميات