Clear Sky Science · ar
السلامة والنشاط البيولوجي لمستقبل خلوي ثنائي التخصص يستهدف بروتين Gag لفيروس HIV لدى ذكور يعيشون مع فيروس HIV: تجربة أولى على البشر
لماذا تهم هذه الدراسة الجديدة حول فيروس HIV
يمكن للأشخاص الذين يعيشون مع فيروس HIV اليوم أن يتوقعوا أعمارًا قريبة من العادية بفضل مجموعات الأدوية الحديثة. لكن هذه الأدوية، المسماة بالعلاج المضاد للفيروسات القهقرية (ART)، لا تزيل الفيروس؛ بل تحافظ عليه تحت السيطرة. تظل جيوب مخفية من فيروس HIV داخل الجسم ويمكن أن تعيد بدء العدوى إذا توقف العلاج. تختبر هذه الدراسة نوعًا جديدًا من العلاج المناعي الدقيق — مبنيًا على مستقبل خلوي صناعي — يهدف إلى تدريب الجهاز المناعي على تعقب تلك البؤر المخفية بأمان لدى أشخاص خاضعين جيدًا لـ ART.
الفيروس الخفي الذي لا يزول
حتى عندما تُظهر فحوصات الدم أن الفيروس «غير قابل للكشف»، يبقى HIV كالمادة الوراثية المختبئة داخل خلايا طويلة العمر، وخصوصًا نوع من خلايا الدم البيضاء يُدعى الخلايا التائية CD4. هذه الخلايا الحافظة تحمل فيروسًا خامدًا لكن سليمًا يمكن أن يستيقظ مرة أخرى، مما يجبر الأشخاص على تناول الحبوب يوميًا مدى الحياة. محو كل خلية مصابة تمامًا أمر بالغ الصعوبة ولم يتحقق إلا لدى عدد قليل من الأشخاص الذين خضعوا لعمليات زرع نخاع عظم محفوفة بالمخاطر لعلاج السرطان. يسعى العديد من الباحثين بدلًا من ذلك إلى «علاج وظيفي»: تقليص المستودع الفيروسي بما يكفي ليتمكن دفاع الجسم الذاتية من إبقاء HIV تحت السيطرة بدون دواء مستمر.
جزيء مصمم لإعادة توجيه الخلايا التائية
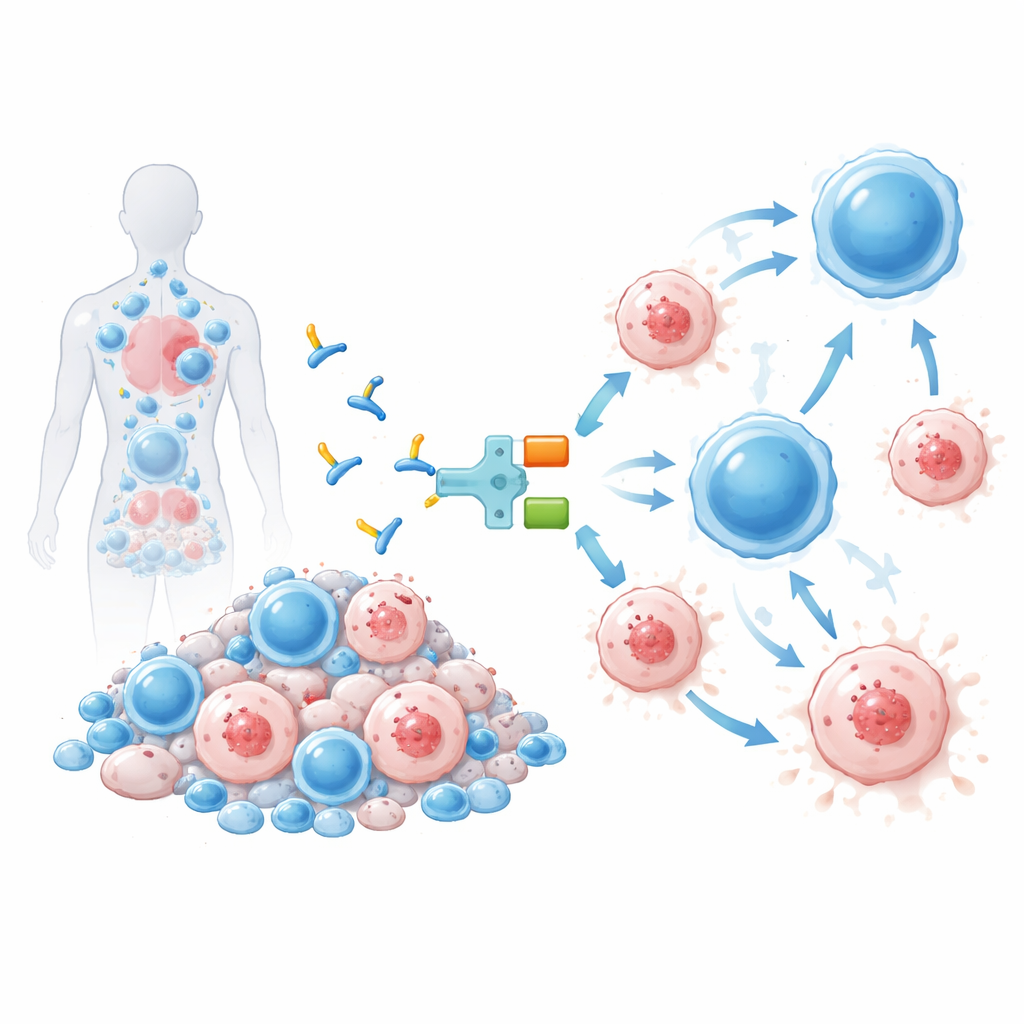
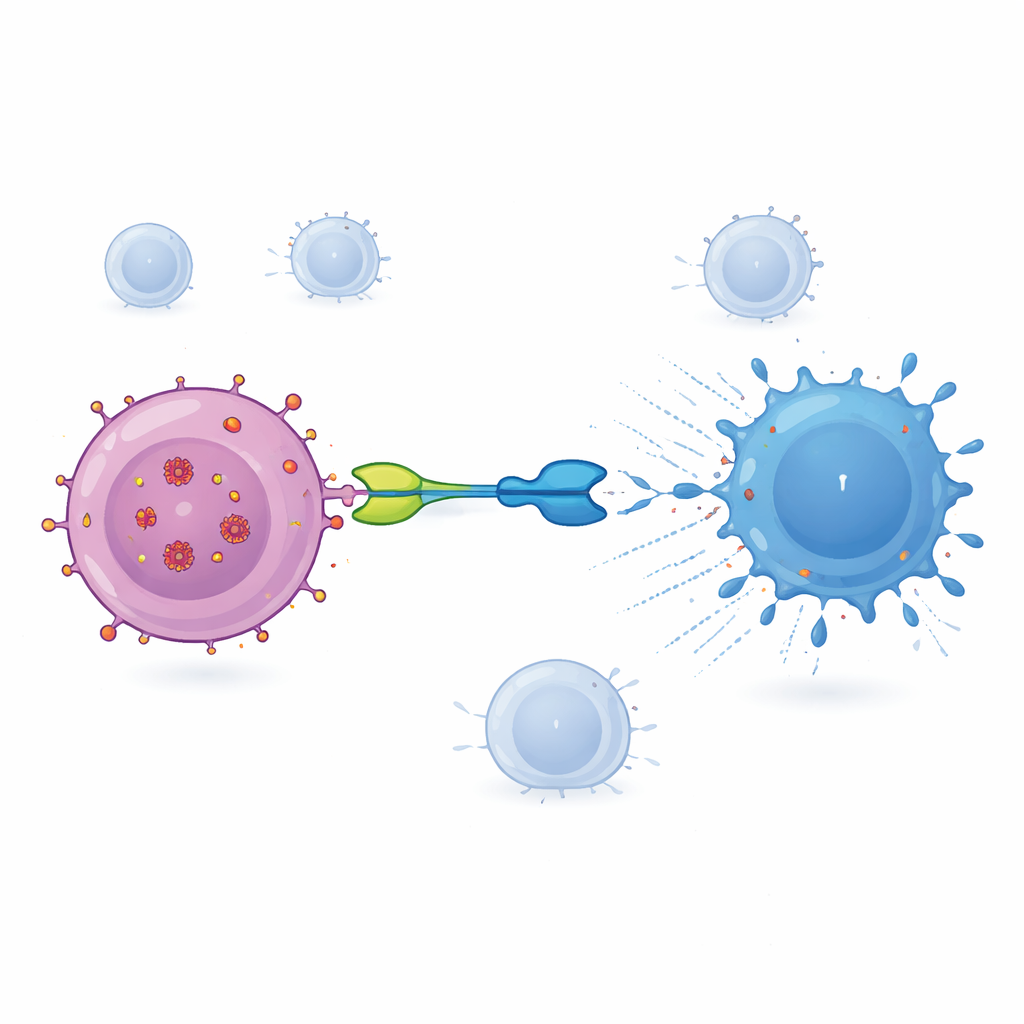
العلاج الذي تم اختباره هنا، المسمى IMC‑M113V، هو بروتين صغير يعمل كمحول جزيئي بين الخلايا المصابة والجهاز المناعي. أحد طرفي IMC‑M113V هو مستقبل خلوي معدّل يتعرف على قطعة صغيرة من فيروس HIV من بروتين Gag معروضة على سطح الخلايا المصابة في سياق علامة مناعية شائعة (HLA‑A*02:01). الطرف الآخر يتشبث ببنية CD3 الموجودة على جميع الخلايا التائية. عندما يربط IMC‑M113V كلا الجانبين معًا، يقرب الخلايا التائية العادية من الخلية المصابة بفيروس HIV ويحفزها على قتلها. في اختبارات المختبر، أظهر هذا الجزيء حساسية عالية، ملاحظًا نسخة أو بضع نسخ فقط من قطعة الفيروس على سطح الخلية وقادرًا بفعالية على القضاء على خلايا مصابة بعدة متغيرات شائعة لفيروس HIV، مع عدم إظهار تنشيط ذي دلالة ضد مجموعة من الخلايا البشرية السليمة.
الاختبار الأول لدى أشخاص يعيشون مع HIV
لرؤية ما إذا كانت هذه المقاربة آمنة لدى البشر، أجرى الباحثون تجربة مبكرة الطور شملت اثني عشر رجلاً بالغًا يعيشون مع HIV في المملكة المتحدة وبلجيكا وإسبانيا. كان جميع المشاركين خاضعين لتحكم جيد للعدوى على ART، لديهم أعداد مرتفعة من خلايا CD4 وحملوا النوع المناعي المطلوب. تلقى كل شخص جرعة وريدية واحدة من IMC‑M113V عند أحد ثلاثة مستويات جرعة منخفضة ثم تمت متابعته عن كثب لمدة شهر. كان التركيز الرئيسي في هذه المرحلة على السلامة: البحث عن آثار جانبية مثل الحمى أو الالتهاب الشديد أو مشاكل عصبية، والتي قد تحدث مع أدوية أخرى قوية تُشرك الخلايا التائية المستخدمة في علاج السرطان.
ما رآه الباحثون في العيادة
عبر جميع الجرعات، كان IMC‑M113V محتمل التحمل عمومًا. أبلغ نصف المشاركين عن بعض الآثار الجانبية، غالبًا مشاكل طفيفة مثل التعب أو تهيج الجلد، ولم يُصَب أحد بمشكلات خطيرة مثل متلازمة إفراز السيتوكين أو السمية العصبية. أظهرت اختبارات الدم أن مستويات الدواء ارتفعت وانخفضت خلال يوم تقريبًا، مع عمر نصف يقارب 15–22 ساعة. عند أعلى جرعة (15 ميكروغرام)، أظهر عدة مشاركين ارتفاعات مؤقتة في جزيئات التهابية، لا سيما الإنترلوكين‑6، وعلامات على أن خلاياهم التائية أصبحت منشطة وأكثر قدرة على إنتاج بروتينات قاتلة للخلايا. كانت هذه التغيرات المناعية أقوى لدى المتطوعين الذين حملت فيروساتهم متغيرات Gag التي يمكن لـ IMC‑M113V أن يرتبط بها بإحكام خاص، مما يشير إلى أن الدواء كان يتفاعل مع أهدافه المقصودة في الجسم. مع ذلك، بعد جرعة واحدة، لم يكن هناك انخفاض قابل للقياس في حجم المستودع الفيروسي في الدم، كما قِيس بواسطة RNA الفيروسي والـ DNA الفيروسي السليم داخل خلايا CD4.
ماذا يعني ذلك لعلاج HIV في المستقبل
للقارئ غير المتخصص، الرسالة الرئيسية هي أن هذه الدراسة تقدم إثبات مفهوم مهمًا أوليًا: يمكن إعطاء جزيء «جسر» مناعي مستهدف بدقة بأمان للأشخاص الذين يعيشون مع HIV الخاضع للسيطرة، ويمكنه تحفيز خلاياهم التائية للتعرف على الخلايا التي تجمع الفيروس. لم يشفِ المرضى من HIV ولا سمح لهم التوقف عن ART، لكن هذا لم يكن هدف تجربة البشر الأولى هذه. تدعم النتائج اختبار جرعات أعلى ومتكررة، وربما بالاقتران مع أدوية تحفز المزيد من الخلايا المصابة على الإفصاح عن نفسها، وتوسيع المقاربة لتشمل أنواع مناعية أخرى بخلاف HLA‑A*02:01. إذا أكدت الدراسات المستقبلية أن هذه الاستراتيجية يمكنها تقليص المستودعات الفيروسية بشكل موثوق دون آثار جانبية خطيرة، فقد تصبح جزءًا رئيسيًا من علاجات مركبة تهدف إلى التحكم طويل الأمد في HIV بدون دواء.
الاستشهاد: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
الكلمات المفتاحية: علاج شفاء فيروس HIV, علاج بالخلايا التائية, مستودع الفيروس, مستقبل ثنائي التخصص, تجربة سريرية