Clear Sky Science · ar
المشهد الوظيفي للتعبير البديل في تحديد مسار الخلايا المكونة للدم
كيف تشكّل تعديلات صغيرة على الجينات دمنا
كل ثانية، يصنع جسمك ملايين الخلايا الدموية الجديدة. وراء هذا المعجزة الهادئة توجد منظومة تحرير جزيئية قادرة على قص ولصق أجزاء من الرسائل الوراثية بطرق مختلفة، مكوِّنة نسخًا متباينة قليلاً من نفس البروتين. تستكشف هذه الدراسة كيف يساعد هذا التحرير، المسمى بالقص البديل، في توجيه الخلايا الجذعية غير الناضجة لتتحول إلى خلايا حمراء أو خلايا بيضاء أو أنواع دموية أخرى — وماذا يحدث عندما يغيب جزء معدل واحد.
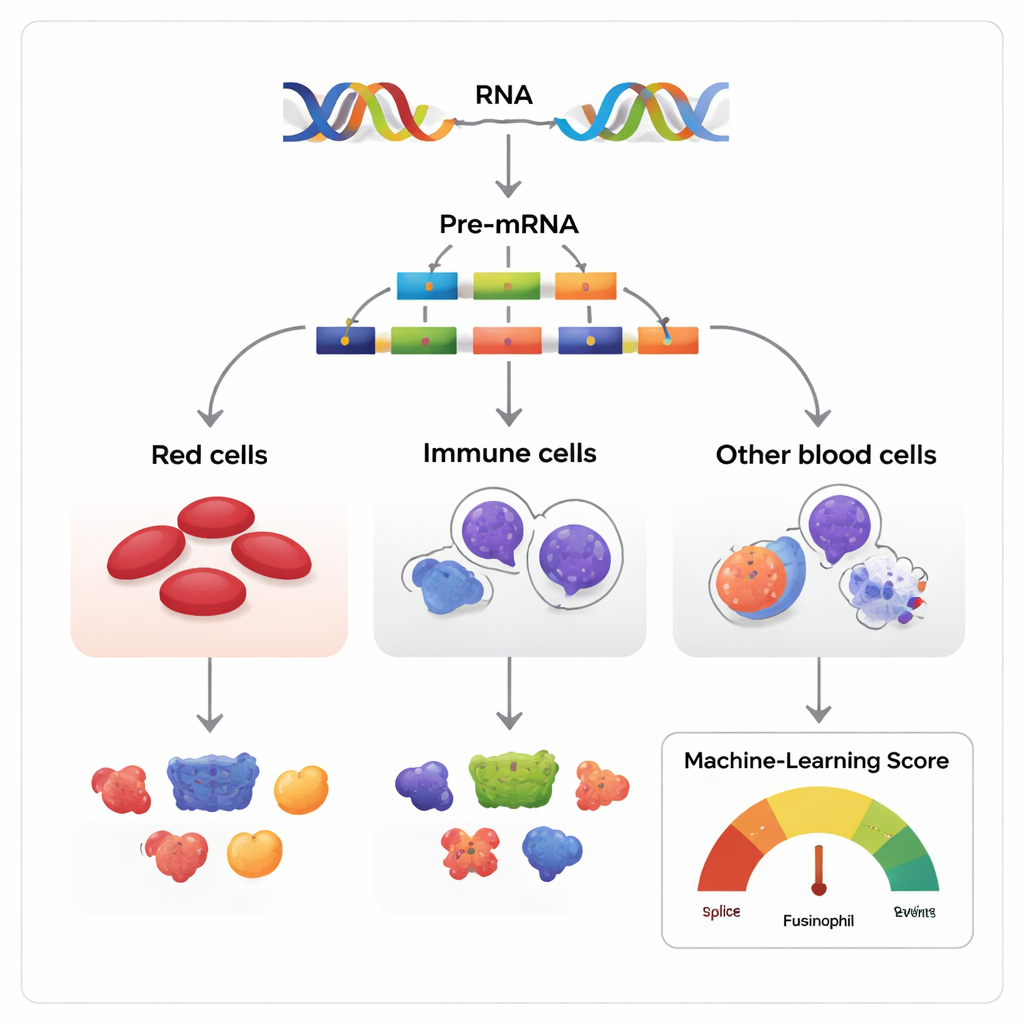
إصدارات متعددة من نفس النص الجيني
غالبًا ما تُوصف الجينات بأنها مخططات، لكن في الواقع هي أشبه بنصوص يمكن إعادة ترتيبها. عندما تُقرأ الجينات، تحتوي النسخة الأولية من الـRNA على مقاطع تُسمى الإكسونات يمكن الاحتفاظ بها أو تجاوزها قبل أن تُحوّل الرسالة النهائية إلى بروتين. نظر الباحثون في هذه العملية، المعروفة بتجاوز الإكسون، عبر أنسجة مكوّنة للدم في الإنسان والجرذان وعدة فقاريات أخرى. جمعوا أكثر من 270 مجموعة بيانات RNA تتابع معًا الخلايا الجذعية والبروجنitor المكوّنة للدم أثناء نضوجها إلى ثلاث عائلات رئيسية: الخلايا الحمراء المنتجة للحمض الحديدي، والخلايا النخاعية Myeloid المقاتلة للعدوى، والخلايا اللمفاوية المنتجة للأجسام المضادة.
ترتيب أي تغيّرات القص مهمة فعلاً
نظرًا لأن معظم الجينات متعددة الإكسونات يمكن أن تُقصَّص بعدة طرق، يكمن التحدي المركزي في تمييز التباينات البريئة عن تلك التي تؤثر فعليًا في مصير الخلية. بنى الباحثون نموذجًا للتعلّم الآلي أطلقوا عليه درجة القص الوظيفي (FAScore) لمعالجة هذه المشكلة. لكل حدث تجاوز إكسون، يأخذ النموذج في الاعتبار 19 معلومة، مثل مدى تغير استخدامه أثناء تطور الخلية، ومدى حفاظ التسلسل المحيط عبر الأنواع، وما إذا كان يغيّر مجالات بروتينية معروفة، وما إذا كان يحتوي مواقع لتعديلات كيميائية للبروتين. يُدرَّب الخوارزم، باستخدام إستراتيجية إيجابية–غير معنونة ومصنف الغابة العشوائية، ليخرج درجة بين 0 و1 تشير إلى احتمال تأثير حدث القص وظيفيًا.
اكتشاف مفاتيح محمية ومحددة للسلالة
بتطبيق FAScore على عشرات الآلاف من أحداث تجاوز الإكسون، صنَّف الفريق هذه الأحداث إلى مجموعات مرجَّحة أن تكون وظيفية، أو غير وظيفية، أو غير مؤكدة. كانت الأحداث المتوقعة كوظيفية أكثر تواجدًا في مناطق بروتينية مهمة للتفاعلات، وفي تسلسلات محفوظة تطوريًا، وفي مقاطع تستضيف علامات كيميائية مثل الفسفرة أو الSUMOylation. كما أن العديد من هذه الأحداث كانت نشطة فقط في سلالات دموية محددة أو أثناء تكوّن الدم الجنيني، ما يشير إلى أنها تعمل كمفاتيح مضبوطة بدقة خلال نوافذ تطورية معينة. أظهرت الدراسة كذلك أن بعض أحداث القص الأقدم — تلك المشتركة عبر الفقاريات لمئات الملايين من السنين — من المرجح أن تكون وظيفية بشكل خاص، مما يعكس كيف تميل الجينات الأقدم إلى حمل أدوار بيولوجية أساسية.
دليل تجريبي: تعديل نتائج تكوّن الخلايا الدموية
لاختبار توقعات النموذج، اختار المؤلفون عدة إكسونات عالية الدرجة في جينات نشطة في سلالات دموية مختلفة وحذفوا تلك الإكسونات في خلايا جذعية وبروجنitor دموية للفأر باستخدام CRISPR. تطابقت النتائج مع توقعات النموذج: إزالة إكسونات معينة في جينات KLF6 وSSBP3 أضعفت تكوين مستعمرات نَخاعية دون الإضرار بإنتاج الخلايا الحمراء، بينما غيَّرت إزالة إكسونات في EPB41L1 وTBC1D23 تشكيل المستعمرات الحمرية. على وجه الخصوص، أدى تجاوز الإكسون 15 في TBC1D23 إلى تقليل إنتاج نُسَلاً من خلايا الدم الحمراء في الفئران والأسماك الزارعة (زِبرافِيش)، مما نتج عنه عدد أقل من كريات الدم الحمراء الدائرة ومستويات هيموغلوبين أقل، مع حفاظ نسبي على الخلايا البيضاء.
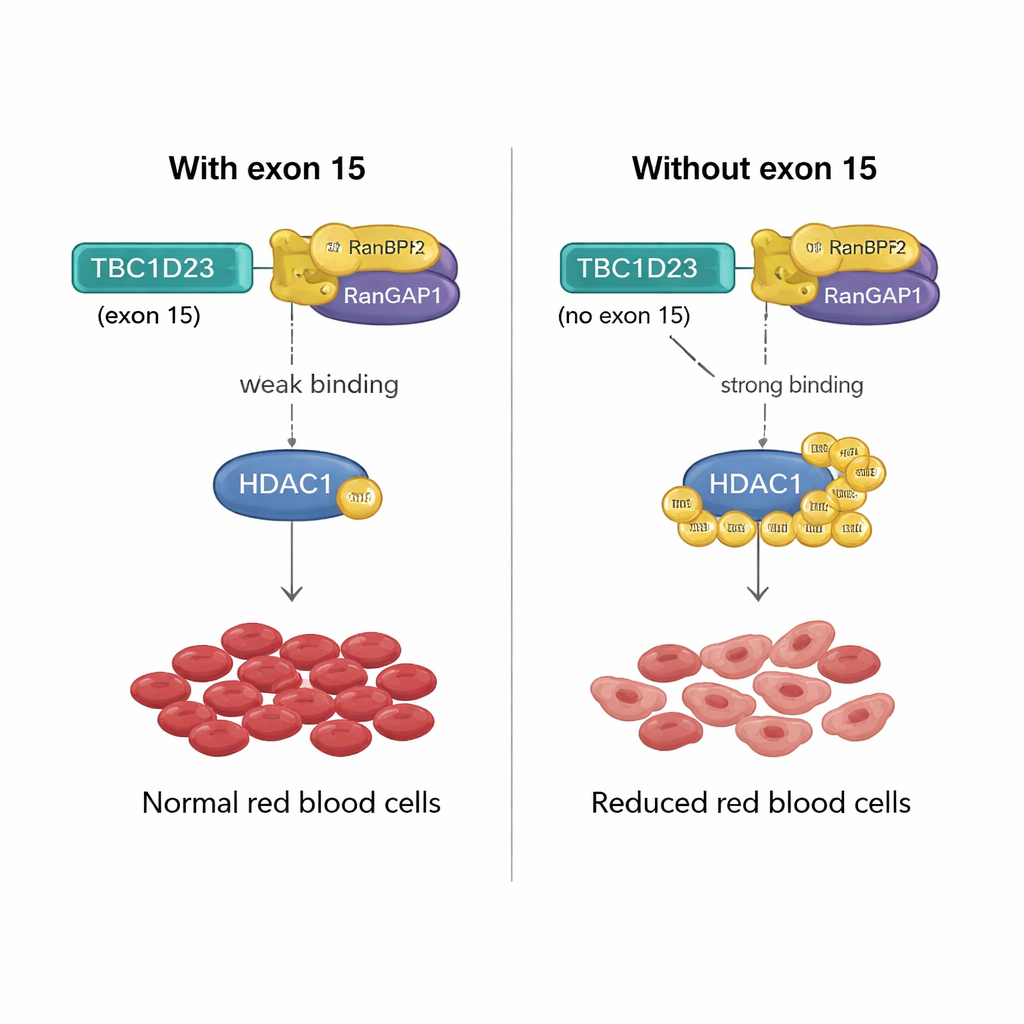
كيف يمكن لمقطع مؤلف من 15 حمضًا أمينيًا مشفَّر بواسطة الإكسون 15 في TBC1D23 أن يحدث مثل هذا التأثير؟ وجد الفريق أن إدراج هذا الإكسون يضعف ارتباط TBC1D23 بزوج بروتينات يُدعى RANBP2/RANGAP1، اللذان يتعاونان لإرفاق علامات SUMO إلى بروتينات أخرى. بدون الإكسون 15، يرتبط TBC1D23 بهذا الزوج بشكل أقوى، مما يعزز SUMOylation لإنزيم رئيسي هو HDAC1. هذا التوسيم المعزز يغيّر نشاط العديد من عوامل النسخ — المنظمين الرئيسيين للتعبير الجيني — مما يعطّل البرامج الجينية اللازمة للنضج السليم للخلايا الحمرية. عندما صنع الباحثون نسخة من HDAC1 لا يمكن تمييزها بعلامات SUMO في موضعين حاسمين، أعاد ذلك تكوين الخلايا الحمرية في الخلايا التي تفتقد إكسون TBC1D23 15، مؤكّدين أن هذا التوسيم الكيميائي هو الخطوة الحرجة.
لماذا يهم هذا للصحة والعلاجات المستقبلية
لغير المتخصص، رسالة هذا العمل هي أن ليس كل التغييرات الجينية متكافئة: في بعض الأحيان يكمن الفرق بين دم صحي وفقر دم في ما إذا كان جزء صغير من جين يُحتفظ به أو يُتجاوز في الرسالة النهائية. من خلال دمج بيانات RNA واسعة النطاق مع نظام تصنيف متطور، تقدّم الدراسة خارطة طريق لتحديد أي متغيرات القص من المرجح أن تؤثر في كيفية اختيار الخلايا الجذعية لمصائرها. لا يقتصر هذا النهج على تعميق فهمنا لتكوين الخلايا الدموية في الصحة والمرض فحسب، بل يقدم أيضًا استراتيجية عامة لتحديد أحداث القص الهامة في أعضاء أخرى، ما قد يوجّه علاجات جينية مستقبلية وعلاجات دقيقة.
الاستشهاد: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
الكلمات المفتاحية: القص البديل, تكوّن الدم, التعلّم الآلي, كريات الدم الحمراء, تنظيم الجينات