Clear Sky Science · ar
توصيل مشابِكات الببتيد لتشكيل مراكز تفاعل مستقرة داخل الخلايا
بناء "محطات عمل" جديدة داخل الخلايا
خلاياّنا مليئة بمحطات عمل صغيرة تُؤدى فيها مهام مهمة — مثل إنتاج الطاقة أو الاستجابة للإجهاد. مع مرور الوقت، أو في حالات المرض، قد تتدهور هذه المحطات الطبيعية. تستكشف هذه الدراسة طريقة لإضافة "مراكز تفاعل" جديدة داخل الخلايا الحية باستخدام قطرات بسيطة مُصنّعة في المختبر مكوّنة من ببتيدات قصيرة. يمكن لهذه المراكز التركيبية أن تحتجز بروتينات محددة، وتكثفها، بل وتساهم في تدميرها، مما يقترح استراتيجيات جديدة للعلاجات المستقبلية وهندسة الخلايا.
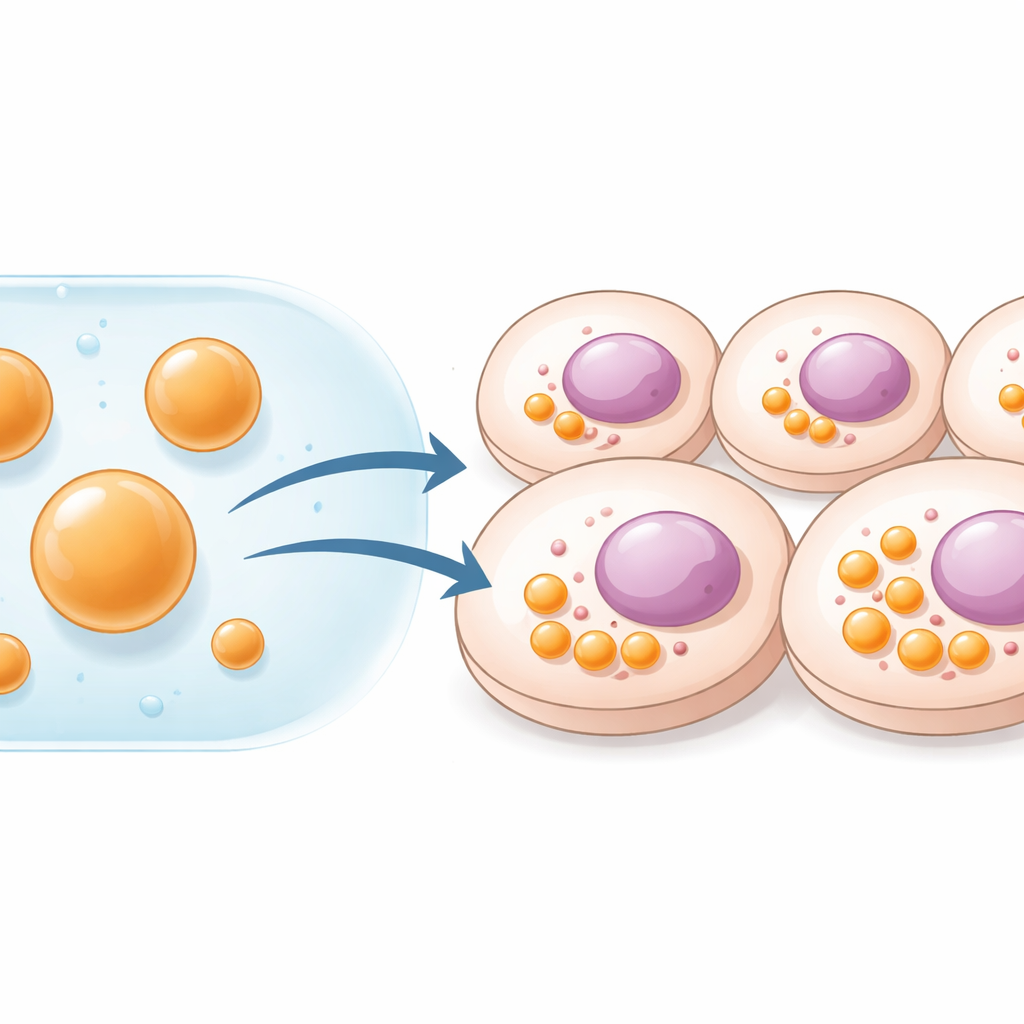
لماذا تحتاج الخلايا محطات عمل مخصّصة
تحافظ الخلايا على النظام بتقسيم المهام المختلفة إلى مقصورات متميزة. بعضها محاط بأغشية، مثل الميتوكوندريا؛ والبعض الآخر أكثر ليونة، على شكل قطرات تتكوّن عندما تتجمع بروتينات وريبونوكلييك أساسية. تعمل هذه القطرات المائعة، أو المكثفات، كمراكز تفاعل تُسَرّع أو تُوقِف مسارات كيميائية حيوية معيّنة. سبق للعلماء أن صمّموا مثل هذه المقصورات بجعل الخلايا تُنتج بروتينات سقالة خاصة عبر إدخال جينات. رغم فعالية هذه الطريقة، فهي تتطلب توصيل الحمض النووي وتحد من كمية المواد التي يمكن للخلايا إنتاجها. حاول مؤلفو هذه الدراسة تجاوز الحمض النووي بالكامل وبناء مقصورات جاهزة خارج الخلية، ثم توصيلها مباشرة كقُطيرات مستقرة بحجم ميكروني.
قطرات ببتيدية تُشكّل مراكز تفاعل مستقرة
عمل الفريق مع ببتيدات قصيرة غير منظمة تُعرف باسم HBpep ومتغيّر حساس للأكسدة والاختزال، HBpep‑SA. تحت ظروف حمضية خفيفة تظل هذه الببتيدات مذابة، لكن عندما يُغير الرقم الهيدروجيني إلى مستويات قريبة من الفيزيولوجية — أو عند خفض الحرارة — تنفصل أطوارها لتكوّن قطرات ناعمة شبيهة بالهلام بحجم نحو 1–5 ميكرومترات. من خلال ضبط تركيز الببتيد، تمكن الباحثون من التحكم في حجم وعدد القطرات. أظهرت تقنيات الفلورة أن جزيئات الببتيد داخل هذه القطرات تتحرك ببطء، مما يشير إلى حالة هلامية متماسكة بما يكفي لتحمل التخفيف والمعالجة. عند إضافتها إلى مزروعات لخلايا سرطانية بشرية، وخلايا ميلانوما فأرية، وخلايا مناعية بشرية أولية، استُؤصلت القطرات بكفاءة وتجَمَّعت في السيتوبلازم. القطرات الأكبر، لا سيما، بقيت سليمة لما لا يقل عن خمسة أيام، فتعمل عمليًا كعضيات تركيبية اصطناعية طويلة العمر داخل الخلايا الحية.
تحميل وتوجيه المراكز
لكي تكون هذه المراكز مفيدة، يجب أن تحتفظ بالبروتينات الحمولية وتُنظمها. حسّن الباحثون أولًا التحميل عن طريق إرفاق وسم قصير مشتق من HBpep إلى بروتين نموذجي، GFP. شجّع هذا الوسم GFP على الانقسام بقوة إلى القطرات، وبشكل لافت، على التركّز قرب أسطحها، مكوّنًا تنظيمًا من نوع النواة‑القشرة. بعد ذلك أدخلوا النانوبوديّات — بروتينات صغيرة شبيهة بالأجسام المضادة تلتصق بقوة بأهداف مختارة — داخل القطرات. سمحت نانوبوديّات مرتبطة بـGFP للمراكز بأن تلتقط GFP انتقائيًا في الأنابيب وفي الخلايا. نظرًا لكثافة هلام الببتيد، تراكم معظم GFP المحتجز بدايةً عند سطح القطرات. لكن عندما ارتخى البنية الداخلية جزئيًا، إما بتغيير ظروف الأكسدة والاختزال أو بمساعدة القطرات على الهروب من أغشية الإندوسومات المحيطة بها، بدأ GFP أيضًا بالتغلغل إلى الداخل. داخل الخلايا، زادت المساعدات الكيميائية التي تعزز هروب الإندوسومات بشكل كبير نسبة المراكز التي نجحت في تجنيد أهدافها.
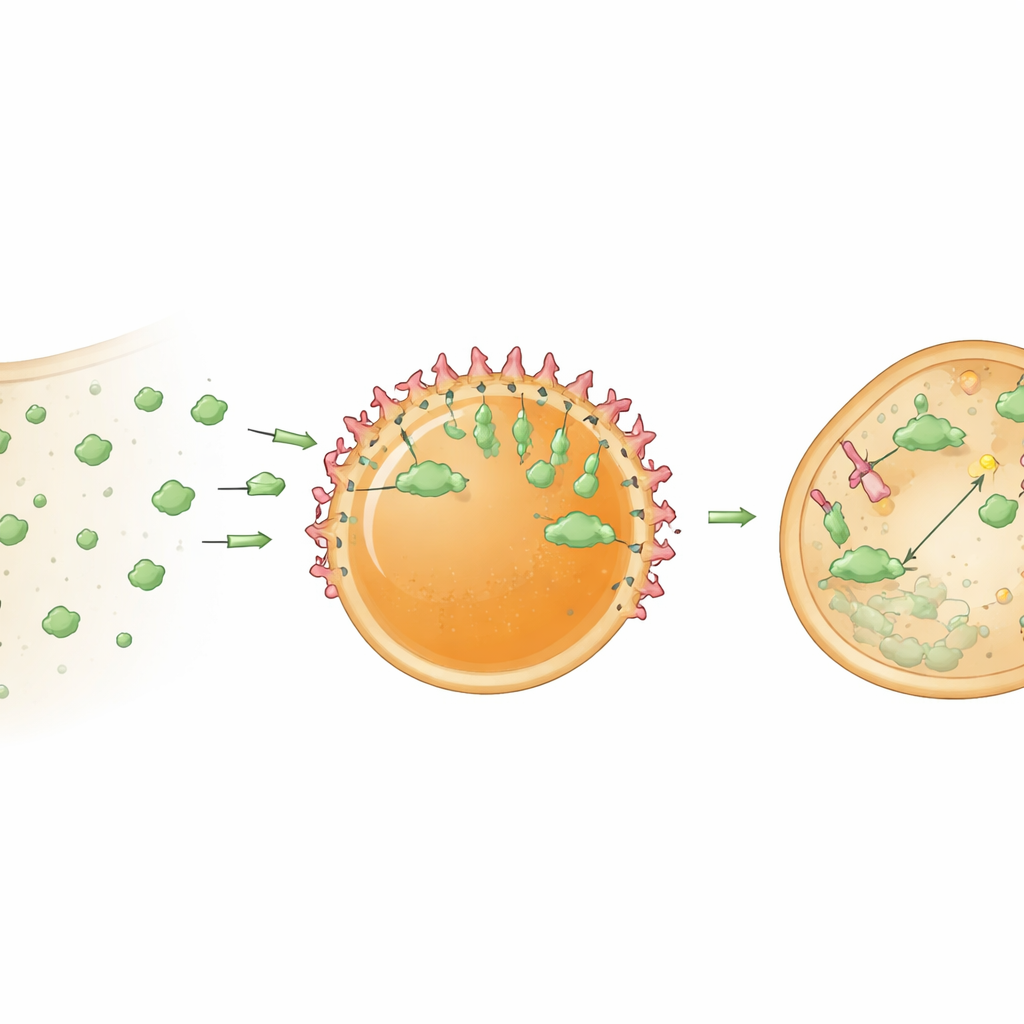
تحويل المراكز إلى مفرِّمات للبروتين
ارتقى المؤلفون بعد ذلك بهذه المراكز من فخاخ سلبية إلى مراكز معالجة نشطة. حمّلوا القطرات ببروتين bioPROTAC — وهو بروتين اندماجي يجمع بين نانوبودي يربط الهدف وجزء من موائم إنزيمي يؤشر البروتينات للتدمير عبر آلية التخلص في الخلية. عندما وُصلت هذه القطرات "المحللة" إلى خلايا معبرّ فيها عن GFP بشكل مستقر، انخفضت مستويات GFP السيتوسولي بحوالي 78 بالمئة خلال يوم واحد. المراكز الضابطة التي احتوت فقط على النانوبودي احتجزت GFP لكنها لم تقلل مستواه العام بشكل ملحوظ، مما يؤكد أن الانخفاض الكبير ناتج عن التحلل الموجَّه لا عن الالتقاط البسيط. تشير النتائج إلى أن تجميع bioPROTACs داخل بيئة ميكروية مكثفة يجعلها أقوى بكثير مما لو كانت متفرقة في السيتوبلازم.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن العلماء يمكنهم تصنيع قطرات قائمة على الببتيد في أنبوبة اختبار، وعبئها بأدوات بروتينية مخصّصة، ثم توصيلها إلى خلايا حية حيث تتصرف كعضيات جديدة وطويلة الأمد. تستطيع هذه المراكز التركيبية سحب البروتينات الطبيعية انتقائيًا، وعندما تُزوَّد بآليات التحلل، يمكنها إزالة أهداف مختارة من الخلية بنشاط. وبما أن هذه المنصة تتجنب تعديل جينوم الخلية وتتمتع بالقدرة على حمل عناصر متنوعة بشكل معياري، فإنها تفتح مسارًا نحو علاجات تعيد أو تعيد كتابة سلوك الخلايا — مثل إزالة البروتينات الضارة أو إعادة توجيه الإشارات المعيبة — عبر تثبيت "محطات عمل" جديدة قابلة للبرمجة داخل خلايانا.
الاستشهاد: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
الكلمات المفتاحية: عضيات تركيبية, مشابِكات الببتيد, تسليم داخل الخلايا, تحلل البروتين, هندسة الخلايا