Clear Sky Science · ar
القطع الثانوي بواسطة CRISPR-Cas9 يتعثر بسبب حلقة R محاطة، وفاصل مطوَّل، ومجال HNH غير نشط
لماذا تهم القطوع الدقيقة في الحمض النووي
تشتهر تقنية CRISPR-Cas9 باعتبارها مشرطًا جزيئيًا قادرًا على قطع الحمض النووي في مواقع مُختارة، لكن لهذا الأداة سلوكًا ثانويًا أقل شهرة: بمجرد تنشيطها، يمكنها أيضًا قَضم أجزاء أخرى من المادة الوراثية القريبة. فهم متى يتشغّل أو يتوقف هذا القطع «الجانبي» أمر بالغ الأهمية لتطوير علاجات تحرير جينات أكثر أمانًا واختبارات تشخيصية أكثر حساسية. تفكك هذه الدراسة السمات البنائية والفيزيائية لمجمع Cas9–DNA–RNA التي تحدد ما إذا كان Cas9 سيُنجز قطعه المقصود بهدوء، أم سيبدأ أيضًا في تمزيق خيوط مفردة من الحمض النووي العالقة.
كيف تبدأ المقصّات الجزيئية عملها
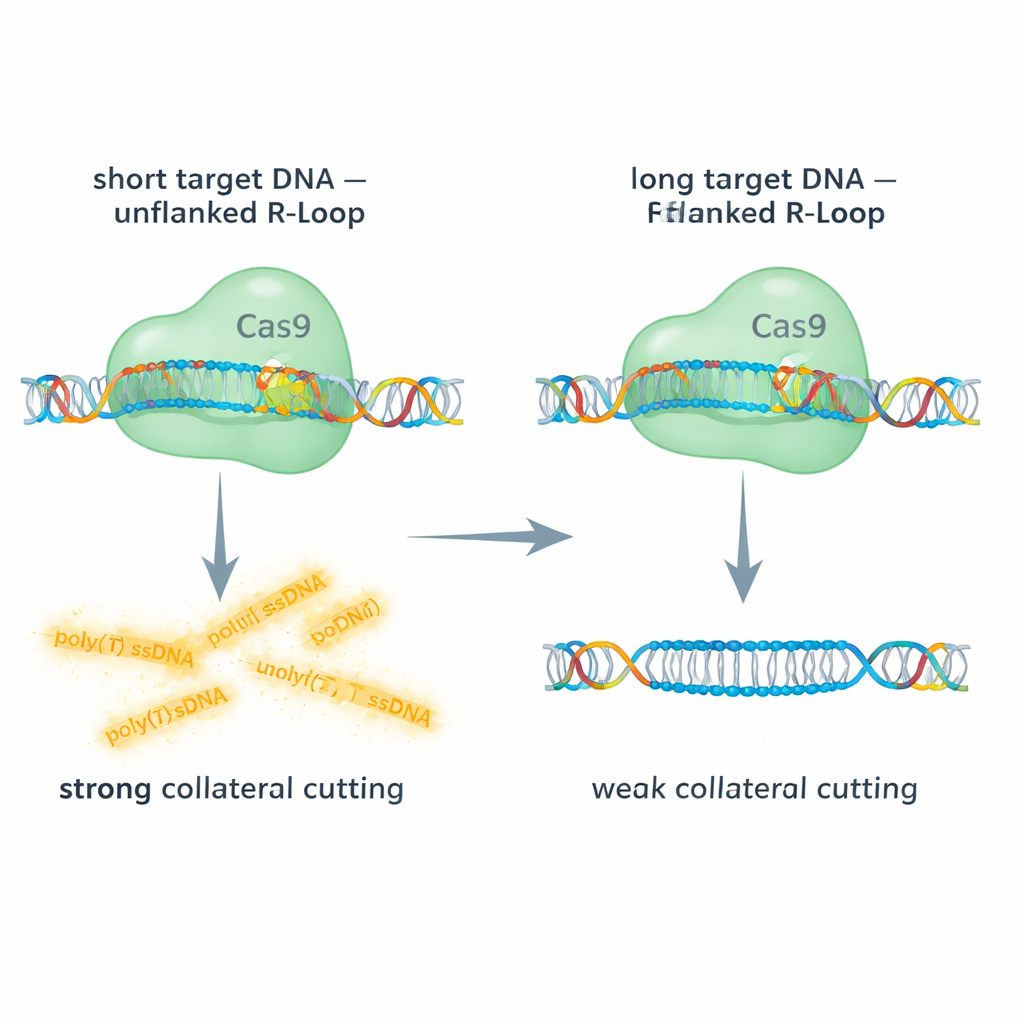
لكي يعمل، يرتبط Cas9 بقطعة قصيرة من الحمض النووي الريبوزي الإرشادي التي توجهه إلى تسلسل مطابق في الجينوم. عندما يجد Cas9 الهدف، يقترن الحمض النووي الريبوزي بأحد خيطي الحمض النووي، مما يفصل الخيطين ويُنشئ منطقة هجين DNA–RNA تُسمى حلقة R. في دوره التقليدي، يقطع Cas9 الخيطين عند تلك البقعة. لكن أعمالًا حديثة أظهرت أنه بعد تنشيطه بهذه الطريقة، يمكن لمجال القطع RuvC أن يقطع أيضًا سلاسل مفردة غير ذات صلة من الحمض النووي، مثل تراكيب بولي(تي)، في أماكن أخرى من المحلول. طرح الباحثون السؤال التالي: ما هي السمات الهندسية والبنائية الدقيقة لتسلسل الهدف والحمض النووي الريبوزي الإرشادي التي تجعل هذا النشاط الجانبي قويًا أو ضعيفًا أو غير موجود؟
أهداف قصيرة مقابل طويلة: إعطاء Cas9 مساحة للحركة
قارن الفريق عمل Cas9 على أهداف ثنائية الشريط قصيرة وطويلة باستخدام قراءات فلورية لتتبع كل من القطع على الهدف والقطع الجانبي لمسبار من حمض نووي أحادي الشريط. مع الأهداف القصيرة، كانت حلقة R عند الطرف 5′ للحمض النووي الريبوزي الإرشادي «غير محاطة» — لم يكن هناك حمض نووي ثنائي الشريط يواصل ما بعد منطقة الهجين. تحت هذه الشروط، أظهر Cas9 نشاطًا جانبيًا قويًا على الحمض النووي أحادي الشريط. بالمقابل، عندما استخدموا مقاطع DNA أطول تركت حمضًا نوويًا ثنائي الشريط يحيط بحلقة R، انخفض القطع الجانبي بشكل كبير، أحيانًا بنحو 90%، رغم أن القطع الأساسي على الهدف لا يزال يحدث. استهداف DNA أحادي الشريط طويل، الذي يزيل حلقة R تمامًا، أعاد النشاط الجانبي إلى حد كبير. تكشف هذه المقارنات أن «غطاء» ثنائي الشريط بجانب حلقة R يُقوّي المجمع ويعيق ماديًا الوصول أو المرونة اللازمة لمجال RuvC لقطع خيوط أخرى.
التعديل الدقيق بطول الدليل والاختلافات المطابقة
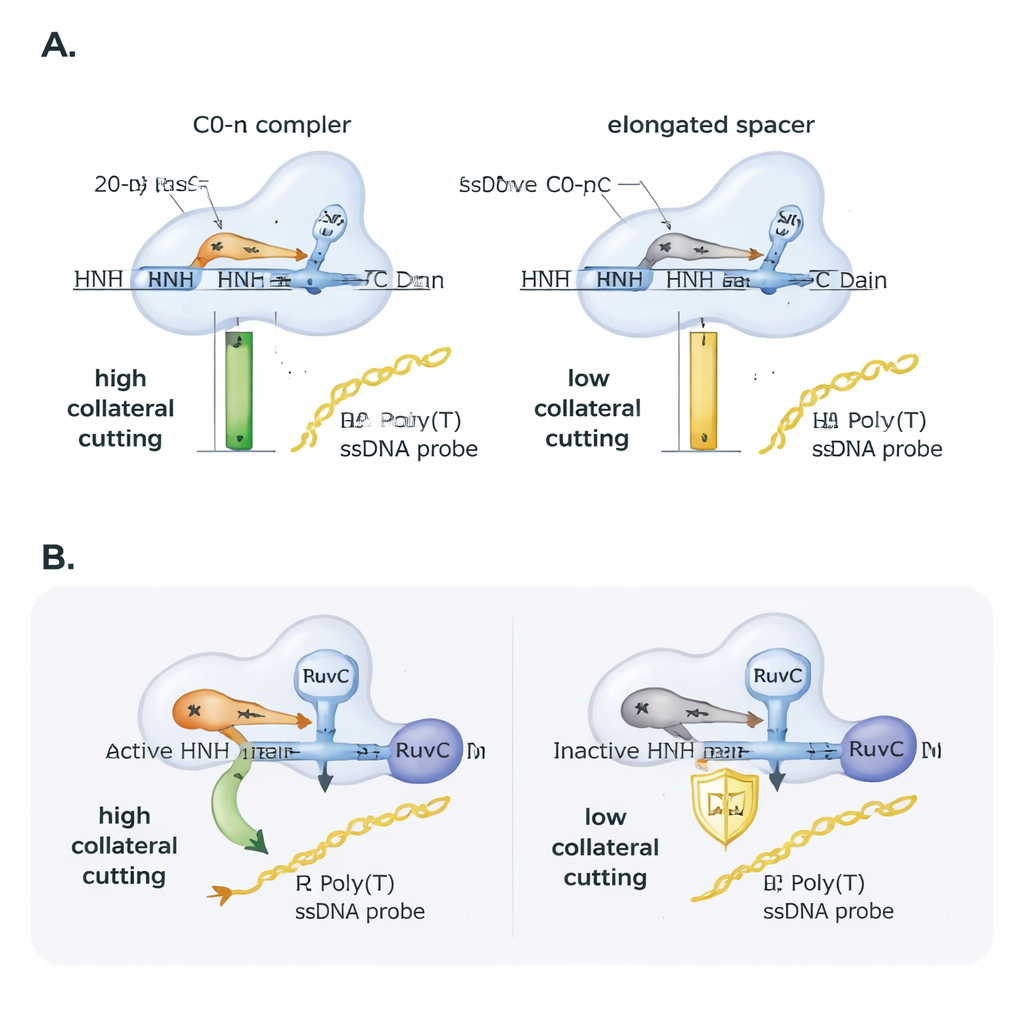
استكشف الباحثون بعد ذلك كيف يضبط الحمض النووي الريبوزي الإرشادي هذا السلوك. أدخلوا اختلافات صغيرة أحادية القاعدة بين الدليل والهدف وتابعوا مدى استمرار Cas9 في القطع. تحمل القطع الأساسي على الهدف العديد من الاختلافات أحادية القاعدة، لكن القطع الجانبي كان أكثر هشاشة واعتمد بقوة على الموقع الدقيق للاختلاف، مما يبرز حساسيته. بعد ذلك، مددوا فاصل الحمض النووي الريبوزي الإرشادي منهجيًا إلى ما بعد الطول المعتاد 20 قاعدة. على الرغم من أن Cas9 ما زال قادرًا على الالتقاط وقطع الهدف، انخفض النشاط الجانبي تقريبًا بشكل خطي مع زيادة طول الفاصل: إضافة قاعدتين فقط قلّصت النشاط الجانبي بنحو النصف، وإضافة أربع قواعد خفضته أكثر. في اختبارات عملية باستخدام مواد جينية من SARS-CoV-2، أعطت فقط أمبيكونات DNA المصممة لإنتاج حلقة R غير محاطة مع دليل بطول قياسي إشارة جانبية قوية، ما يبرز أن تصميم البرايمر والدليل يمكن أن يصنع أو يفسد اختبارات الكشف المستندة إلى CRISPR.
مجال مساعد أساسي وراء الكواليس
يحتوي Cas9 على مجالين قاطعين، RuvC وHNH. ربطت أعمال سابقة القطع الجانبي مباشرةً بـRuvC، لكن هذه الدراسة تُظهر أن HNH لا يزال ذا أهمية. عندما استخدم المؤلفون نسخة من Cas9 بميدان HNH غير نشط، انهار النشاط الجانبي، رغم أن الارتباط بالهدف وسلوك الشقّ ظلا قائمين. بشكل مثير، إذا زودوا Cas9 بهدف DNA كان مشقوقًا بالفعل في أحد الخيطين، استعادت نسخة HNH غير النشطة النشاط الجانبي بمستوى مشابه للإنزيم العادي. هذا يشير إلى أن دور HNH جزئيًا ميكانيكي: عن طريق قصّ أو إرخاء الخيط المستهدف، يساعد البروتين على الانتقال إلى شكل يكشِف RuvC نحو الحمض النووي أحادي الشريط القريب. دعمت التحليلات الهيكلية لنماذج ثلاثية الأبعاد موجودة هذا التصور، مبينة أن حلقات R غير المحاطة والأدلة بطول قياسي تسمح للطرف 5′ من الـRNA بأن «يغطّي» مقابل Cas9 وتضع المناطق التحفيزية بشكل مناسب، بينما الحلقات المحاطة والأدلة المطوَّلة تضغط البروتين بإحكام أكثر وتحتمل أن تحجب موقع RuvC عن الخيوط العابرة.
ما الذي يعنيه هذا للأدوات المستقبلية
لغير المتخصصين، الرسالة الأساسية أن سلوك Cas9 ليس مسألة كل شيء أو لا شيء: التفاصيل الهندسية الدقيقة — مدى امتداد الـDNA، طول الدليل، وما إذا كان المجال المساعد يمكنه إتمام قطعه — تقرر ما إذا كان الإنزيم يلتزم بمهمته الرئيسية أو يشرع أيضًا في تمزيق الخيوط المفردة المحيطة. الأهداف القصيرة التي تترك حلقة R غير محاطة، الأدلة القياسية بطول 20 قاعدة، ومجال HNH النشط تشجع معًا نشاطًا جانبيًا قوياً؛ أما الـDNA المحاط الطويل، والأدلة المطوّلة، أو مجال HNH غير النشط فتكبحه. تمنح هذه الرؤى الباحثين قابض ضبط أكثر دقة لـCas9، تساعدهم على تصميم أنظمة تحرير جينات أكثر أمانًا تتجنب الأضرار الجانبية غير المرغوبة، أو اختبارات تشخيصية أقوى تستغل هذا النشاط الجانبي عمدًا للكشف عن كميات ضئيلة من المادة الفيروسية أو الجينية.
الاستشهاد: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
الكلمات المفتاحية: CRISPR-Cas9, القطع الجانبي, حلقة R, فاصل الحمض النووي الراهن الإرشادي, تشخيص الأحماض النووية