Clear Sky Science · ar
إنزيم NatA يشارك في مركبات متعددة العوامل عند مخرج نفق الببتيد في الريبوسوم
كيف تضبط الخلايا البروتينات الجديدة أثناء نشأتها
تصنع خلاياك آلاف البروتينات الجديدة كل ثانية على آلات صغيرة تُسمى الريبوسومات. عند بروز كل سلسلة بروتينية، يجب تقليمها ووضع علامات عليها وطيها بشكل صحيح، وإلا فقد تُخطئ في أدائها وتساهم في المرض. تدرس هذه الدراسة أحد أنظمة الوسم الرئيسية، تعديل يُدعى الأسيتلة الطرفية N، وتوضح كيف يعمل مركب إنزيمي مركزي، NatA، جنبًا إلى جنب مع عدة شركاء عند المكان الذي تخرج عنده البروتينات الجديدة من الريبوسوم. فهم هذا التنسيق يوضح كيف تحافظ الخلايا على تشغيل مصانع البروتين بسلاسة.
الوسم الكيميائي الصغير الذي يُحدث فرقًا
تبدأ معظم البروتينات حياتها بنفس وحدة البناء الأولى، الحامض الأميني ميثيونين. غالبًا ما يُزال هذا الميثيونين الابتدائي ويُستبدل بعلامة كيميائية صغيرة تُسمى مجموعة أسيتيل. تُضاف هذه العلامة إلى طرف البروتين الأمامي (طرف N)، ويمكن أن تؤثر على مدة بقاء البروتين، ومكانه داخل الخلية، ووظيفته. نوعان رئيسيان من الإنزيمات يجلسان عند مخرج نفق الريبوسوم لإدارة هذه المرحلة الأولى من التعديل: ميثيونين أمينوببتيدازات (MAPs)، التي تقص الميثيونين الابتدائي، وإنزيمات ناقلة الأسيتيل الطرفية N (NATs)، التي تضيف علامة الأسيتيل. من بين هذه الإنزيمات، يعتبر NatA العامل الرئيسي في الخلايا البشرية، وقد يعدل ما يقرب من 40% من البروتينات. وبما أن العديد من البروتينات تُنتَج في آن واحد، يجب على الخلية تنظيم هذه الإنزيمات بحيث يحدث التقليم والوسم بسرعة وبالترتيب الصحيح.
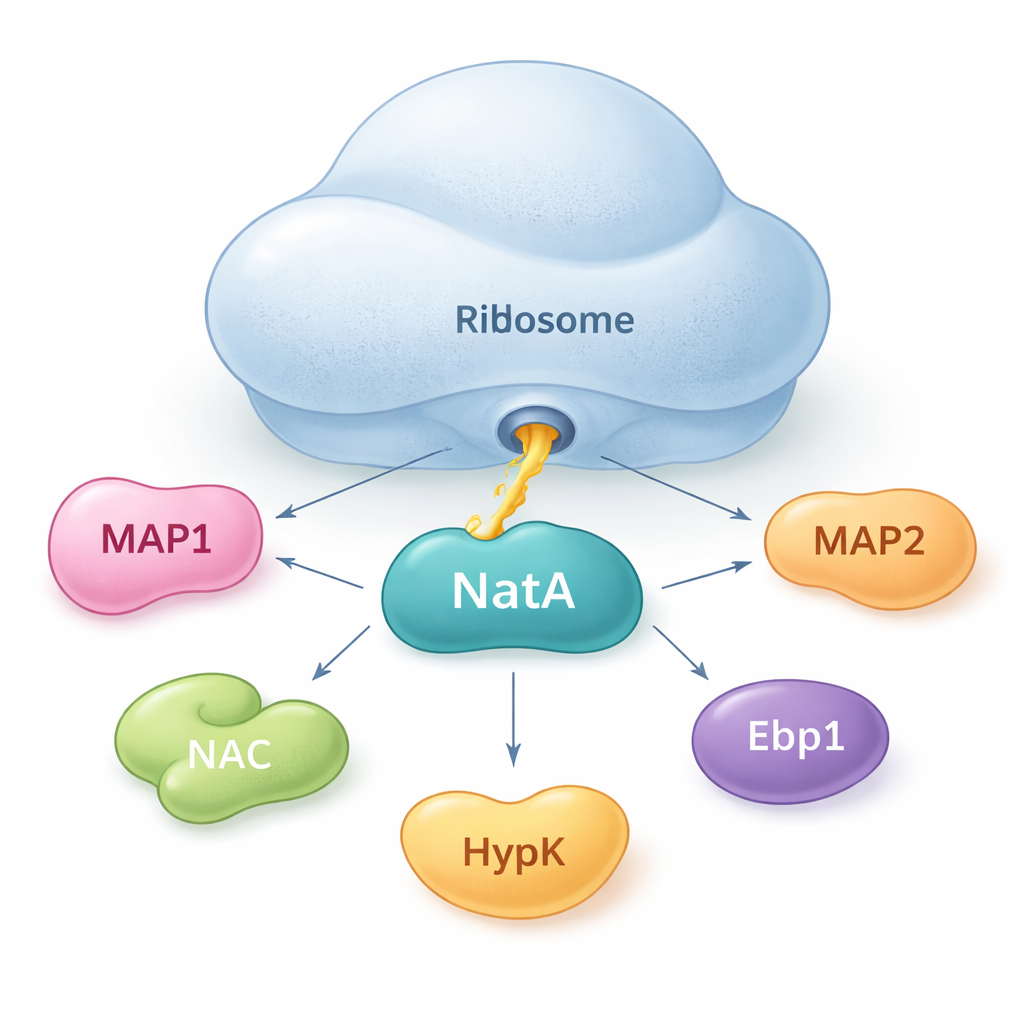
NatA كنقطة تجمع لمساعدي البروتين
يبين المؤلفون أن NatA لا يعمل بمفرده. بل يتصرف كمحور يجمع عدة بروتينات مساعدة، سواء على الريبوسوم أو خارجه. باستخدام قياسات ارتباط حساسة في المحلول، وجدوا أن NatA يمكنه تشكيل مركبات قوية مع MAP1، والمجمع المرتبط بالسلاسل الناشئة (NAC)، والبروتين المنظم HypK، وإنزيم آخر Naa50، حتى في غياب الريبوسوم. يمكن لـ NAC أن يجسر NatA إلى MAP1، مما يسمح بربط مرحلتي القص والوسم داخل تركيب واحد. ومع ذلك، يمكن أن يمنع HypK، الذي يثبط نشاط NatA عادة، ارتباط NAC. يوحي هذا بأن الخلايا قد تبدل NatA بين حالة أكثر نشاطًا مربوطة بـ NAC وحالة مقيدة مربوطة بـ HypK، بحسب احتياجاتها.
موضع تثبيت ثانٍ قرب مخرج النفق مباشرة
باستخدام المجهر الإلكتروني بالتبريد، وهو تقنية تصور الجزيئات الكبيرة بتفصيل يكاد يلامس الذري، اكتشف الباحثون أن NatA يمكن أن يرتبط بالريبوسوم في موضعين متميزين. أحدهما، المعروف سابقًا، يجلس بعيدًا قليلًا عن مخرج النفق. أما الموضع الجديد «القريب» فيضع لب NatA التحفيزي قريبًا جدًا من مكان بروز سلسلة البروتين المتنامية، مما يقصر المسافة التي يجب أن تقطعها السلسلة لتخضع للتعديل. وما يثير الاهتمام هو أن الموضعين يمكن أن يكونا مشغولين في الوقت نفسه، ما يعني أن نسختين من NatA يمكن أن تجلسا على نفس الريبوسوم. النسخة الأبعد تعمل كهيكل ومرساة، بينما تكون النسخة القريبة مثالية لوضع علامة على البروتينات الجديدة. كما تتلامس جزيئتا NatA مع بعضهما، مما يشير إلى أن NatA يمكنه تنسيق نسخاته لتشكل فرقًا متعددة الإنزيمات.
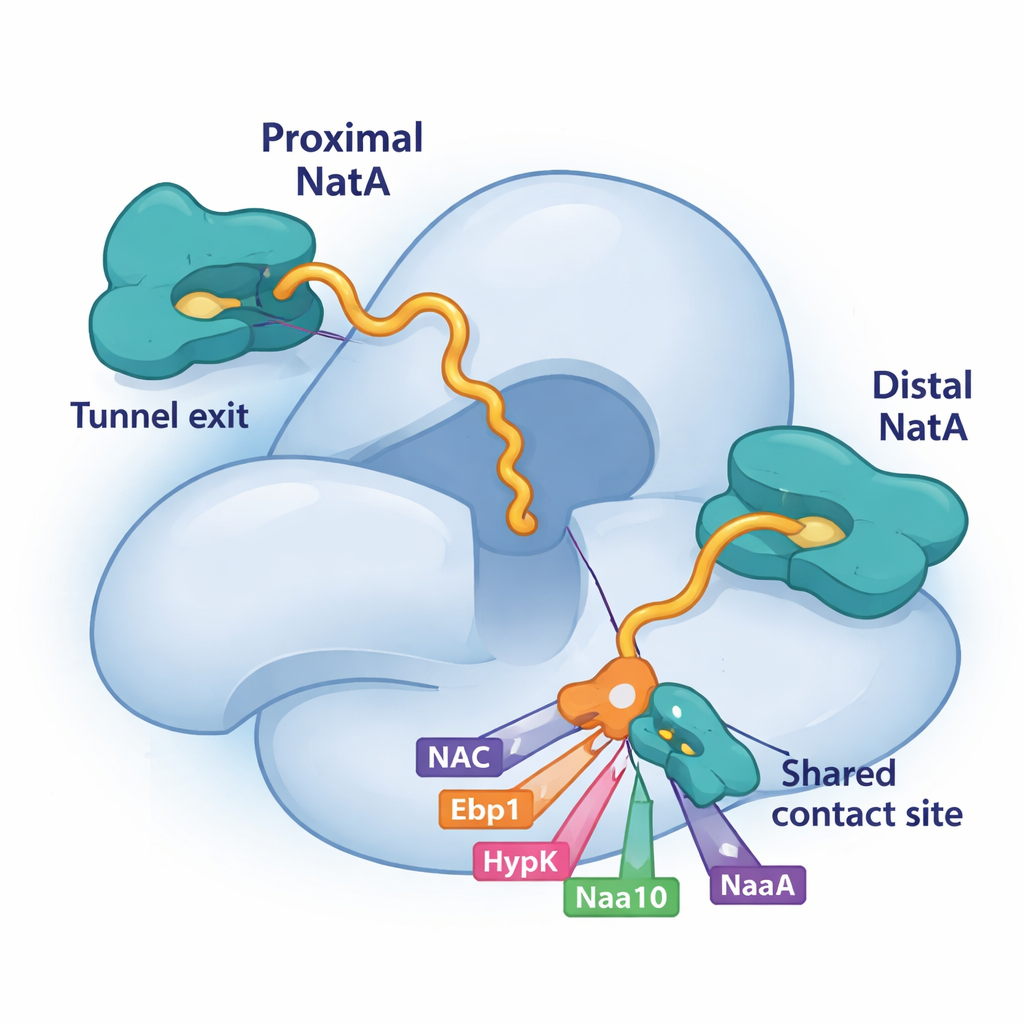
تنافس على لوحة هبوط مشتركة في NatA
عنصر أساسي في هذه الحكاية هو شق صغير على الوحدة الكبيرة من NatA، Naa15. تُظهر الدراسة أن أربعة عوامل مرتبطة بالريبوسوم—NAC وHypK وEbp1 وحتى مقطع ذيّل من وحدة NatA التحفيزية نفسها، Naa10—تستعمل حلقات قصيرة لالتحام بنفس البقعة تمامًا على Naa15. وبما أنهم جميعًا يعتمدون على لوحة هبوط مشتركة، فهم يتنافسون على الوصول إليها. عندما يشغل HypK الموقع، فإنه لا يطفئ نشاط NatA فحسب، بل يمنع أيضًا NatA من الارتباط بـ NAC أو تشكيل ثنائيات NatA–NatA. عندما يرتبط هناك NAC أو الإنزيم الزائف Ebp1 أو جزء Naa10 الطرفي القريب، يمكنهم إعادة تشكيل وضع NatA أو وصلاته على الريبوسوم. يمنح هذا الارتباط التنافسي الخلية طريقة مرنة لاختيار الشركاء المُجمّعين حول NatA في أي لحظة.
إنزيم زائف كمنظم لحركة المرور الجزيئية
البروتين Ebp1 يثير اهتمامًا خاصًا. يشبه أحد إنزيمات إزالة الميثيونين لكنه يفتقر إلى النشاط التحفيزي؛ إنه «إنزيم زائف». أظهرت أعمال سابقة أن Ebp1 يمكنه الجلوس على الريبوسوم قرب مخرج النفق ويشد شريطًا طويلًا من الـ RNA. في هذه الدراسة، يجد المؤلفون أنه عندما ينضم NatA إلى الريبوسوم، يتحرك Ebp1 عن موضعه، ويتخلى عن الـ RNA، ويستخدم بدلًا من ذلك حلزونه الخاص ليحتل نفس موقع الارتباط على Naa15 الذي يستخدمه NAC وHypK. توحي هذه إعادة الترتيبة بأن Ebp1 يمكن أن يعمل كحاجز مؤقت أو منظِّم: يشكل البيئة المحلية للـ RNA، ثم ينقل التحكم إلى إنزيمات نشطة مثل MAPs وNatA، من دون أن يُجرِي التفاعل الكيميائي بنفسه.
لماذا يهم هذا التحكم في الازدحام الجزيئي
قد تبدو تفاصيل الحلقات ومواقع الارتباط مجرد تفاصيل مجردة لغير المتخصص، لكن الرسالة بسيطة: تُدير الخلايا نظامًا منسقًا ومكوّنًا من عدة خطوات لمراقبة الجودة مباشرةً حيث تُولد البروتينات. يجلس NatA في مركز هذا النظام، قادرًا على استقطاب أو تحرير شركاء مختلفين اعتمادًا على من يفوز بالوصول إلى رقعة التثبيت الحاسمة وأي موقع ريبوسومي تحتله NatA. تساعد هذه الشبكة المرنة على ضمان أن يحدث التقليم والأسيتلة بالتوقيت والترتيب المناسبين لآلاف البروتينات المختلفة. وبما أن الأخطاء في معالجة الطرف N ترتبط باضطرابات النمو والتنكس العصبي والسرطان، فإن رسم خرائط كيفية تجمّع NatA وشركائه يعطي الباحثين مخططًا أوضح لكيفية التحكم في معالجة البروتين المبكرة—وكيفية استهدافها عندما تسوء الأمور.
الاستشهاد: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
الكلمات المفتاحية: مراقبة جودة البروتين, أسيتلة الطرف N, مخرج نفق الريبوسوم, مركب NatA, تعديل أثناء الترجمة