Clear Sky Science · ar
تؤدي فيكوزيلترانسفيراز النباتات FUT11 إلى تشويه ناقل السكر لتحفيز التفاعل عبر وسيط أكسوكربونيوني عابر
كيف تضبط النباتات السكريات على بروتيناتها بدقة
تُزَيَّن البروتينات داخل خلايانا وفي النباتات غالباً بسلاسل معقدة من السكريات تعمل كرموز شريطية تُرشد كيفية طي هذه البروتينات، مدة بقائها، والشركاء الذين يمكنها الارتباط بهم. تركز هذه الدراسة على إنزيم نباتي يُسمى FUT11 يضيف سكرًا صغيرًا، الفوكوز، إلى هذه السلاسل. من خلال كشف كيفية عمل FUT11 على المستوى الذري، يكشف المؤلفون خدعة مفاجئة: الإنزيم يشوّه لفترة وجيزة شريكه السكري لدفع خطوة كيميائية صعبة. فهم هذه العملية مهم ليس فقط للبيولوجيا الأساسية، بل أيضاً لتصميم أدوية مصنوعة في النباتات تكون أكثر أمانًا وتتجنّب إثارة استجابات مناعية غير مرغوب فيها في البشر.
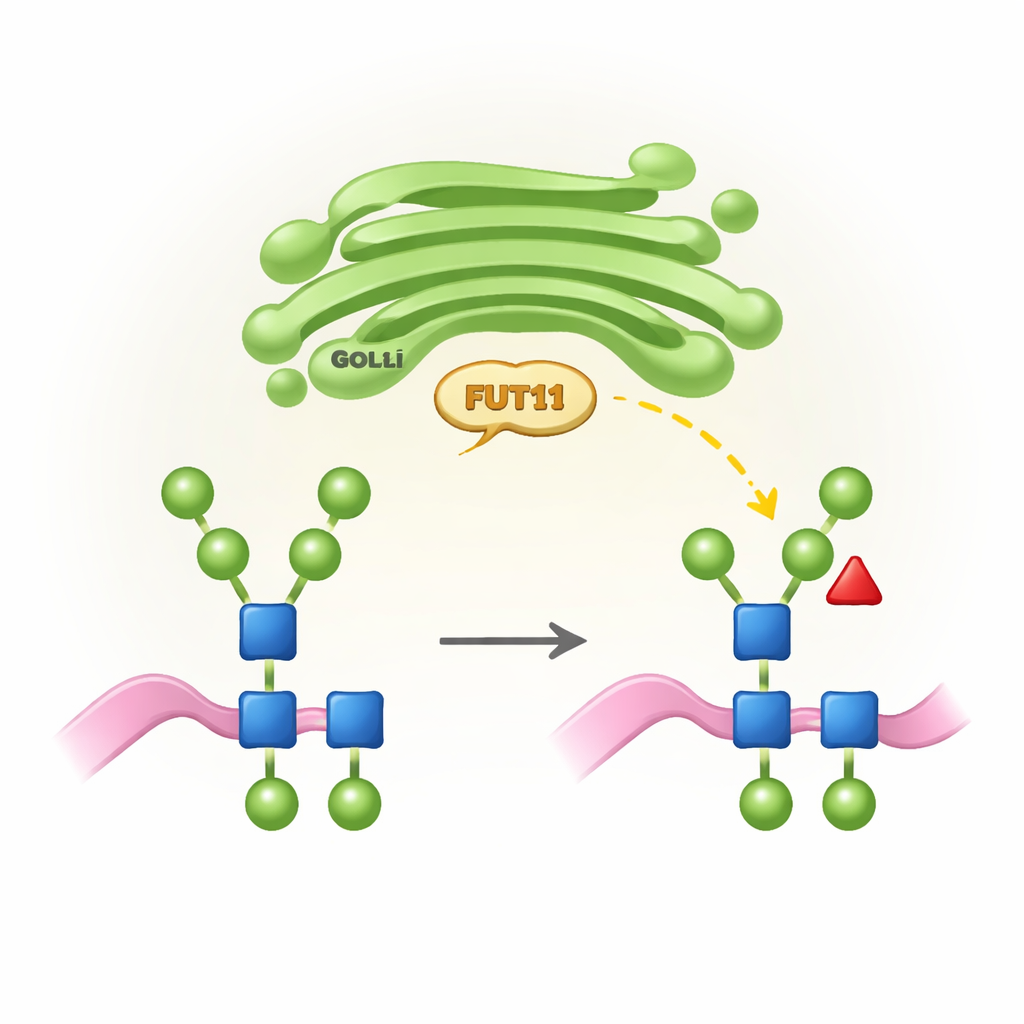
وسومات سكرية خاصة بالنبات ولماذا هي مهمة
تستخدم جميع الكائنات العليا عملية تُدعى إن-تغليكوزلة لإرفاق سلاسل سكرية (إن-غليكانات) بنقاط معينة على البروتينات. في الحيوانات تُعاد تشكيل هذه السلاسل في جهاز جولجي إلى هياكل معقدة غالبًا ما تنتهي بأحماض السياليك وتحمل فوكوزًا أساسيًا في موضع محدد. تتبع النباتات، مع ذلك، «قاعدة تصميم» مختلفة: إن-غليكاناتها عادة تفتقر إلى حمض السياليك لكنها تحمل فوكوزًا أساسيًا في موضع آخر (يُسمى b1,3) بالإضافة إلى سكر زيلوز إضافي. هذه السمات الخاصة بالنبات أساسية للنمو الطبيعي والخصوبة، لكنها قد تُعتبر أجنبية من قبل الجهاز المناعي البشري. FUT11 هو واحد من الإنزيمات النباتية الرئيسية التي يركّب بها هذا الفوكوز الأساسي، ونشاطه يشكّل تطوير النبات وكيفية إدراك البروتينات العلاجية المصنوعة في النباتات داخل أجسامنا.
تعيين أين يمكن لـ FUT11 أن يعمل على فروع السكر المعقدة
لفهم ما يتعرف عليه FUT11، اختبر الباحثون الإنزيم على ميكروأراي يضم 144 بنية إن-غليكان مختلفة. وجدوا أن FUT11 انتقائي إلى حد كبير تجاه أحد فروع شجرة السكر — الذراع المسماة b1,3 — التي يجب أن تحمل وحدة بنائية معينة (N-أسيتيلغلوكوزامين نهائية، أو GlcNAc) حتى يتقدم التفاعل. في الوقت نفسه، كان FUT11 متسامحًا مع زينة أخرى: فهو يعمل حتى عندما يحمل المنوز المركزي زيلوزًا خاصًا بالنبات، وحتى عندما تمت إضافة فوكوز آخر بالفعل في الموضع الحيواني على النواة. الفرع المقابل (b1,6) يكون في الغالب معرضًا للمذيب ويُكوّن تواصلات ضعيفة فقط مع الإنزيم، مما يفسّر لماذا يمكن لـ FUT11 التعامل مع مجموعة واسعة من التعديلات هناك. تساعد تفضيلات الارتباط هذه على تفسير سبب إنتاج النباتات لمجموعة مميزة من هياكل الإن-غليكان وتُظهر كيف يمكن استخدام FUT11 أو تجنّبه عند هندسة خلايا نباتية للتطبيقات الحيوية.
تصميم هيكلي فريد لالتقاط وتوجيه السكريات
باستخدام البنية البلورية بالأشعة السينية، حَلَّ الفريق البنية ثلاثية الأبعاد لـ FUT11 مرتبطًا بمانح السكر (GDP-فوكوز) ومستقبل إن-غليكان. يمتلك الإنزيم هندسة ذات فصين من نوع «GT-B»: فص واحد يحتضن GDP-الفوكوز، بينما يلتف فص المستقبل، الذي يتميّز بتعقيد غير عادي ويشمل تحت-نطاق طرفي-أميني خاص بالنبات، حول الإن-غليكان. هذا التحت-النطاق الإضافي، المرتبط ببقية الإنزيم عبر جسور ديسلفيدية، يرسّخ الجزء المركزي من الغليكان ويساعد في تقديم وحدة GlcNAc التفاعلية نحو المانح. أكدت طفرات في حوامض أمينية رئيسية أدوارها: تغيير حمض جلوتامات واحد (Glu158) ألغى النشاط، بينما أضعف تغيير اثنين من البقايا المجاورة عملية الفوكوزلة بشكل كبير في خلايا بشرية مهندسة. تربط هذه النتائج لقطات بنيوية بوظيفة خلوية حقيقية، مبيّنة بالضبط أي أجزاء البروتين لا غنى عنها للارتباط والتحفيز.
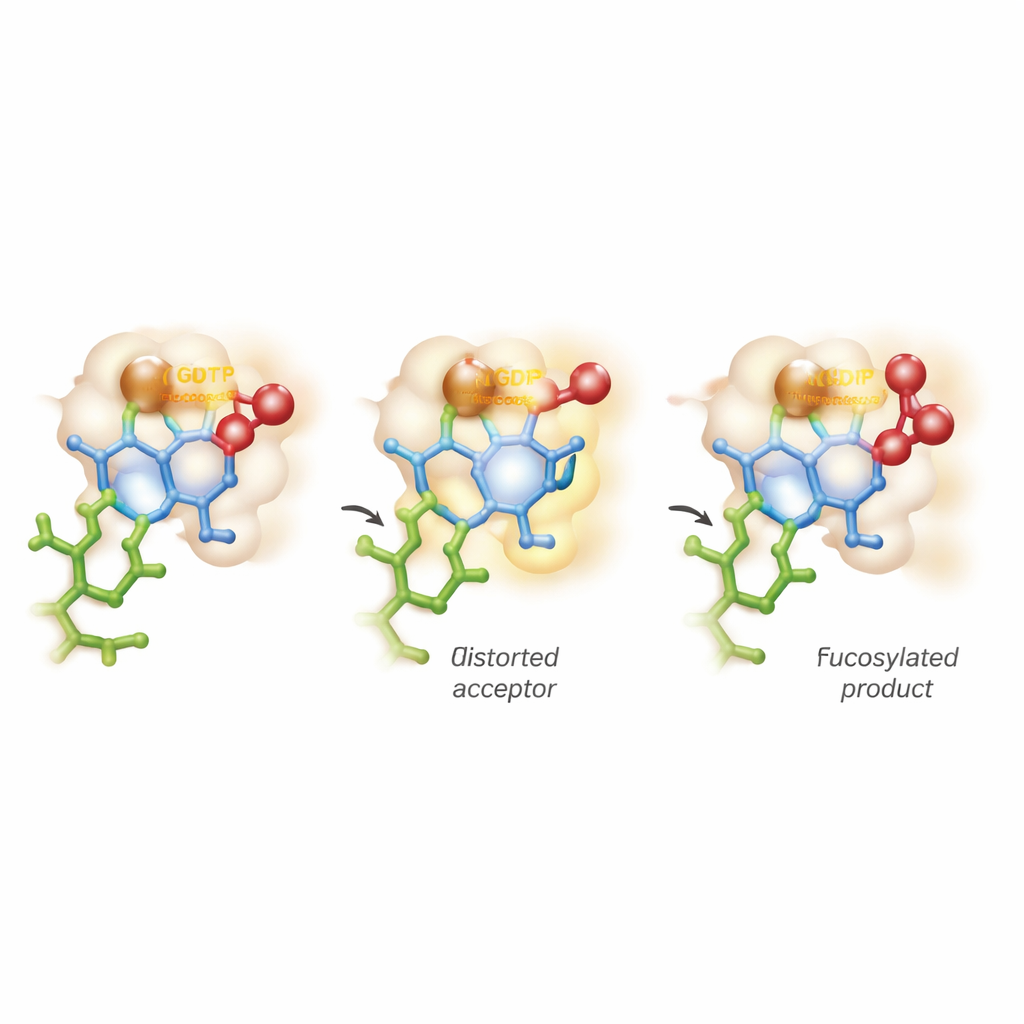
ثني السكر والمشي على خطين تفاعليين
أبرز الرؤى جاءت من محاكيات حاسوبية متقدمة تجمع بين ميكانيكا الكم والديناميكا الجزيئية. تفترض النظريات التقليدية أن السكر المستقبل يحتفظ بشكله المستقر الشبيه بالكرسي بينما يقوم الإنزيم ببساطة بتفعيل المانح. هنا، يتصرف FUT11 بشكل أكثر عدوانية: التفاعلات التي يقودها Glu158 تشوّه مؤقتًا حلقة GlcNAc الداخلية إلى شكل مكسور أقل راحة. في هذا الوضع المشدود، تُسفن مجموعة الهيدروكسيل الحرجة في المحاذاة المثالية لمهاجمة مانح الفوكوز. تكشف الحسابات أنه أثناء انكسار الرابطة الكيميائية إلى GDP يظهر على السكر حالة موجبة الشحنة قصيرة العمر تشبه الأكسوكربونيوم، قبل أن تتكوّن الرابطة الجديدة إلى المستقبل بالكامل. هذا يعني أن التفاعل لا يناسب تمامًا تصنيفات SN1 أو SN2 المدرسية، بل يسير على امتداد طيف، وبأسلوب غير متزامن يقارب الخطوة الواحدة المتتابعة.
المرونة الخفية وصدى التطور
بمقارنة FUT11 مع إنزيم بشري ذي صلة، FUT9، وجد المؤلفون أن الإنزيم النباتي يمكن أن يعدّل أيضًا، وإن كان بضعف، نوعًا مختلفًا من الوحدات السكرية (LacNAc) لصنع بنية تُعرف باسم لويس X. من المحتمل أن هذا النشاط الجانبي ليس مهمًا بيولوجيًا في النباتات، حيث لا يُرى لويس X عادة، لكنه يبرز كيف أن سقالات البروتين المتشابهة يمكن إعادة توظيفها عبر التطور للعمل على سياقات سكرية مختلفة. تشير الدراسة إلى أن FUT11 وأقاربه يشاركون إطارًا معياريًا للتعرف على الإن-غليكانات، مع تعديلات طفيفة تُحوّل التحديد بين نوى نباتية وذُرَيّات حيوانية.
لماذا تهم هذه الخدعة الثني في العلم والطب
تُظهر النتائج مجتمعة أن FUT11 يفعل أكثر من مجرد تقريب شريكين سكريين معًا: إنه يثنّي بنشاط سكر المستقبل إلى وضع تفاعلي ويوجّه الكيمياء عبر وسيط مشحون عابر وفاني. بالنسبة للقارئ العام، يعني هذا أن السكر على البروتين ليس موقع إرساء جامدًا بل مشارك مرن يشكّله الإنزيم وفق حاجته. تساعد هذه الرؤية الجديدة لـ «التحفيز بالامتثال البنيوي» على تفسير كيف تحقق الإنزيمات السرعة والانتقائية معًا وتوفّر مخططًا لإعادة تصميم مسارات التغليكوزلة. عمليًا، فإن معرفة كيفية تعرف FUT11 بالضبط على إن-غليكانات النبات وتعديلها يمكن أن توجه هندسة المحاصيل وأنظمة الإنتاج النباتية لتقليل أنماط السكريات المثيرة للمناعة في العلاجات البشرية، أو لصنع بروتينات غليكوسية مصممة بخصائص بيولوجية محددة.
الاستشهاد: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
الكلمات المفتاحية: تغليكوزلة النبات, فيكوزيلترانسفيراز FUT11, إن-غليكانات, آلية الإنزيم, هندسة الغليكوس