Clear Sky Science · ar
التحليل البروتيومي لبقع إصلاح أضرار الأشعة فوق البنفسجية يكشف عن ناقلات الهيستون ذات وظائف محورية في إصلاح الكروماتين
كيف تشفي خلايانا أضرار ضوء الشمس
في كل مرة تتعرض بشرتنا لأشعة الشمس القوية، تظهر إصابات غير مرئية في حمض نووي الخلايا. إذا تُركت دون إصلاح، يمكن لتلك الندوب الصغيرة أن تتراكم وتساهم في الشيخوخة والسرطان. لكن الحمض النووي ليس عارياً؛ إنه ملفوف بعناية حول بروتينات تسمى هيستونات، مشكلة بنية تُعرف بالكروماتين التي تساعد في تحديد هوية كل خلية. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذا تبعات كبيرة: عندما تُصلح الخلايا أضرار الأشعة فوق البنفسجية في حمضها النووي، كيف تعيد بناء هذا الهيكل المعقد للكروماتين بحيث تُحافظ هوية الخلية بدلاً من أن تُختلط؟
كشف منطقة الإصلاح المخفية
للإجابة عن ذلك، اضطر الباحثون إلى التركيز تحديداً على المواقع في الجينوم التي كان الإصلاح يحدث فيها بنشاط، بدلاً من فحص النواة بأكملها دفعة واحدة. طوروا نهجاً أسموه IPOND-R الذي يوسم كيميائياً مقاطع قصيرة من الحمض النووي المُنتج حديثاً أثناء الإصلاح، وليس أثناء النسخ الطبيعي للجينوم. من خلال سحب هذه «بقع الإصلاح» الموسومة مع كل البروتينات المرتبطة بها، ثم تحديد تلك البروتينات بواسطة طيف كتلي عالي الدقة، أنشأوا فهرساً زمانياً لمن يحضر ومتى أثناء الاستجابة لأضرار الأشعة فوق البنفسجية في خلايا بشرية. منحهم ذلك لقطة غير متحيزة للحقل البروتيني المتخصص الذي يتشكل مباشرةً في مواقع الإصلاح.
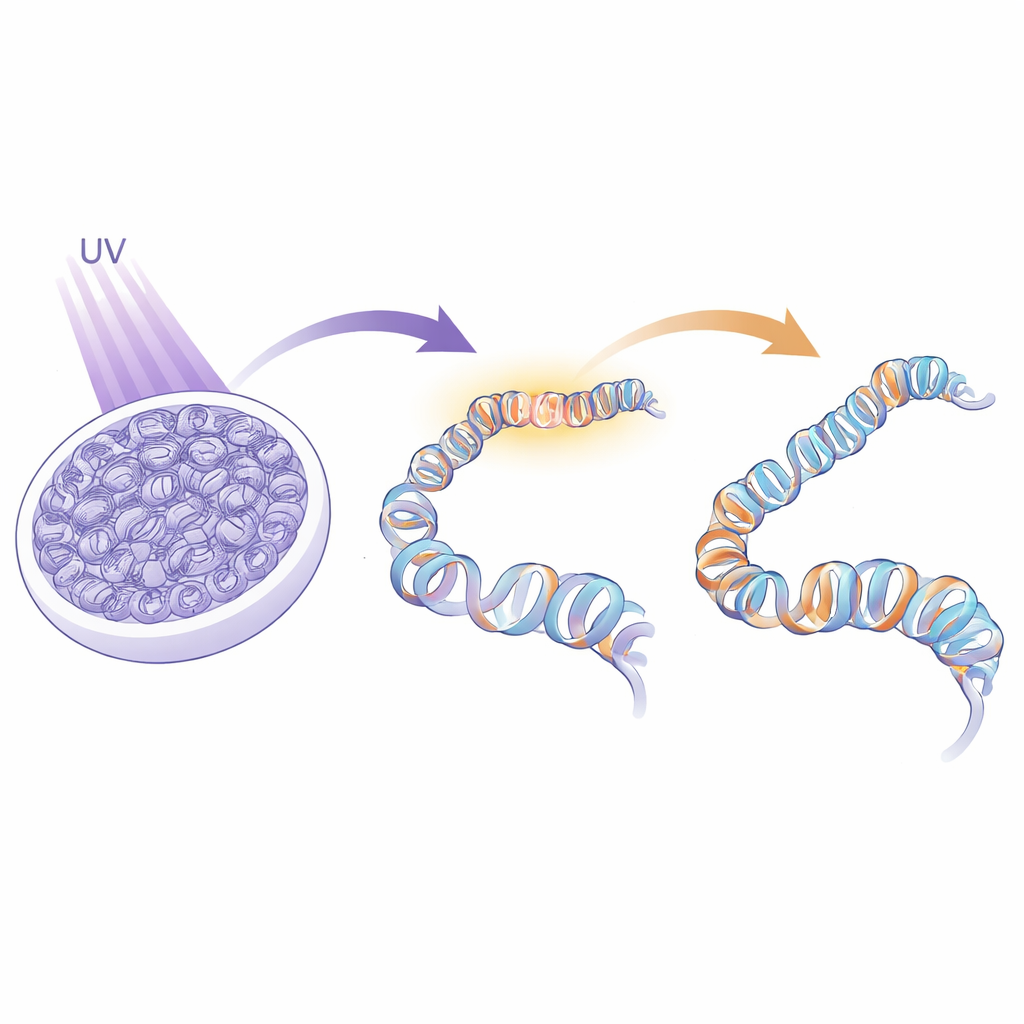
حشود نشطة على سقالة الإصلاح
كشف أسلوب IPOND-R عن مئات البروتينات المعززة على الحمض النووي الخاضع للإصلاح بعد وقت قصير من التعرض للأشعة فوق البنفسجية. كما كان متوقعاً، تواجدت عوامل إصلاح الحمض النووي المعروفة التي تتعرف على الآفات الناتجة عن الأشعة وتستأصلها. لكن مجموعة البيانات امتدت أبعد من ذلك، لتشمل بروتينات مشاركة في تنظيم الجينات، وبنية النواة، وبشكل حاسم تنظيم الكروماتين. كان العديد من هؤلاء الزوار ناقلات هيستون—بروتينات متخصصة ترافق الهيستونات عند دخولها وخروجها من الحمض النووي. أظهر المقارنة بين نقاط زمنية مبكرة ومتأخرة أن معظم هذه الناقلات تظهر بشكل عابر فقط، مما يشير إلى سلسلة متقنة من تفكيك وإعادة تركيب الكروماتين مرتبطة بإحكام بعملية إصلاح الحمض النووي.
موردون جدد ومُعادو تدوير للهيستونات
من بين البروتينات المعززة في بقع الإصلاح، تميزت ناقلتا هيستون: DNAJC9 وMCM2. كانت هذه العوامل معروفة سابقاً بدورانها أساساً قرب شوكات تكرار الحمض النووي، حيث يُنسخ الجينوم، لكنها لم تُربط سابقاً بإصلاح أضرار الأشعة فوق البنفسجية. هنا، تُظهر الفرق أن DNAJC9 هو مورد مركزي لوحدات الهيستون الجديدة (تحديداً أزواج H3–H4) أثناء الإصلاح. باستخدام علامات فلورية تميز الهيستونات الجديدة عن القديمة، وجدوا أن خفض مستويات DNAJC9 يقلل بشكل كبير من قدوم متغيرات الهيستون المصنعة حديثاً إلى مواقع التلف الناتج عن الأشعة فوق البنفسجية، بينما تبقى خطوات إصلاح الحمض النووي الأساسية سليمة. يعمل DNAJC9 في مرتبة تسبق ناقلات الترسيب المعروفة للهيستون مثل CAF-1 وHIRA، مزوداً إياهم بهيستونات جديدة دون تغيير وجودهم في مواقع الضرر.
موازنة لبنات البناء القديمة والجديدة
إصلاح الكروماتين ليس مجرد إدخال أجزاء جديدة. تحمل الهيستونات الأصلية أيضاً علامات كيميائية تخزن معلومات إبيجينية—إشارات تخبر الخلية أي الجينات يجب تشغيلها أو إيقافها. تُظهر الدراسة أن DNAJC9 يساعد أيضاً في إعادة هذه الهيستونات الأبوية بعد أن تبتعد مؤقتاً عن المناطق المتضررة. عندما نُقص DNAJC9، فشلت الهيستونات القديمة في العودة بشكل كامل، وانخفضت كثافة الهيستون الإجمالية في مواقع الإصلاح. ثم اكتشف الباحثون أن DNAJC9 يعمل مع MCM2 لتنسيق هذه الموازنة الحساسة: كلاهما مطلوب لإعادة تدوير الهيستونات القديمة بشكل فعال ولترسيب الجديدة بشكل سليم، حتى في خلايا لا تقوم بتكرار حمضها النووي بنشاط. يشير هذا إلى دور مستقل عن التكرار لـMCM2 ويؤسس شراكة وظيفية بين الناقلين في مواقع الإصلاح.
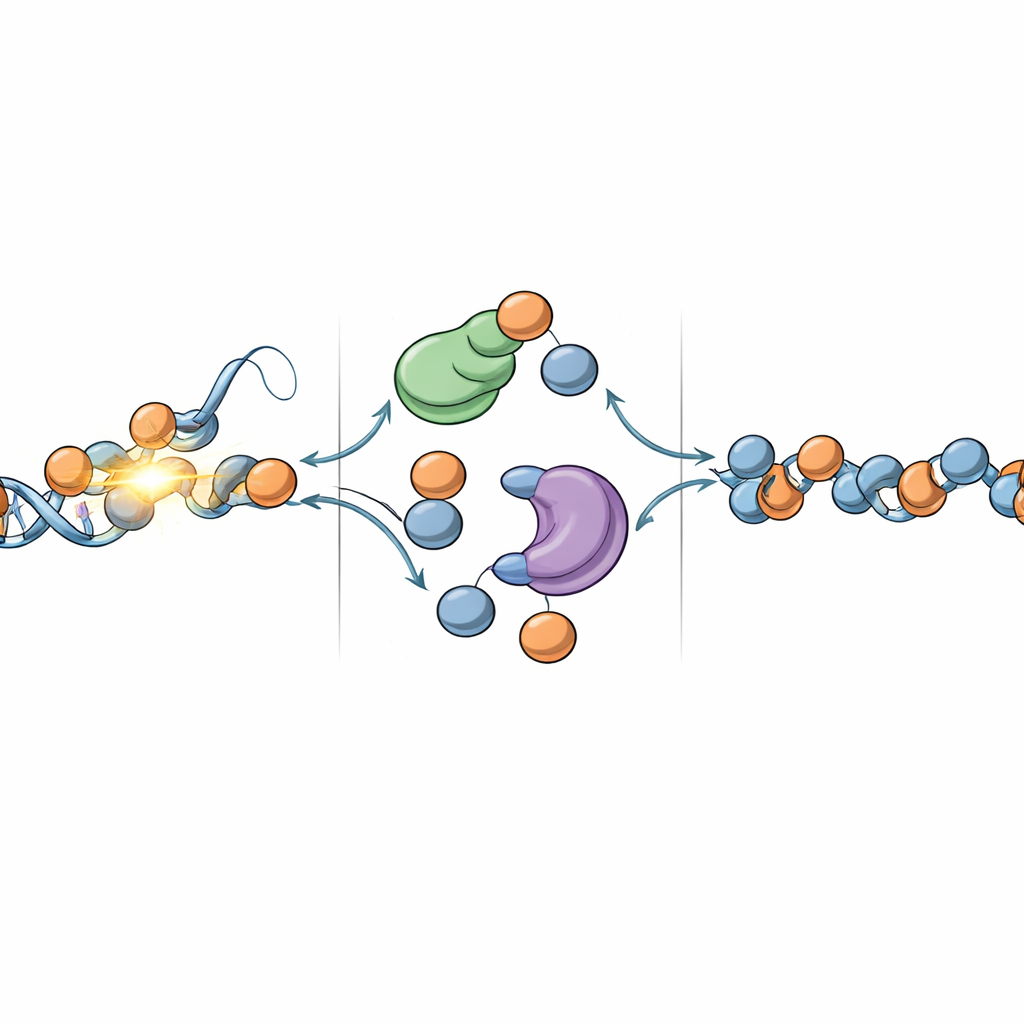
لماذا يهم هذا لهوية الخلايا والمرض
تصوّر هذه العمل عملية إصلاح الكروماتين كعملية ذات وجهين: يُصلح الحمض النووي التالف بينما يُعاد بناء مشهد الهيستونات المحيط باستخدام مزيج من المكونات المعاد استخدامها والموردة حديثاً. يقف DNAJC9 وMCM2 عند مفترق طرق في هذه العملية، منسقين تدفق الهيستونات القديمة والجديدة بحيث تتمكن الخلايا بعد أضرار الأشعة فوق البنفسجية من استعادة ليس فقط الشيفرة الجينية ولكن أيضاً الأنماط الإبيجينية التي تحدد هويتها. وبما أن تحديات مماثلة تنشأ مع أنواع عديدة من تلف الحمض النووي، فإن هذا الإطار يوفر أساساً لفهم كيف تحافظ الخلايا على إبيجينوم مستقر تحت الضغط—مؤسسة مركزية للشيخوخة والسرطان وأمراض أخرى ينحرف فيها تنظيم الكروماتين عن مساره.
الاستشهاد: Plessier, A., Chansard, A., Petit, E. et al. Proteomic profiling of UV damage repair patches uncovers histone chaperones with central functions in chromatin repair. Nat Commun 17, 2127 (2026). https://doi.org/10.1038/s41467-026-68781-x
الكلمات المفتاحية: إصلاح تلف الحمض النووي, الكروماتين, ناقلات الهيستون, الإشعاع فوق البنفسجي, استقرار الإبيجينوم