Clear Sky Science · ar
الأساس البنيوي والآثار المرضية للمجمع الأساسي ثنائي التكافؤ OS9-SEL1L-HRD1 في تحلل البروتين المرتبط بالشبكة الإندوبلازمية
طواقم التنظيف الخلوية تحت المجهر
داخل كل خلية لدينا، تعمل ورشة نشطة تحول التعليمات الجينية إلى بروتينات عاملة. مثل أي مصنع، تحدث أخطاء. عندما تطوى البروتينات بشكل خاطئ، قد تسد النظام وتساهم في الإصابة بالأمراض. يركز هذا البحث على واحدة من آليات الرقابة النوعية الرئيسية في الخلية — مجمع SEL1L‑HRD1 — ليكشف عن بنيته ثلاثية الأبعاد بتفصيل دقيق ويُظهر كيف أن تغييرات جينية دقيقة قد تعطل هذه الآلية وتؤدي ربما إلى أمراض لدى البشر.
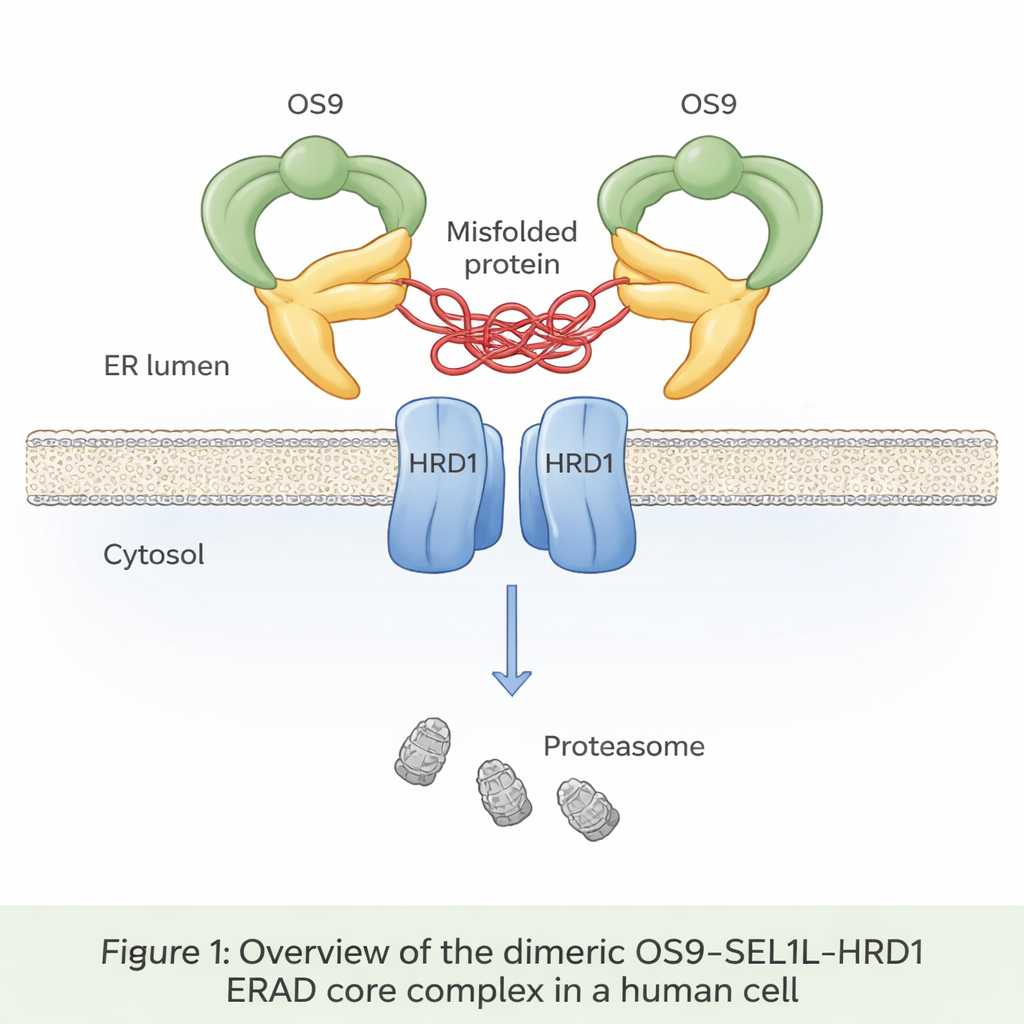
حزام ناقل مخفي داخل الخلية
ما يصل إلى ثلث البروتينات الجديدة تدخل حجرة تسمى الشبكة الإندوبلازمية (ER)، حيث تُطوى وتُفحص. عادةً ما تُعرف البروتينات المطوية خطأ، وتُسحب خارج الشبكة الإندوبلازمية، وتُدمر في عملية تعرف بتحلل البروتين المرتبط بالشبكة الإندوبلازمية (ER‑associated degradation أو ERAD). في قلب أحد مسارات ERAD الرئيسية يوجد ثلاثي من البروتينات: OS9 وSEL1L وHRD1. يعمل OS9 كمستشعر للبروتينات المعيبة الموسومة بالسكريات؛ ويؤدي SEL1L دور السقالة؛ بينما يوسم HRD1 البروتينات المحكوم عليها بالهلاك بعلامات اليوبكويتين الصغيرة التي تؤشر لتدميرها بواسطة وحدات التخلص من النفايات الخلوية، البروتيزومات. وحتى الآن، لم يرَ أحد بالتفصيل الذري كيف تتكامل هذه القطع الثلاث في الخلايا البشرية.
كشف شكل الآلية الأساسية
استخدم الباحثون التصوير بالمجهر الإلكتروني بالتبريد (cryo‑EM)، وهي تقنية تصوّر الجزيئات المجمدة فجأة بدقة تقارب الذرية، لتصوير مجمع OS9‑SEL1L‑HRD1 المُنقَّى من خلايا بشرية. اكتشفوا أنه يتكوّن على شكل ثنائي — بمعنى نسختين متطابقتين ملتحمتين معًا — بدل البقاء كوحدات فردية. على جانب لمعة الشبكة الإندوبلازمية (الجهة الداخلية للشبكة)، يجتمع جزيئان من OS9 وجزيئان من SEL1L لتشكيل حلقة شبيهة بمخلب السلطعون ذات فتحة مركزية تبدو مُصمَّمة للإمساك بالبروتينات المطوية خطأ. داخل الغشاء نفسه، يتزاوجان جزيئان من HRD1 لتكوّن قناة مشتركة. يضع هذا الترتيب "المخلب" مباشرة فوق بوابة HRD1، مكوّناً مسارًا متصلاً يسمح للبروتينات المعيبة بالانتقال من لمعة الشبكة، عبر الغشاء، ونحو التحلل في السيتوبلازم.
كيف تكسر تغييرات صغيرة نظامًا كبيرًا
بما أن طفرات في SEL1L وHRD1 وُجدت لدى مرضى يعانون اضطرابات نمائية عصبية شديدة واضطرابات أخرى، قام الفريق بترسيم عدة متغيرات مرتبطة بالمرض على بنيتهم واختبر كيفية سلوكها في الخلايا. تقع طفراتا SEL1L، G585D وS658P، عند نقاط التماس مع OS9 وHRD1 على التوالي. في تجارب خلوية، ألغت G585D تقريبًا قدرة SEL1L على الارتباط بـOS9، بينما أضعفت S658P بشكل كبير تماسكه مع HRD1؛ ومزجهما معًا أدى أساسًا إلى تفكك المجمع الأساسي، مع بقاء الشركاء الآخرين دون مساس. نتيجة لذلك، كافحت الخلايا لوضع العلامات والتخلص من مُسبق هرمون مطوي خطأ، مما سمح لبروتينات معيبة بالتراكم.
طفرة مرضية في قناة الغشاء
تُظهر البنية أيضًا أن القطعة العابرة للغشاء رقم 3 في HRD1 هي واجهة الاتصال الرئيسية حيث يلتقي جزيئان من HRD1 لتشكيل القناة. صنع الباحثون مقابض من السيستئين في مواقع محددة واستخدموا الربط الكيميائي لتأكيد أن هذه المناطق تقترب من بعضها في الخلايا الحية، مما يثبت أن HRD1 يتزاوج فعليًا في الكائن الحي. عندما عطّلوا بقاعدة واحدة عالية الحفظ (T93) في هذه الواجهة، انهار الثنائي وتراجع نشاط ERAD، رغم أن المجمع ظل يتجمع مع OS9 وSEL1L. ثم فحصوا متغيرًا مرضيًا حديث الاكتشاف، HRD1 A91D، الموجود لدى طفل يعاني من مشاكل قلبية ورئوية. هذا التغيير، الموجود أيضًا في واجهة الثنائي، خفض تزواج HRD1 بنحو النصف وأضعف بشكل كبير التخلص من البروتينات المطوية خطأ، مرة أخرى دون التأثير على الارتباط الكلي للشركاء.
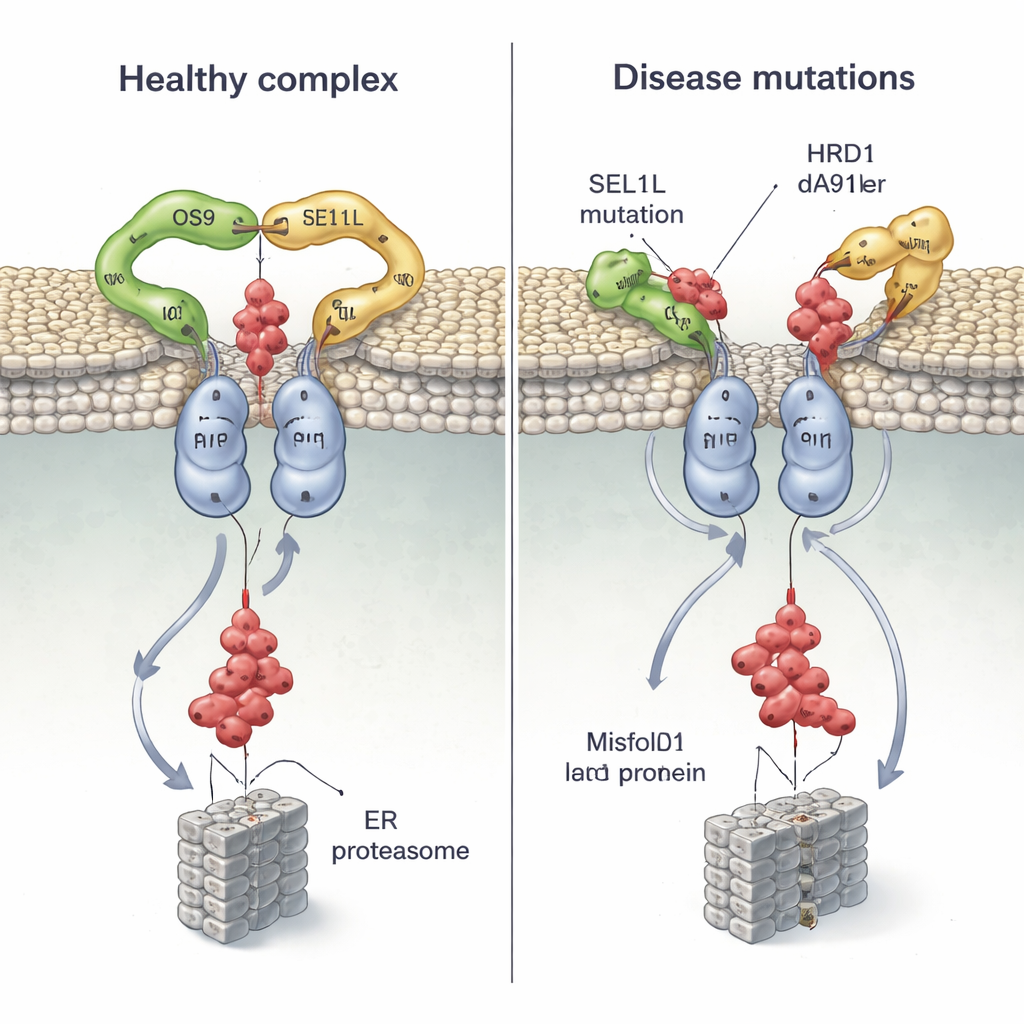
رؤية جديدة لمراقبة جودة البروتين والمرض
من خلال دمج علم البنية مع اختبارات خلوية، تُظهر هذه الدراسة أن مجمع OS9‑SEL1L‑HRD1 يعمل كآلة مزدوجة ثنائية: ممسك شبيه بالمخلب مرتبط بقناة مشتركة تنقل البروتينات المعيبة خارج الشبكة الإندوبلازمية. الطفرات التي تضعف قبضة المخلب أو تزعزع استقرار زوج HRD1 لا تُعدّل الكفاءة فحسب — بل قد تسد النظام فعليًا، مما يسمح بتراكم البروتينات المتضررة والمساهمة في الأمراض البشرية. للقراء غير المتخصصين، الرسالة الأساسية هي أن حتى التغيير بحرف واحد في شفرتنا الجينية يمكن أن يشوّه شكل آلات خلوية أساسية بشكل طفيف، مع عواقب بعيدة المدى على تطور الدماغ والمناعة ووظائف الأعضاء.
الاستشهاد: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
الكلمات المفتاحية: مراقبة جودة البروتين, الشبكة الإندوبلازمية, ERAD, مجمع SEL1L-HRD1, طَيّ البروتينات بشكل خاطئ