Clear Sky Science · ar
نانوإنزيم محاكي للجرازيم B لتطبيقات مضادة للسرطان مستهدفة بواسطة الحويصلات النانوية
إعادة ابتكار قاتلات الجسم للسرطان
جهاز المناعة لدينا يمتلك خلايا متخصصة يمكنها تتبع الخلايا السرطانية وقتلها، لكن في العديد من الأورام الصلبة تواجه هذه الخلايا صعوبة في الوصول إلى الداخل، أو تتعب سريعًا، أو تهاجم الأهداف الخاطئة. تصف هذه الدراسة نظامًا اصطناعيًا كاملًا على مقياس النانومتر يحاكي أحد أقوى أسلحة جهاز المناعة ويُوصل هذا السلاح مباشرة إلى داخل خلايا الورم. أهمية العمل تكمن في أنه يشير إلى علاجات للسرطان تتصرف مثل الخلايا المناعية الحية، لكنها مصنوعة من مواد ثابتة وقابلة للتحكم بدلاً من خلايا بشرية هشة.
تحويل قاتل طبيعي إلى نموذج تصميم
خلايا T السامة، نوع من خلايا الدم البيضاء، تقتل الخلايا الخطرة باستخدام إنزيم يسمى جرازيم B. عندما تتعرف على هدف، تُحدث ثقوبًا صغيرة في غشاءه وتحقن الجرازيم B، الذي يُفعّل برامج الانتحار داخل الخلية. تستند هذه الاستراتيجية إلى علاجات حديثة مثل خلايا CAR‑T، القادرة على شفاء بعض سرطانات الدم. ومع ذلك، في الأورام الصلبة غالبًا ما تفشل خلايا CAR‑T لأنها لا تستطيع الوصول إلى كل مناطق الورم أو تصبح مستنفدة أو تصيب أنسجة سليمة عن طريق الخطأ. تساءل الباحثون عما إذا كان بإمكانهم بناء جهاز غير حي على مقياس النانو يعيد إنتاج الوظيفة الأساسية للجرازيم B — تفعيل آلية الانتحار داخل الخلية — دون الاعتماد على خلايا T الحية.
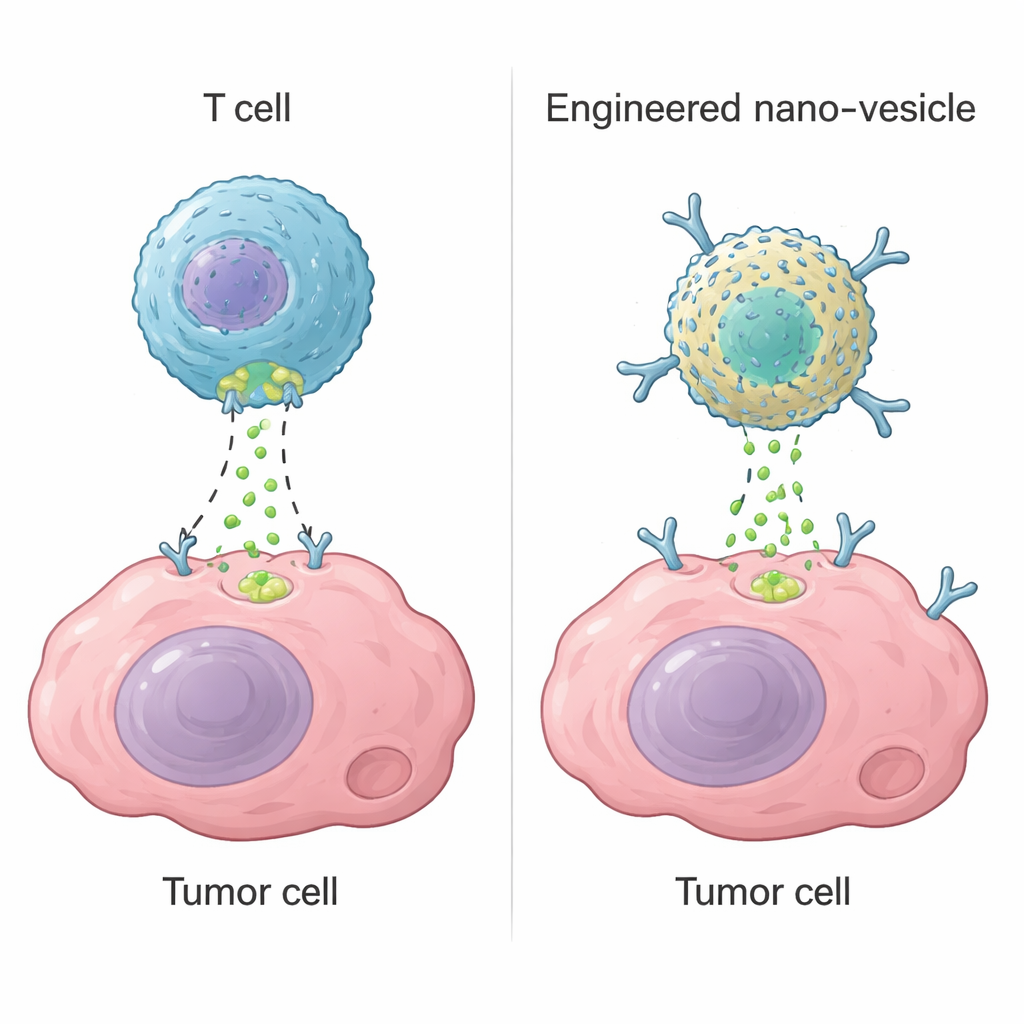
تصميم إنزيم اصطناعي دقيق
بدأ الفريق من الفيريتين، بروتين طبيعي يشكل قفصًا نانويًا مجوفًا ويسهل إنتاجه بكميات كبيرة. بربط أيونات البالاديوم بالفيريتين البشري أنشأوا «نانوإنزيم» يتصرف كإنزيم حقيقي. كشفت دراسات بنيوية دقيقة أن ذرتَي بالاديوم تستقران في جيب محدد على سطح البروتين، مثبتتين بواسطة أحماض أمينية تحتوي على الكبريت والنيتروجين وجزيئات ماء. يعمل هذا المركز المعدني الثنائي كموضع قطع اصطناعي يتعرف على نفس التسلسل القصير الذي يستهدفه جرازيم B على هدف حاسم يُعرف باسم كاسبيز‑3. في اختبارات مخبرية، قطع النانوإنزيم كاسبيز‑3 بكفاءة عند الموضع الصحيح، مفعلًا إياه، بينما تجاهل البروتينات المماثلة عن قرب. كان الإنزيم الاصطناعي أقل كفاءة قليلًا من جرازيم B الطبيعي لكنه كان أكثر ثباتًا عبر نطاق واسع من درجات الحرارة والحموضة.
تهريب النانوإنزيم إلى داخل خلايا الورم
تعمل الإنزيمات مثل جرازيم B فقط إذا وصلت إلى داخل خلايا الورم. لتحقيق ذلك، عبأ الباحثون نانوإنزيم البالاديوم‑فيريتين داخل حويصلات نانوية دهنية — فقاعات صغيرة وطرية مصنوعة من جزيئات شبيهة بالدهون. ثم غلفوا هذه الحويصلات بشظايا من الأجسام المضادة تتعرف على HER2، البروتين الذي يُفرط في التعبير عنه في كثير من خلايا سرطان الثدي والمثانة. عندما تلتقي هذه الحويصلات المموهة بخلايا غنية بـ HER2، ترتبط بها بإحكام وتندمج مع غشاء الخلية، مما يسمح لشحنة النانوإنزيم بالانزلاق مباشرة إلى السيتوبلازم بدلاً من أن تُحتجز وتُهضم في محطات إعادة تدوير خلوية. أظهرت الميكروسكوبات وجود الحويصلات عند سطح الخلية بينما ينتشر النانوإنزيم إلى الداخل، مهيئًا حالة لتدمير مبرمج من داخل الخلية.
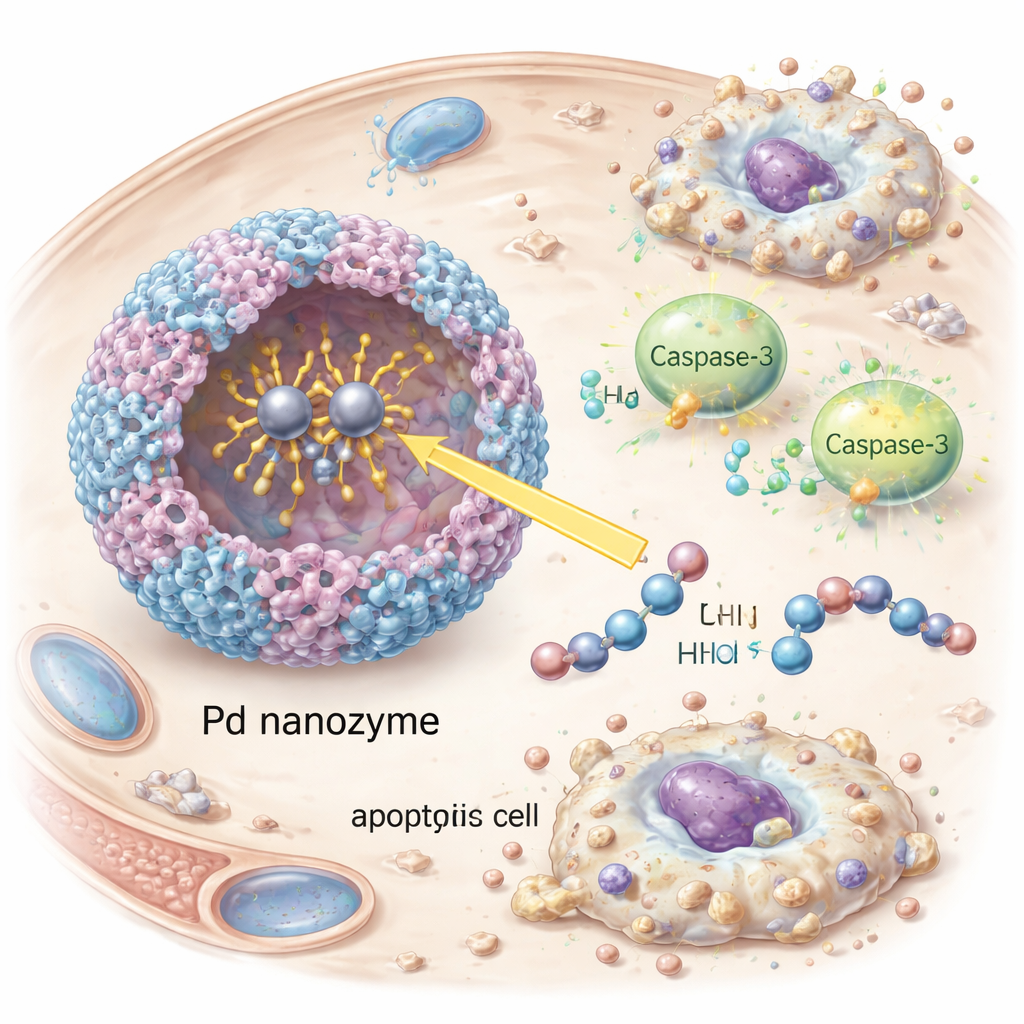
تحفيز انتحار الخلايا السرطانية بدقة
عند دخولها خلايا السرطان، فعّل النانوإنزيم كاسبيز‑3، القاضي المركزي للموت الخلوي المبرمج. لوحظ ظهور كاسبيز‑3 المنشط وهدفه التالي PARP، إضافة إلى علامات واضحة على الاستماتة (الابوبتوسيس)— تقلص الخلايا وتجزئها— في خلايا ورمية مستزرعة موجبة لـ HER2. أدى إسكات كاسبيز‑3 بواسطة تدخل RNA إلى تقليل كبير في موت الخلايا، مما أكد أن التأثير كان يعتمد على هذا المسار وليس على تلف غير نوعي. في فئران حاملة لأورام موجبة لـ HER2، دارت الحويصلات المزينة بالأجسام المضادة لفترة أطول في مجرى الدم، وتراكمت بقوة أكبر في الأورام، وأبطأت نمو الورم بفعالية أكبر من الحويصلات التي تفتقر إما إلى الأجسام المضادة المستهدفة أو إلى شحنة النانوإنزيم. والأهم من ذلك، لم تظهر على الحيوانات المعالجة خسارة وزن واضحة أو اضطرابات دموية أو تلف في أنسجة الأعضاء الرئيسية، مما يوحي بملف سلامة مشجع في هذه الاختبارات المبكرة.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن الباحثين بنوا جهازًا صغيرًا وغير حي يتصرف مثل جزء مهم من آلية جهاز المناعة في قتل السرطان. بدلًا من تعديل خلايا T الحية، صمموا نانوإنزيم ثابتًا يفعّل نفس مفتاح الانتحار داخل خلايا الورم وغلفوه بغلاف توصيل ذكي يصوب نحو سرطانات معينة. رغم أن هناك الكثير من العمل قبل الاستخدام البشري، فإن هذا النهج يقدم منصة مرنة: من حيث المبدأ، يمكن استبدال طلاء الأجسام المضادة لاستهداف علامات ورمية مختلفة، ويمكن تحسين الإنزيم الاصطناعي أكثر. تظهر الدراسة مسارًا واعدًا نحو مناعة علاجية خالية من الخلايا، حيث تُستخدم مواد نانوية مصممة بعناية، بدلًا من خلايا مناعية حية، لتعقب وتدمير الأورام الصلبة.
الاستشهاد: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
الكلمات المفتاحية: نانوطب السرطان, المناعة العلاجية, جرازيم B, نانوإنزيم, الأورام الموجبة لـ HER2