Clear Sky Science · ar
الكيمياء الحيوية الأرثوغونالية المنشّطة بأنواع الأكسجين التفاعلية في الأنظمة الحية شغّلتها ديهيدروتيترازينات محتجزة بالبورونات
تحويل إجهاد الخلايا إلى مفتاح دقيق
تتصف العديد من الأمراض، من السرطان إلى مشاكل القلب، بخلايا تحت ضغط أكسدي تنتج مستويات مرتفعة من أنواع الأكسجين التفاعلية مثل بيروكسيد الهيدروجين. تُظهر هذه الدراسة كيف يمكن للكيميائيين أن يستغلوا هذا الإجهاد نفسه كمفتاح مدمج لتشغيل علاجات قوية فقط حيثما تكون هناك حاجة إليها. من خلال تصميم مكونات دوائية تتفاعل فقط في هذه البيئات المتأملة، يسعى الباحثون إلى قتل خلايا الورم أو تدمير البروتينات الضارة مع الحفاظ على الأنسجة السليمة.
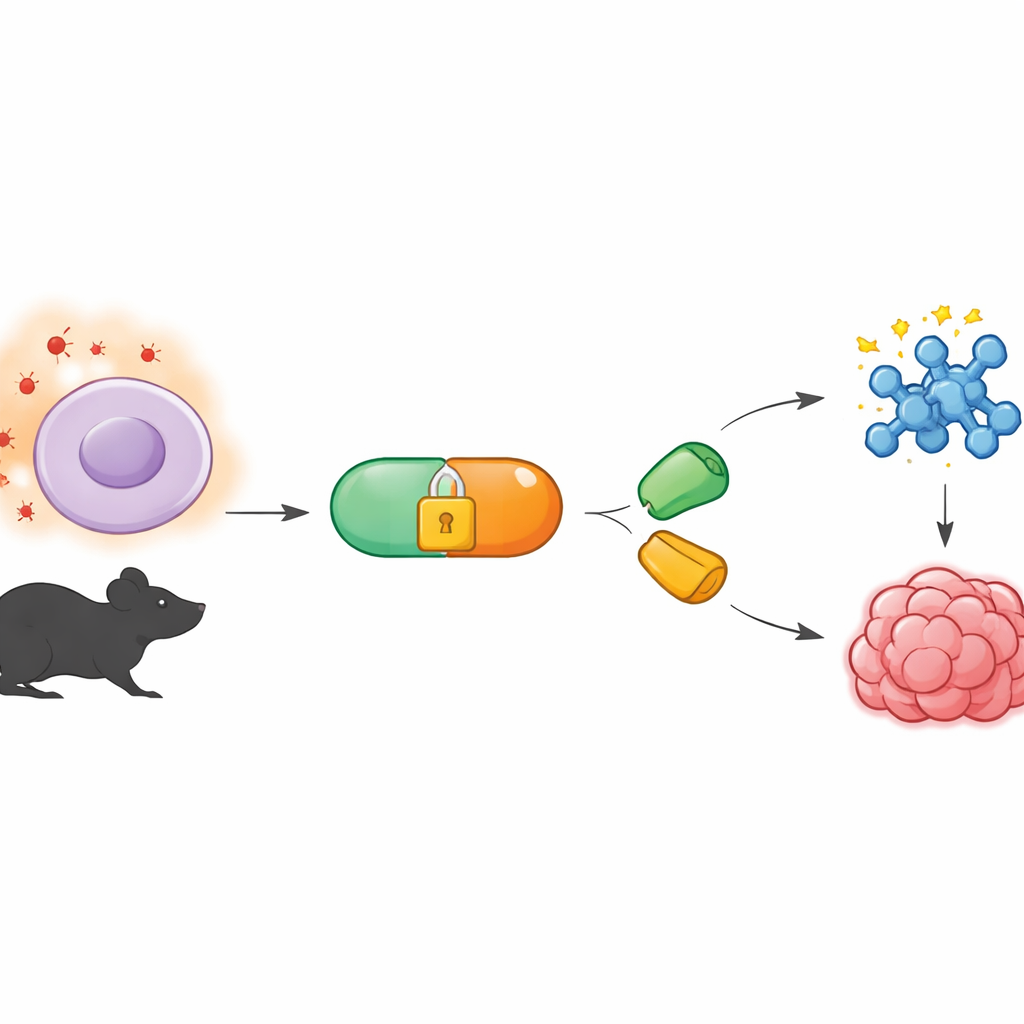
أداة كيميائية تعمل بهدوء في الخلفية
تبني العمل على مجال يُسمى الكيمياء الحيوية الأرثوغونالية، التي تطور تفاعلات يمكن أن تجري داخل الكائنات الحية دون تعطيل البيولوجيا الطبيعية. إصدار شائع يستخدم أزواجاً خاصة من الجزيئات التي تتصل بسرعة كقطع أحجية، حتى في البيئة المزدحمة داخل الخلية. أحد الشركاء، المسمى التيترازين، يتفاعل بسرعة مع شريك حلقي مطابق يُعرف بالديينوفيل. حتى الآن، كان العديد من هذه التفاعلات يتم التحكم فيه عن طريق التعرض للضوء أو إضافة إنزيمات. أراد المؤلفون بدلاً من ذلك نظاماً يستمع إلى إشارات الجسم الكيميائية نفسها — وبالتحديد مستويات أنواع الأكسجين التفاعلية المرتفعة غير المعتادة الموجودة في الأورام والأنسجة المريضة الأخرى.
بناء زناد كيميائي حساس لأنواع الأكسجين
لتحقيق ذلك، أنشأ الفريق سوابق للتيترازين أسماها BTz، وهي مُحتجَزة كيميائياً بحيث تظل خاملة في الأنسجة الطبيعية. البِزِة تتكوّن من مجموعة بورونات مرتبطة بشكل مختزل من التيترازين. عندما يكون بيروكسيد الهيدروجين نادراً، يكون BTz مستقراً في الماء وفي مزروعات الخلايا لساعات عديدة. لكن عندما يتوفر بيروكسيد الهيدروجين بوفرة — بمستويات مماثلة لتلك المقاسة في الأورام — تُؤكسد مجموعة البورونات وتتفكك عبر سلسلة تدمير ذاتي، كاشفةً التيترازين الفعّال. في تجارب أنابيب الاختبار، أدى رفع تراكيز بيروكسيد الهيدروجين خطوة بخطوة إلى زيادة مطابقة في كمية التيترازين النشط المولّد، مؤكداً أن التفاعل انتقائي ويعتمد بقوة على الجرعة.
استخدام إجهاد الخلية لتدمير بروتين يحرّك السرطان
استخدم الباحثون أولاً مفتاحهم للتحكم في استراتيجية دوائية حديثة تسمى التحلل الهدف للبروتين. ربطوا BTz بالثاليدومايد، جزيء صغير يمكنه تجنيد مجمع إنزيمي مسؤول عن وسم البروتينات للتخلص منها. في خلايا السرطان، ظل هذا المركب BTz–ثاليدومايد خاملاً حتى ارتفعت مستويات بيروكسيد الهيدروجين، وفي تلك اللحظة انفتحت الحِجْرة لتشكّل التيترازين النشط. تفاعل هذا التيترازين بعد ذلك مع شريك مطابق مربوط إلى دواء يربط BRD4، مكوّناً «تشيميرا» أكبر تجذب بروتين BRD4 المرتبط بالسرطان إلى آلية النفايات داخل الخلية. في خطوط خلايا سرطان الرئة وعنق الرحم، انخفضت مستويات BRD4 بشكل حاد فقط عندما كانت كل الأجزاء موجودة وبوجود بيروكسيد الهيدروجين؛ إذ منعت حصارة أنواع الأكسجين التفاعلية التحلل، مما يبرز أن العملية مفعلّة فعلاً بالإجهاد.
توصيل دواء سام فقط حيثما يلزم
بعد ذلك،حوّل الفريق نفس الكيمياء إلى نظام توصيل دقيق للدوكسوروبيسين، وهو علاج كيميائي فعال لكنه ضار للقلب. ربطوا الدوكسوروبيسين بشريك حلقي متوتر بحيث يُحجز في شكل دواء سابق غير نشط. عندما واجه هذا الدواء السابق BTz في بيئة غنية ببيروكسيد الهيدروجين، تفاعل التيترازين المتكون حديثاً مع الحلقة في عملية «انقر للإطلاق»، فتتلاقى القطع وتطلق دوكسوروبيسين الحر. في خلايا سرطان القولون المزروعة في أطباق، قتل هذا النظام ذي الخطوتين الخلايا بكفاءة تقارب الدواء الحر، لكن فقط عند وجود بيروكسيد الهيدروجين؛ وبدونه بقيت الخلايا إلى حد كبير سالمة. كان دواء سابق أبسط حساس لبيروكسيد الهيدروجين أقل فعالية وأقل انتقائية في هذه الاختبارات، مما يبرز ميزة فصل الاستشعار والإطلاق إلى خطوتين منسقتين.
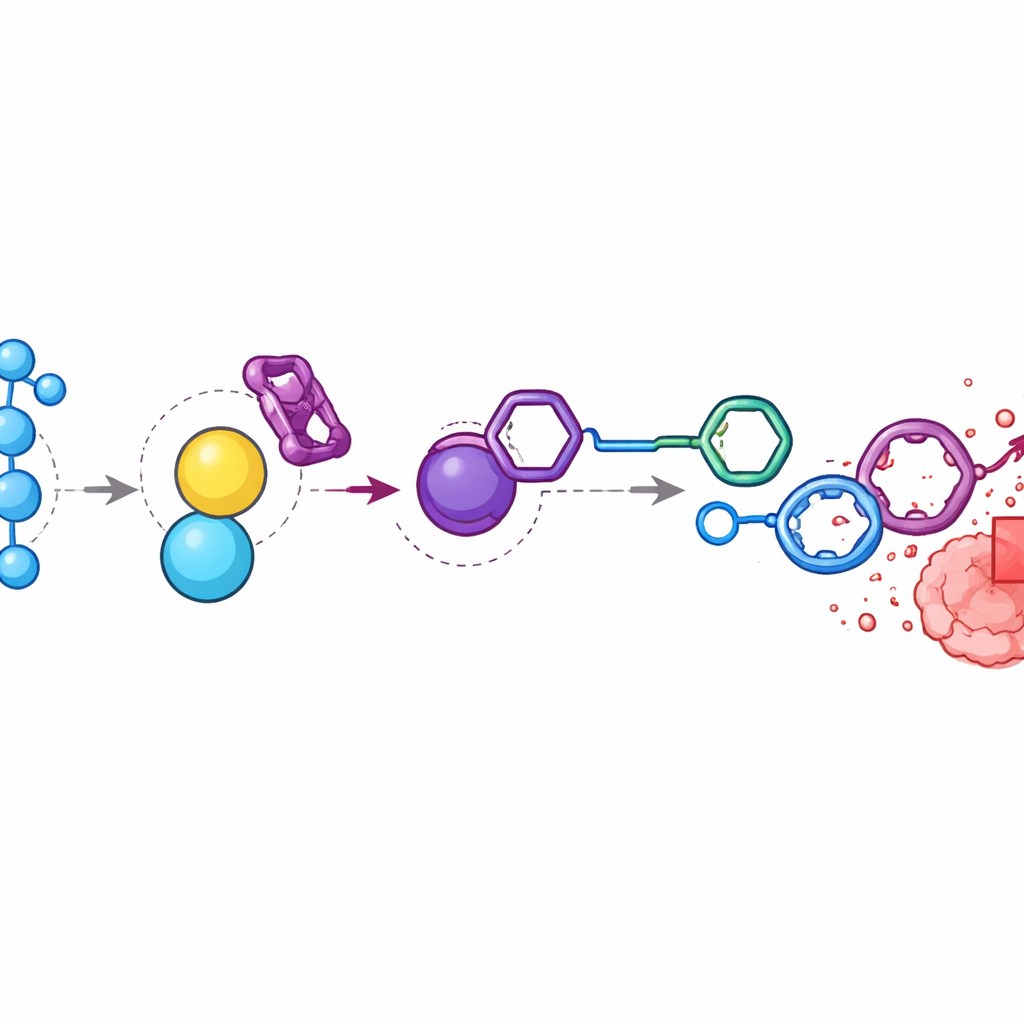
تركيز العلاج الكيميائي داخل الأورام
في فئران تحمل أورام قولون، وجد الباحثون أن مستويات بيروكسيد الهيدروجين في الأورام كانت أعلى بنحو تسع مرّات مقارنة بالعضلات المحيطة. حقنوا الدواء السابق للدوكسوروبيسين وBTz بتسلسل زماني بحيث يتراكم كلاهما قرب الورم. أظهر التحليل الكيميائي أن المكونات اختفت إلى حد كبير من مجرى الدم والأعضاء لكنها ولّدت مستويات عالية من الدوكسوروبيسين الحر داخل الأورام. بالمقارنة مع الحيوانات التي أعطيت دوكسوروبيسين القياسي، أظهرت الحيوانات المعالجة بالنظام المفعل تضخّماً مماثلاً أو أفضل للأورام ولكنها حافظت على وزن جسم مستقر وتجنّبت السُّمّية الشديدة المرصودة عند جرعات أعلى من الدواء. عندما ألغى الفريق إشارة بيروكسيد الهيدروجين بحقن الكاتالاز، إنزيم يزيل بيروكسيد الهيدروجين، تقلّص إطلاق الدواء وتراكمه الانتقائي في الورم بشكل كبير، مؤكداً أن الإجهاد التأكسدي في موقع الورم هو المحرّك الرئيسي.
من إشارة الإجهاد إلى العلاج الدقيق
تجتمع النتائج لتُظهِر منصة كيميائية متعددة الاستخدامات تحوّل سمة مميزة للمرض — فائض أنواع الأكسجين التفاعلية — إلى مقبض تحكم دقيق لتفاعلات قوية داخل الأنظمة الحية. من خلال إبقاء مقبض التيترازين التفاعلي مقفلاً حتى يلتقي ببيروكسيد الهيدروجين، يتيح النهج للباحثين بناء علاجات معقّدة داخل الجسم فقط حيثما هناك حاجة إليها، سواء لتفكيك بروتين محفز للسرطان أو لإطلاق دواء سام داخل الورم. وبما أن الإجهاد التأكسدي يلعب أيضاً أدواراً في الشيخوخة والالتهاب والسكري واضطرابات تنكسية عصبية، يمكن تكييف تفاعلات مستجيبة للإجهاد مماثلة في نهاية المطاف للعديد من الحالات التي تكون فيها الدقة والسلامة في غاية الأهمية.
الاستشهاد: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
الكلمات المفتاحية: الكيمياء الحيوية الأرثوغونالية, أنواع الأكسجين التفاعلية, رابطة التيترازين, توصيل الدواء المستهدف, PROTAC