Clear Sky Science · ar
تجميعات جزيئية دورية لتصوير جهاز غولجي وتعطيله
تحويل مركز الشحن في الخلية إلى هدف استراتيجي
في داخل كل خلية حيوانية يوجد جهاز غولجي، محطة فرز مشغولة تُنهِي وتعبّئ وتشحن آلاف البروتينات والدهون. تعتمد العديد من خلايا السرطان اعتمادًا كبيرًا على هذا المركز لتعديل إشارات النمو وإفراز عوامل تشكّل محيطها. يقدم هذا البحث جزيئات مصممة دقيقة تتوجه نحو غولجي، وتضيئه لتصوير سريع، وعند إعادة تصميمها يمكن أن تعطل عملياته بشكل اختياري لتضعف الخلايا السرطانية مع المحافظة على بعض الخلايا السليمة.
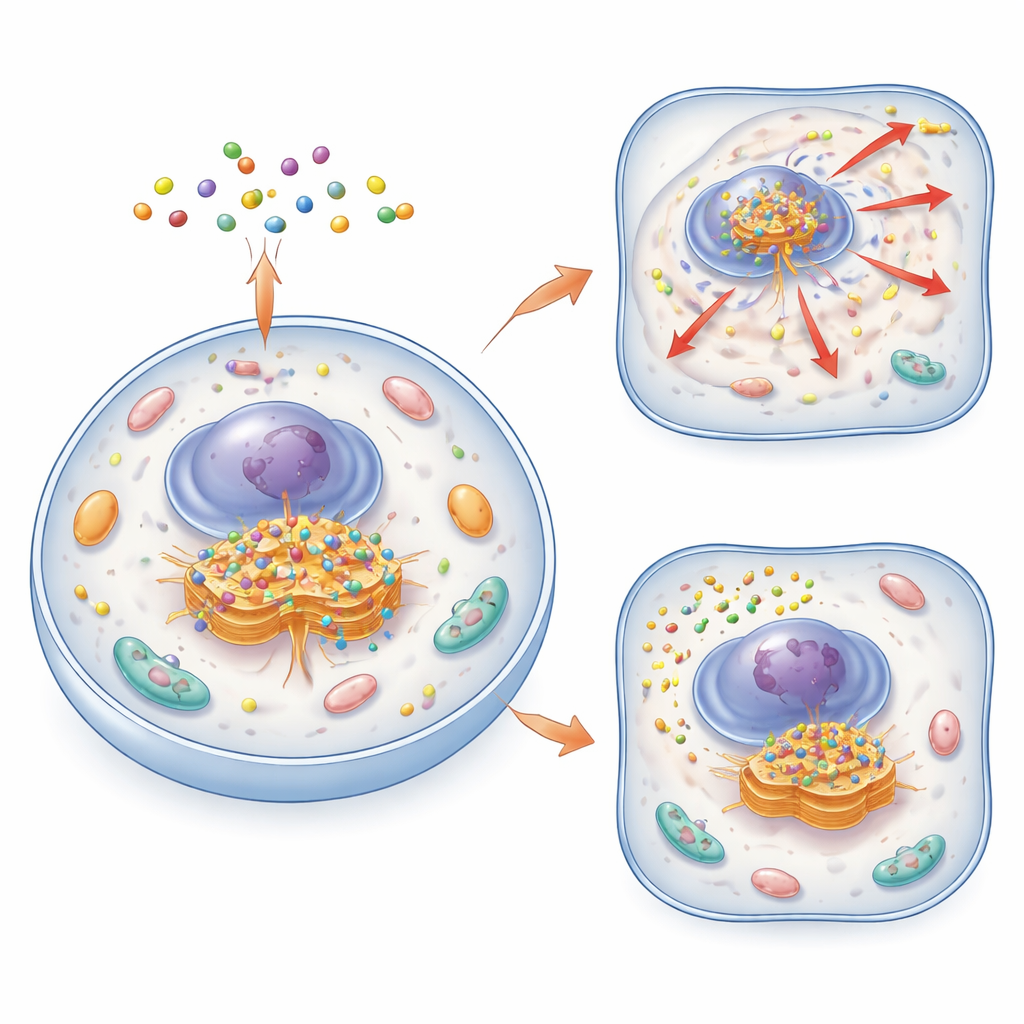
طريقة جديدة لاكتشاف ومراقبة الغولجي
ابتكر الباحثون عائلة من الجزيئات الصغيرة والذكية تُدعى التجميعات الجزيئية الدورية، أو CyMA. تُبنى هذه الجزيئات من ببتيدات قصيرة يمكنها اختراق أغشية الخلايا والتلاصق معًا لتشكيل تجمعات دقيقة. في نسختها الخاصة بالتصوير (CyMA‑i)، تحمل الببتيدات صبغة فلورية تتوهّج بشدة عند تجمع الجزيئات. بمجرد دخولها الخلية، تقصّ إنزيمات غطاءً واقيًا من سلف CyMA، كاشفةً مقبضًا تفاعليًا. ثم تلحق إنزيمات مقيمة في الغولجي سلسلة دهنية بهذا المقبض، مما يجعل الجزيئات أكثر لزوجة وميلًا للتجمع تحديدًا عند الغولجي. لأن هذه العملية سريعة وتستغل آلية خلوية طبيعية، يستطيع الباحثون رسم شكل الغولجي في خلايا حية خلال دقائق وبتركيزات منخفضة جدًا من المجس.
دورة عبثية تثبت الجزيئات على الغولجي
لا تقتصر CyMA على كونها وسمًا؛ بل صممت لتشارك في «دورة عبثية» عند الغولجي. مجموعة من الإنزيمات تضيف سلاسل دهنية إلى الببتيد، في حين تزيلها مجموعة أخرى. ومع تكرار الخلية لإضافة وإزالة هذه السلاسل، تستمر الببتيدات المعدلة في التجمع والانفصال في مكانها. هذا التبادل المستمر يحبس نواة صلبة من التجميعات على أغشية الغولجي، بينما تظل الجزيئات الفردية تمرّ عبر الدورة. على الخلية أن تستمر في إنفاق وحدات البناء الدهنية الخاصة بها للحفاظ على هذا الحلقة، مما يغذي التجميعات ويساعدها على البقاء. في الوقت نفسه، يمكن لإنزيمات إضافية أن تقص ببطء رابطة إستر مميزة داخل CyMA، محولةً إياها إلى شظايا أكثر محبة للماء تنجرف بعيدًا. ولأن بعض الخلايا السليمة، مثل خلايا الكبد وبعض خلايا الجهاز المناعي، غنية بهذه الإنزيمات القاطعة للإستر، فهي أفضل بطبيعتها في تفكيك CyMA وبالتالي تتأثر أقل.
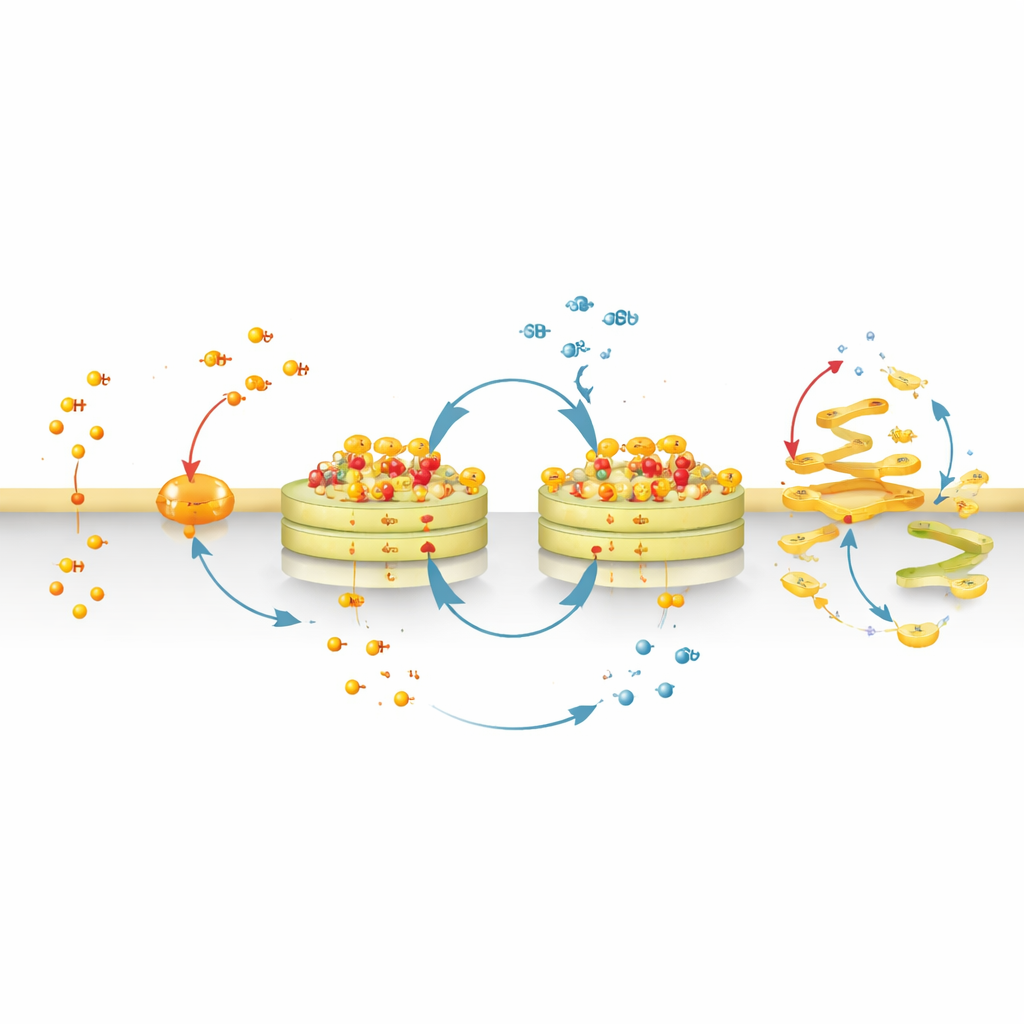
من أداة تصوير رقيقة إلى معطل للغولجي
باستبدال الصبغة الفلورية بمجموعة كيميائية أكثر انجذابًا للأغشية، حوّل الفريق CyMA‑i إلى CyMA‑d، نسخة معطلة لم تعد تتوهّج لكنها تظل تدخل في دورة وتتجمع عند الغولجي. هذه التجميعات تُزعج هيكل الغولجي وتعيق التدفق المستمر للحويصلات إلى الغولجي ومنه. البروتينات التي عادةً تسير من الشبكة الإندوبلازمية إلى الغولجي ثم إلى سطح الخلية تصبح عالقة أو تُوجَّه خطأ. المسارات الواردة — من سطح الخلية عائدًا إلى الغولجي أو من الغولجي إلى عضيات أخرى — تُعطَّل أيضًا. نتيجة لذلك، تفشل مستقبلات سطحية ومولّفات إشارية أساسية في الوصول إلى وجهاتها أو تتراكم في أماكن خاطئة داخل الخلية.
فوضى في الإشارات الخلوية والرسائل السرية
الغولجي هو المكان الذي تتلقى فيه العديد من البروتينات لمساتها النهائية الضرورية، مثل سلاسل السكر وذيول الدهون. تقلل تجميعات CyMA‑d من تدهين وغليكوزلة العديد من البروتينات بالشكل الصحيح، بما في ذلك محفزات سرطان معروفة مثل Ras وبعض مستقبلات التيروسين كيناز الرئيسية. هذه التغييرات تخرب مسارات تعزيز النمو مثل AKT وmTOR. وفي الوقت نفسه، يتراجع الإخراج الإفرازي للخلية: عوامل مهمة مثل TGF‑β1 وVEGF، التي تستخدمها الأورام لقمع المناعة وتحفيز نمو الأوعية الدموية، لم تعد تُفرَز بفعالية. ضغط هذا الانهيار يسبب شبكات إندوبلازمية متشابكة، وتغيّرًا في الميتوكوندريا، وتوقفًا في البلعمة الذاتية (نظام إعادة تدوير الخلية)، وارتفاعًا في البروتينات المتضررة والموسومة باليوبيكوين، مجتمعةً دافعةً الخلايا السرطانية نحو الموت.
ضغط انتقائي على الأورام وآمال للعلاج
لأن CyMA‑d تعتمد على مجموعة مشتركة من الإنزيمات والمواد المُستقَلَبة التي تفرط العديد من خلايا السرطان في استخدامها، يمكنها قتل مجموعة واسعة من أنواع الأورام، بما في ذلك نماذج سرطان المبيض المقاومة للأدوية، بجرعات منخفضة جدًا. الخلايا التي تحتوي على مستويات عالية من استيرازات معيّنة، مع ذلك، تفكك CyMA‑d بسهولة أكبر وتتأثر أقل، مما يوفر مسارًا مضمّنًا للانتقائية. في الألغام الورمية الثلاثية الأبعاد، وزرعات مشتقة من مرضى، ونماذج الفئران، تقلّص CyMA‑d الأورام وتقلّل النقائل وتحدّ من تراكم السوائل في البطن. عند الجمع بينها وبين علاجات نقاط التفتيش المناعية، تعزز أيضًا السيطرة على الورم والبقاء. جوهريًا، يُظهر هذا العمل أن بناء مواد ديناميكية داخل الغولجي — بدلًا من استهداف بروتين واحد — يمكن أن يعطل عمليات حيوية حاسمة للسرطان في آن واحد.
ماذا يعني هذا لعلاجات المستقبل
لفهم عام، الفكرة الأساسية هي أن الباحثين حوّلوا الغولجي من طرف سلبي إلى هدف علاجي فعّال. من خلال تجنيد إنزيمات الخلية نفسها لتجميع وإعادة تدوير جزيئات دقيقة عند هذه المحطة المركزية، يمكنهم إما إبرازها بلا ضرر أو في نهاية المطاف إغراق وظيفتها. تقترح هذه المنصة ذات الاستخدام المزدوج نوعًا جديدًا من العلاج: بدلاً من تصميم دواء واحد لبروتين واحد، قد نصمم سوابق صغيرة تحولها الخلايا إلى مواد تنظّم نفسها ذاتيًا، قادرة على تعطيل شبكات الاتصالات والنقل التي تعتمد عليها السرطانات للنمو والانتشار.
الاستشهاد: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
الكلمات المفتاحية: جهاز غولجي, تجميعات جزيئية, نقل البروتينات, علاج السرطان, استهداف العضيات