Clear Sky Science · ar
تعزيز PDLIM5 البطاني للأوعية لتشكيل خيوط الخلايا الطليعية وتكوُّن الأوعية الورمية عبر تنظيم تَجميع الأكتين المعتمد على ACTN1/ACTN4
كيف تستغل الأورام الأوعية الدموية
لا يمكن للسرطان أن ينمو أكثر من كتلة صغيرة دون إقناع الأوعية الدموية المجاورة بتوفير الأكسجين والمغذيات. تكشف هذه الدراسة كيف يساعد بروتين غير معروف جيدًا في البطانة الداخلية للأوعية على تشجيع الأورام على إنماء فروع جديدة وغير طبيعية. قد يفتح فهم هذه العملية الباب أمام علاجات أذكى لا تقتصر على تجويع الأورام فحسب، بل تجعل العلاج المناعي أكثر فعالية أيضًا.
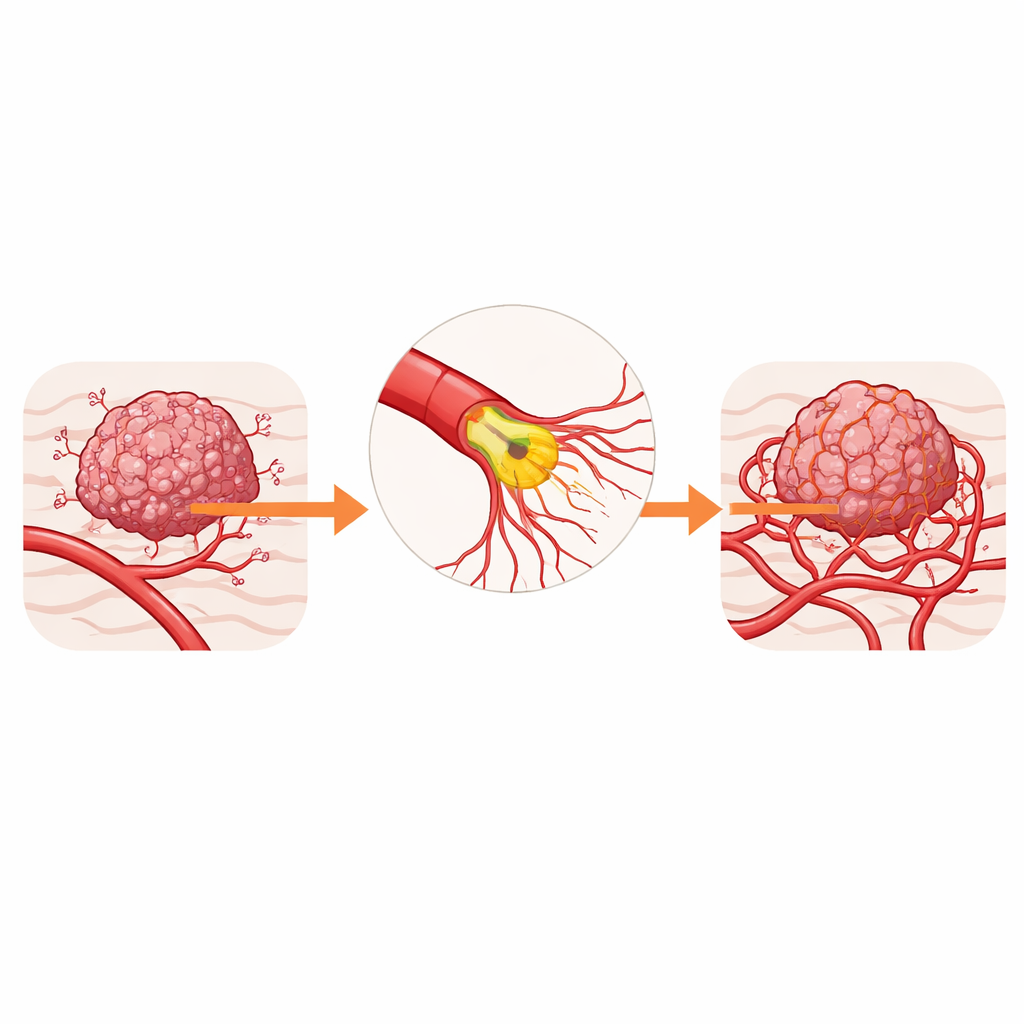
المهندسون الخفيون لإمداد الأورام بالدم
تُبنى الأوعية التي تغذي الأورام من خلايا متخصصة تُسمى الخلايا البطانية، التي تبطن داخل الوعاء. عند مقدمة كل فرع وعائي جديد توجد «خلية طليعة» تطلق نتوءات طويلة تشبه الأصابع تُعرف بالخيوط الهدبية (filopodia). تستشعر هذه النتوءات الإشارات الكيميائية من الورم وتوجّه الفروع الجديدة نحو المناطق المحرومة من الأكسجين. في كثير من السرطانات، يتجاوز هذا التبرعم الحد الطبيعي، مما يولد أوعية متسربة ومتشابكة تزيد من نقص الأكسجين وتجعل من الصعب على الأدوية والخلايا المناعية الوصول إلى الورم.
بروتين يسرّع عملية التبرعم
من خلال فحص خلايا مفردة من أورام رئوية بشرية، وجد الباحثون أن الخلايا البطانية المرتبطة بالورم تنشط بقوة مجموعة من الجينات التي تتحكم في الهيكل الداخلي للخلية، وخصوصًا بروتينًا اسمه PDLIM5. كان مستوى PDLIM5 أعلى في أوعية الورم منه في الأوعية الطبيعية، ومال المرضى الذين عبرت أوعيتهم الورمية عن مستويات أعلى من PDLIM5 إلى أن تكون مدة بقائهم على قيد الحياة أقل. في نماذج فأرية لعدة أنواع من السرطان، أدى تعزيز PDLIM5 في بطانة الأوعية إلى نمو أسرع للأورام وتكوّن شبكات أوعية أكثر كثافة، ما يشير إلى أن هذا البروتين يعمل كمحرك قوي لنمو أوعية الأورام.
كيف يبني PDLIM5 «شعيرات» خلوية
لمعرفة كيف يؤثر PDLIM5 على سلوك الأوعية، لجأت الفرقة إلى أنظمة تجريبية يمكن فيها مراقبة البراعم الجديدة بالتفصيل، مثل أوعية الشبكية النامية في الفأر وزراعات ثلاثية الأبعاد للخلايا البطانية. عندما أُزيل PDLIM5 بطريقة خاصة من الخلايا البطانية، تقدمت البراعم بمعدل أبطأ، وقلت خلايا الطليعة، وتناقصت خيوط الفيلوبوديا بشكل كبير. على مستوى مجهري، وُجد أن PDLIM5 يربط بروتينين رئيسيين تعديلَي تجميع الأكتين، ACTN1 وACTN4، بخيوط طويلة من الأكتين تشكل الإطار الداخلي للخلية. تساعد هذه الجسرية في حزم خيوط الأكتين إلى حزم صلبة تدعم الفيلوبوديا. أدى تحوير نقطتين حاسمتين في PDLIM5 (المسميتان S593 وF596) إلى كسر هذا الاتصال، وإضعاف تجميع الأكتين، ومنع PDLIM5 من استعادة التبرعم الطبيعي، مما يثبت أن هذه المصافحة الجزيئية أساسية لبناء «الشعيرات» في خلية الطليعة.
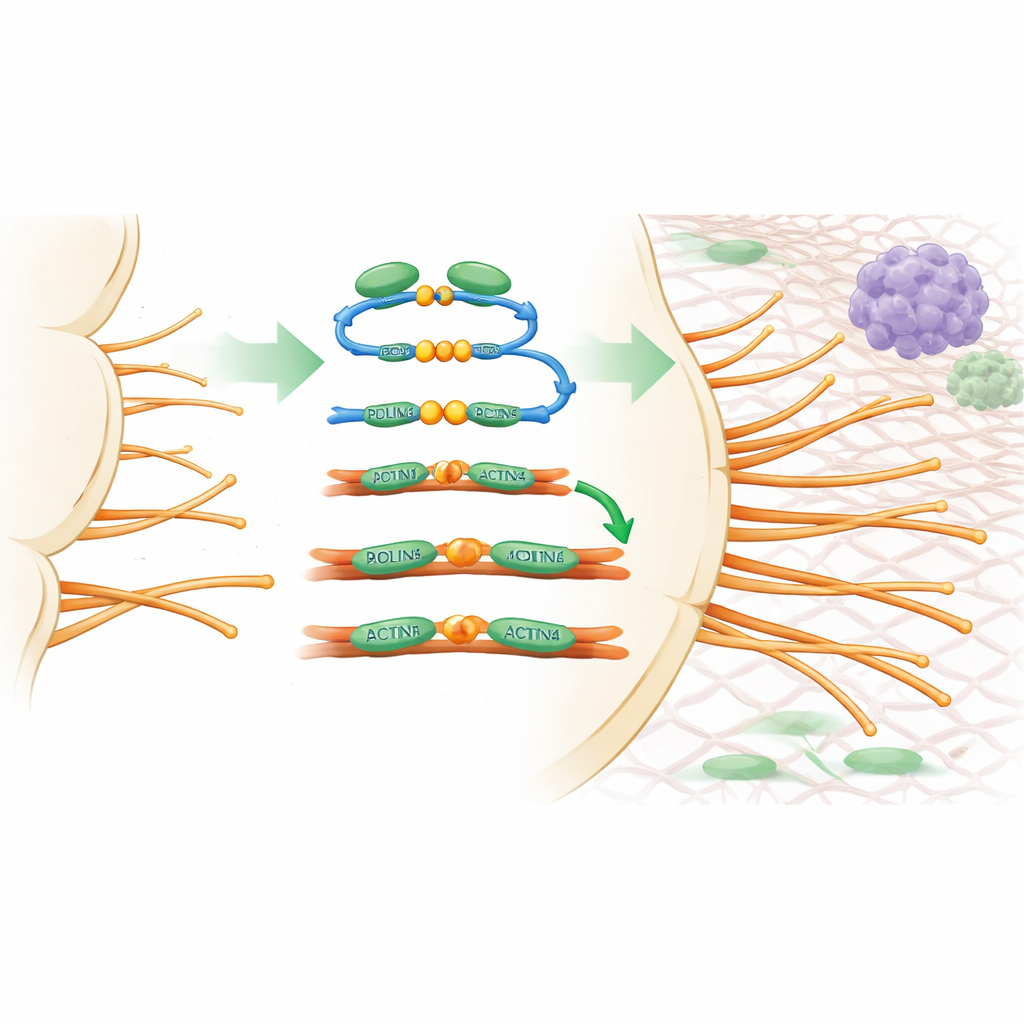
إعادة توصيل أوعية الورم لمساعدة الجهاز المناعي
ومن المدهش أن حجب PDLIM5 في بطانة الأوعية لم يكتفِ بإبطاء نمو الورم. أصبحت أوعية الورم أكثر انتظامًا في الشكل، وأقل تسربًا، ومغطاة بشكل أفضل بخلايا داعمة تعمل على استقرارها. نتيجة لذلك، تحسّن توصيل الأكسجين وتقَصّرت مناطق نقص الأكسجين الحاد. سمحت هذه الأوعية «المطبَّعة» بدخول عدد أكبر من خلايا تي المناعية إلى الورم. غيرت خسارة PDLIM5 أيضًا تنظيم جزيئات الالتصاق على الخلايا البطانية، مما سهّل التصاق خلايا تي بجدران الأوعية واجتيازها إلى نسيج الورم. في أورام فأرية كانت تقاوم عادة أدوية نقاط التفتيش المناعية، جعل حذف PDLIM5 علاجًا بمضاد–PD-L1 أكثر فعالية بكثير، فصغر حجم الأورام وزاد من أعداد خلايا تي المساعدة والقاتلة داخلها.
لماذا يهم هذا لعلاجات السرطان المستقبلية
تُظهر النتائج مجتمعة أن PDLIM5 يعمل كمنظّم مركزي لهكيل الأكتين في خلية الطليعة، مُمكّنًا تكوّن فيلوبوديا قويًا وتبرعمًا وعائيًا سريعًا تجاه الأورام. يؤدي إزالة أو تعطيل PDLIM5 في الخلايا البطانية إلى إبطاء توسع إمداد الدم للورم، ويقوّم ويُثبّت الأوعية المتبقية، ويخفف من حرمان الأكسجين، ويوسع مدخل الخلايا المناعية إلى الورم. بالنسبة للمرضى، تشير هذه النتائج إلى أن أدوية مصممة لتعطيل شراكة PDLIM5–ACTN1/ACTN4 قد تُجوع السرطانات من الأوعية الجديدة وفي الوقت نفسه تُحوّل أوعية الأورام الفوضوية إلى شبكة أفضل تدعم العلاج الكيميائي والعلاج المناعي.
الاستشهاد: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
الكلمات المفتاحية: تكوّن الأوعية في الأورام, خلايا الطليعة البطانية, PDLIM5, هيكل الأكتين الخلوي, العلاج المناعي للسرطان