Clear Sky Science · ar
الأساس البنيوي لعكس الشوكة وتنظيم RAD51 بواسطة مركب ليجاز الإيوبيوتين SCF الخاص بالهيليكاز F-box 1
كيف تنقذ الخلايا آلة نسخ الحمض النووي المتعثرة
في كل مرة تنقسم فيها الخلية، يجب أن تنسخ مليارات الحروف الخاصة بالحمض النووي بسرعة ودقة. لكن آلية النسخ هذه كثيرًا ما تواجه مشاكل—قد يتسبب تلف الحمض النووي أو تسلسلات صعبة النسخ أو العلاجات الدوائية في توقف العملية. عندما يحدث ذلك، تعتمد الخلايا على فرق إصلاح طارئة لتثبيت شوكات النسخ وإعادة تشغيلها. تُظهر هذه الورقة، بتفصيل بنيوي غير مسبوق، كيف يعيد قائد أحد هذه الفرق—مركب بروتيني مبني حول الهيليكاز FBH1—تشكيل الحمض النووي المتعثر ويحافظ على بروتين إصلاح رئيسي آخر، RAD51، تحت رقابة صارمة. يساعد فهم هذا التنسيق في تفسير كيف تتجنب الخلايا تكسرات خطيرة في الجينوم ولماذا ترتبط اختلالات هذه العوامل بالسرطان.
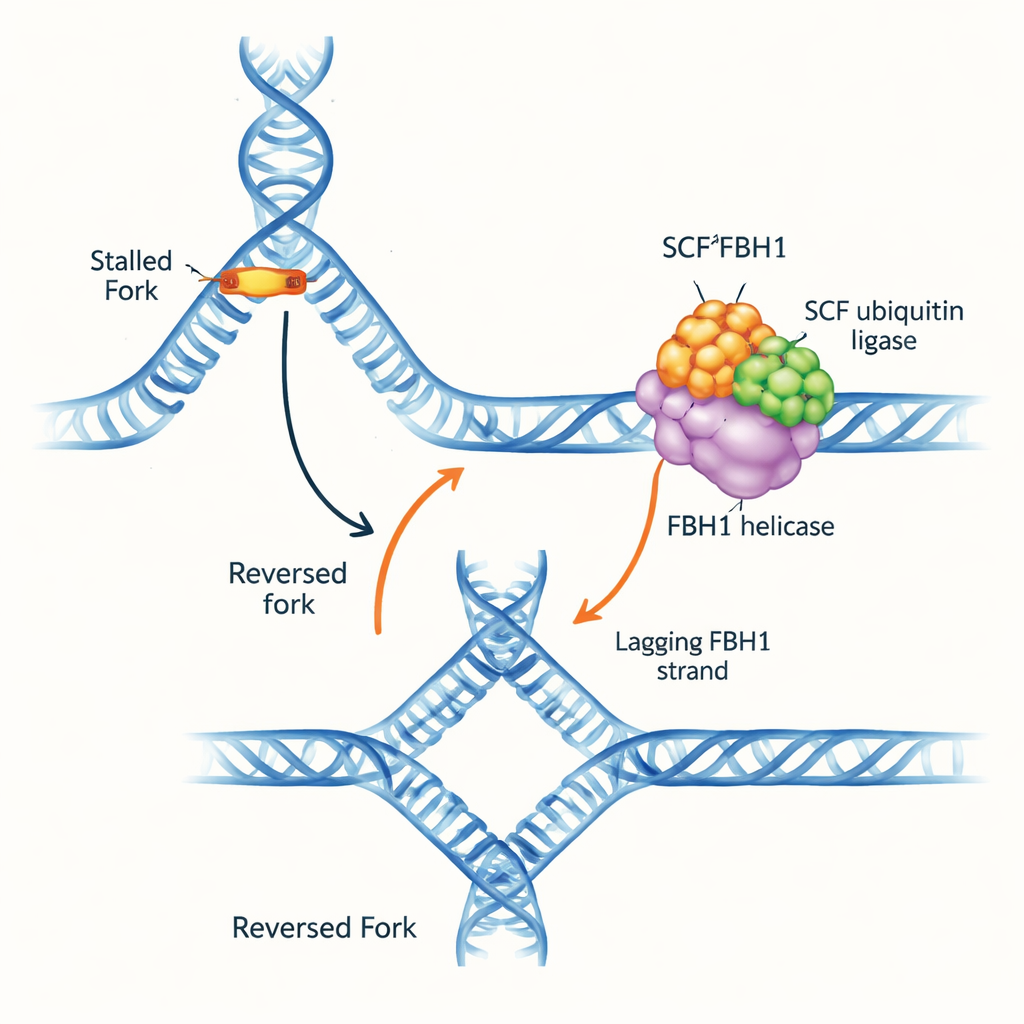
ازدحام مروري على طريق الحمض النووي السريع
شوكات نسخ الحمض النووي هي هياكل على شكل حرف Y حيث يُفكك اللولب المزدوج ويُنسخ. عندما تصادف الشوكة عوائق، يمكن أن تنعكس اتجاهاتها: تعيد الخيوط الأبوية الاقتران، وتقترن الخيوط الجديدة ببعضها، مكونة مفترقًا رباعيًا من الحمض النووي. يمكن لهذا «عكس الشوكة» أن يكسب وقتًا لإصلاح الضرر وإعادة تشغيل النسخ بأمان، لكنه إن أُسيء إدارته يُنتج أيضًا حمض نووي هشا قد ينكسر. تُعرف عدة محركات جزيئية بدفع الشوكات للخلف عن طريق الإمساك بالحمض النووي مزدوج الشريط أمام الشوكة. ومع ذلك، برز FBH1 لأنه يتصرف بشكل مختلف وغالبًا ما يتعرض لتغيرات في الأورام، مما يوحي أنه يعمل عبر مسار متميز ومهم طبيًا.
أخصائي الشوكة ذو الجانب المفضل
نقى المؤلفون مركب SCFFBH1 البشري، الذي يجمع بين هيليكاز FBH1 ووحدة وضع وسوم الإيوبيوتين (SCF). سألوْا أولاً أي أشكال من الحمض النووي يفضلها FBH1. باستخدام تجارب الارتباط والفك، أظهروا أن SCFFBH1 يفضل بقوة هياكل تشبه الشوكة الحقيقية، خصوصًا حيث توجد قطعة قصيرة من الحمض النووي أحادي الشريط على خيط القالب «المتأخر»—الجانب المنسوخ بقطع صغيرة. على هذه الهياكل، يفكك FBH1 الحمض النووي بسرعة أعلى بمئات المرات مقارنةً بطرف سائب بسيط، ما يشير إلى أن الالتقاط السليم عند مفصل الشوكة يعزز نشاط محركه بشكل كبير. أكدت أدوات الملاقط المغناطيسية أحادية الجزيء أن المركب يمكنه فك ثم التحرك على طول الحمض النووي أحادي الشريط لآلاف القواعد دون أن يسقط، مما يجعله محركًا قويًا ومستمرًا.
عكس الشوكة عن طريق السحب من الخلف
لكي يكتشف الفريق كيف يعكس هذا المحرك الشوكات فعليًا، اختبروا ركائز شوكة اصطناعية بها أو بدون فجوات أحادية الشريط. بخلاف معدِّلات الشوكة الأخرى، لم يستطع SCFFBH1 أن يعمل على شوكة كاملة الاقتران؛ بل احتاج إلى فجوة على قالب الخيط المتأخر وتحرك في الاتجاه من 3′ إلى 5′ على ذلك الخيط الأحادي. هذا الحركة «السحب من الخلف» تدفع الخيوط الأبوية لإعادة الاقتران بينما يظل الإنزيم مثبتًا عند المفصل الشوكي. تُظهر صورة مجهرية إلكترونية مجمدة (cryo-EM) لمركب SCFFBH1 مرتبطًا بشوكة متعثرة كيف يتم ذلك: رقعة موجبة الشحنة خاصة، «موقع ربط المفصل» في أحد تحت نطاقات FBH1، تتربع عند نقطة التفرع حيث تلتقي الأذرع الثلاثة للحمض النووي. عندما طوَّر الباحثون طفرات في حمض أمينيين أساسيين في هذا الموقع، انخفضت قدرة عكس الشوكة بحوالي 25 ضعفًا في الاختبارات المختبرية، بينما ظل محرك الفك الأساسي يعمل بشكل معقول. في الخلايا، منعت نفس الطفرة الإبطاء الطبيعي لشوكات النسخ استجابةً لدواء يسبب الإجهاد، وهو علامة مميزة لفشل عكس الشوكة.
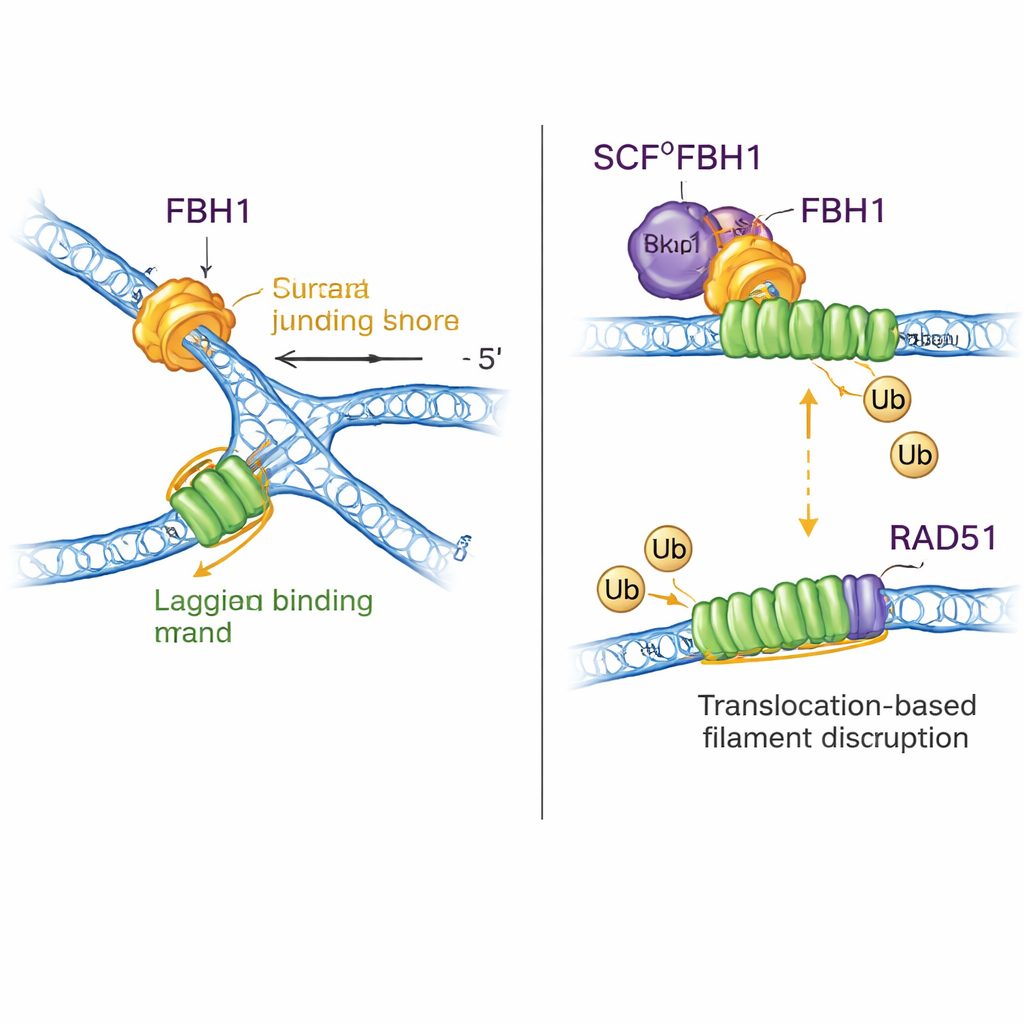
دور مزدوج: إعادة تشكيل الحمض النووي وإزالة RAD51
لا يُعد FBH1 مجرد محرك؛ من خلال مركب SCF يساعد أيضًا على ربط وسوم إيوبيوتين صغيرة بالبروتينات. تُركب الهياكل الجديدة تقريبًا كامل مركب SCFFBH1–الحمض النووي وتُظهر أن «رأس» نقل الإيوبيوتين في الليغاز يجلس على مسافة تقل عن 45 أنغستروم من خيط القالب المتأخر الخارج من FBH1. من خلال دمج هياكل معروفة لليغازات إيوبيوتينية أخرى، يقترح المؤلفون أن هذه الهندسة تضع RAD51—الإنزيم الذي يشكل خيوطات على الحمض النووي لتعزيز إعادة التركيب—مباشرة في خط النار على الخيط المتأخر لشوكة متعطلة. أظهرت أعمال سابقة أن FBH1 قادر ميكانيكيًا على تجريد RAD51 من الحمض النووي وأيضًا وسمه بالإيوبيوتين بحيث لا يعاود الارتباط بسهولة. يوحد النموذج الجديد هذه الأفكار: بينما يسحب FBH1 على طول الخيط المتأخر لإعادة تشكيل الشوكة، يمكن لوحدة SCF القريبة أن تضع وسم إيوبيوتين على وحدات RAD51، مما يساعد على تفكيك أو منع تكوّن خيوطات RAD51 المفرطة التي قد تحجب معالجة الشوكة بشكل صحيح.
ماذا يعني هذا لاستقرار الجينوم والسرطان
معًا، تُظهر الدراسة أن SCFFBH1 يعكس شوكات نسخ الحمض النووي المتعثرة باستخدام آلية مميزة عن معدِّلات الشوكة المعروفة الأخرى: إنه يمسك بنقطة التفرع بإحكام أثناء الانتقال على قالب الخيط المتأخر من الخلف، مما يعزز إعادة اقتران الخيوط الأبوية بأمان دون تشكيل مفترق رباعي طويل العمر ومتحرك. في الوقت نفسه، يكون ليغاز الإيوبيوتين المدمج موضعيًا لإزالة RAD51 من نفس الخيط، مانعًا حدوث إعادة تركيب مفرطة خلال إجهاد النسخ. لأن FBH1 غالبًا ما يُفقد أو يتعرض لطفرات في السرطانات، تساعد هذه الرؤى البنائية والآلية على تفسير كيف تتراكم أضرار الحمض النووي في مثل تلك الأورام ولماذا قد تستجيب بشكل مختلف للأدوية التي تحفز إجهاد النسخ أو تستهدف المسارات ذات الصلة.
الاستشهاد: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
الكلمات المفتاحية: إجهاد نسخ الحمض النووي, عكس الشوكة, هيليكاز FBH1, تنظيم RAD51, استقرار الجينوم