Clear Sky Science · ar
الكاينورينين يتوسط السمية المعوية الناجمة عن العلاج الكيميائي عبر تعديل ميكروبيوتا الأمعاء
لماذا يهم هذا الأشخاص الذين يتلقون العلاج الكيميائي
ينقذ العلاج الكيميائي الأرواح، لكنه غالباً ما يصاحبه آثار جانبية قاسية في الأمعاء—ألم، إسهال، فقدان الوزن—قد تدفع الأطباء إلى تخفيض الجرعات أو إيقاف العلاج مبكراً. تكشف هذه الدراسة عن سلسلة تفاعلات خفية بين مركب في الدم، وخلايا مناعية، وميكروبات الأمعاء تشرح لماذا يمكن لدواء سرطاني شائع مثل oksaliplatin أن يكون قاسياً على الأمعاء، وتشير إلى طرق جديدة لحماية المرضى دون إضعاف فعالية العلاج المضاد للسرطان.
حلقة كيميائية بين العلاج وتلف الأمعاء
بدأ الباحثون بالمرضى المصابين بسرطان القولون والمستقيم الذين يتلقون علاجاً كيميائياً قائمًا على oksaliplatin. قارنوا عينات دم من أشخاص ظهرت لديهم آثار معوية شديدة مع أولئك الذين تحملوا العلاج بشكل أفضل. باستخدام تحليل كيميائي مستهدف، وجدوا أن عدة نواتج تفكك لحمض الأمين التريبتوفان كانت أعلى في مجموعة السمية العالية، مع تميّز جزيء واحد—إل‑كاينورينين—بكونه الأعلى ارتفاعاً. كما أظهر المرضى الذين لديهم مستويات أعلى من إل‑كاينورينين في دمهم علامات أكثر للالتهاب وانخفاضاً في عدد خلايا الدم البيضاء، ما يوحي بأن هذا الجزيء قد يرتبط مباشرة بالضرر المرتبط بالعلاج.
إثبات السبب والنتيجة في الفئران
للانتقال من الارتباط إلى السببية، لجأت الفرق إلى نماذج فئران. عندما أعطي فئران سليمة جرعات عالية من oksaliplatin، طورت علامات كلاسيكية لإصابة الأمعاء: فقدان الوزن، قصر القولون، تورم جدار الأمعاء، انخفاض الخلايا المنقسمة، وزيادة الخلايا الميتة في بطانة الأمعاء. كما أظهرت هذه الفئران ارتفاعاً حاداً في إل‑كاينورينين في دمها، مما يعكس البيانات البشرية. عندما غذّوا فئران المعالجة بالـoksaliplatin بمزيد من إل‑كاينورينين، ازداد تلف الأمعاء—مع بقاء قوة الدواء المضادة للأورام سليمة. وبالمقابل، عندما أزالوا أو منعوا الإنزيم IDO1، الذي يستخدمه الجسم لتحويل التريبتوفان إلى إل‑كاينورينين، أصبحت الفئران أكثر مقاومة لسمية الأمعاء بينما استمرت في الاستفادة من العلاج الكيميائي.
الخلايا المناعية وميكروبات الأمعاء في خط النار
بتعمق أكثر، سأل العلماء أي الخلايا كانت مسؤولة عن إنتاج فائض إل‑كاينورينين أثناء العلاج. وجدوا أن oksaliplatin يحفز خلايا مناعية معينة (خلايا CD8 T) لإطلاق بروتين إشاري يسمى الإنترفيرون‑غاما، الذي بدوره يشغّل IDO1 في الخلايا النخاعية المجاورة—وهي فئة من خلايا الدم البيضاء. الفئران المعدلة بحيث كانت خلاياها النخاعية فقط تفتقر إلى IDO1 أنتجت كميات أقل بكثير من إل‑كاينورينين وحُمت من إصابة الأمعاء، في حين أن حذف IDO1 فقط في خلايا بطانة الأمعاء كان له تأثير ضئيل. في الوقت نفسه، تغيرت تركيبة ميكروبيوتا الأمعاء. في الفئران الطبيعية، ارتبط oksaliplatin والمستويات المرتفعة من إل‑كاينورينين بفقدان بكتيريا مفيدة، Lactobacillus johnsonii. في المقابل، حافظت الفئران ذات مستويات إل‑كاينورينين المنخفضة على مستويات أعلى من L. johnsonii. عندما تم القضاء على بكتيريا الأمعاء بالمضادات الحيوية، اختفى التأثير الوقائي للمستويات المنخفضة من إل‑كاينورينين، وعندما نُقلت بكتيريا من فئران ذات إل‑كاينورينين منخفض إلى فئران عادية، أصبح المستلمون أكثر قدرة على مقاومة تلف الأمعاء الناجم عن oksaliplatin.
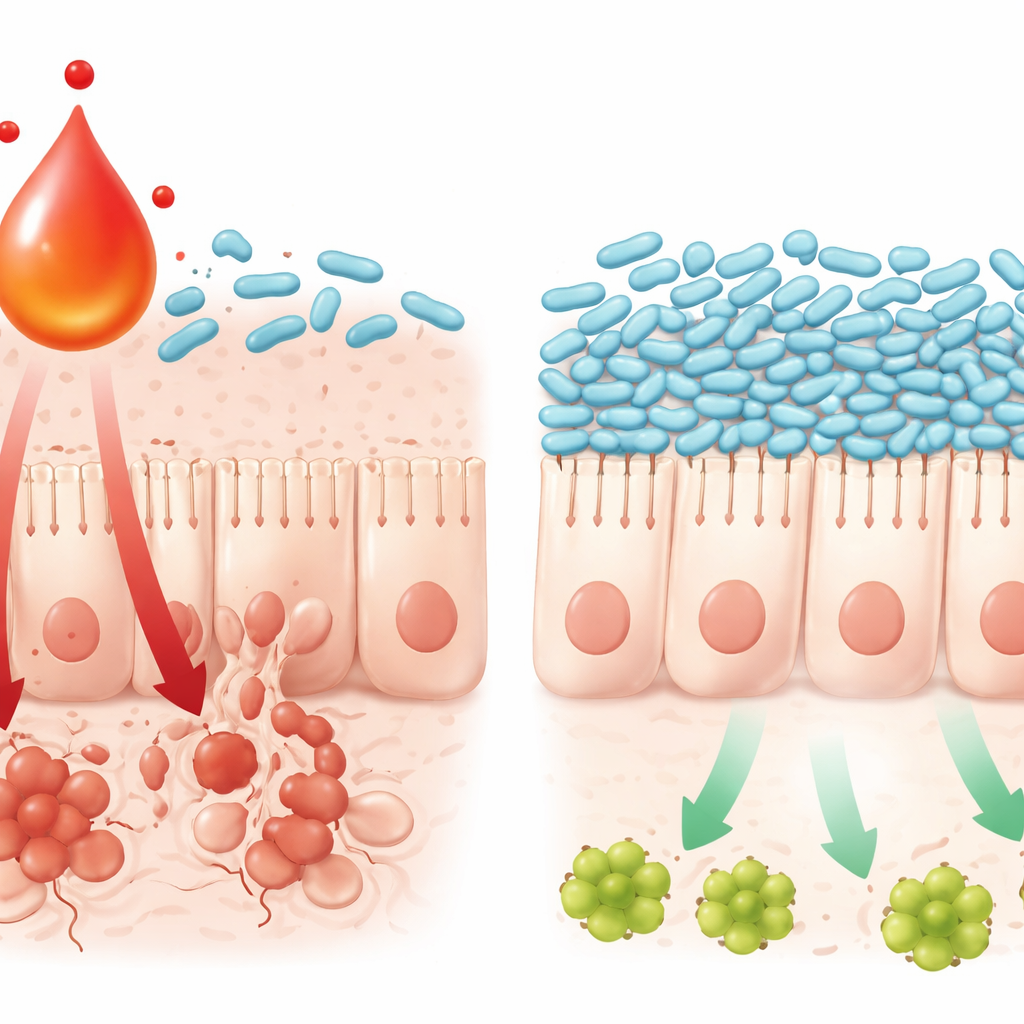
كيف يدفع مستقلب واحد خلية الأمعاء نحو الموت
تتبعت الدراسة أيضاً كيف يسبب هذا التفاعل الكيميائي‑الميكروبي إصابة بطانة الأمعاء. ارتبطت مستويات إل‑كاينورينين العالية بزيادة نشاط مسار التهابي معروف في أنسجة الأمعاء، مسار TNFα/JNK، الذي يدفع الخلايا نحو الموت المبرمج. في زراعة الخلايا، جعل الجمع بين oksaliplatin وإل‑كاينورينين خلايا الأمعاء أكثر ميلاً لتنشيط هذا المسار والموت، بينما أدى إضافة بكتيريا L. johnsonii إلى كبح الإشارة والحفاظ على بقاء الخلايا. كما أن إل‑كاينورينين نفسه استطاع إبطاء نمو L. johnsonii وتقويض آليات بقائها في أطباق المختبر، مما يساعد على تفسير سبب اختفاء هذه البكتيريا عندما يتراكم المستقلب. مجتمعة، ترسم هذه النتائج حلقة تعزيز ذاتي: يحفز العلاج الكيميائي إشارات مناعية، ترفع الخلايا المناعية مستوى إل‑كاينورينين، هذا يزعزع البكتيريا المفيدة مثل L. johnsonii، وتعمل المجموعة الميكروبية المتغيرة على تضخيم الإشارات الالتهابية التي تقتل خلايا الأمعاء.
طرق جديدة لحماية المرضى أثناء العلاج
بشكل مشجع، تشير النتائج أيضاً إلى استراتيجيات عملية. عالج إعطاء دواء يسمى Epacadostat، وهو مثبط لـIDO1، الفئران فأنخفضت مستويات إل‑كاينورينين وقلّت إصابات الأمعاء الناجمة عن oksaliplatin بشكل ملحوظ دون إضعاف السيطرة على الورم. في نهج متمم، هندس الفريق سلالة غير ضارة من E. coli لإنتاج كمية زائدة من إنزيم يكسر إل‑كاينورينين في الأمعاء. كانت الفئران التي أعطيت هذه البكتيريا المهندسة محمية بالمثل من سمية الأمعاء، مرة أخرى دون الإخلال بتأثير العلاج الكيميائي المضاد للسرطان. كما خفف إعطاء L. johnsonii نفسه الأعراض وحافظ على بنية الأمعاء.
ماذا يعني هذا للأشخاص المصابين بالسرطان
مجتمعة، تكشف هذه الدراسة أن مستقلباً واحداً مدفوعاً بالعلاج—إل‑كاينورينين—يعمل كوسيط رئيسي بين العلاج الكيميائي والجهاز المناعي وميكروبات الأمعاء وإصابة الأمعاء. من خلال إظهار أن حجب إنتاجه أو تعزيز تكسيره أو استعادة البكتيريا الواقية يمكن أن يخفف من وطأة العلاج الكيميائي على الأمعاء، تفتح هذه الأبحاث طريقاً نحو علاجات مساعدة تبقي المرضى أقوى وأكثر راحة أثناء محاربتهم للسرطان.
الاستشهاد: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
الكلمات المفتاحية: آثار جانبية للعلاج الكيميائي, ميكروبيوم الأمعاء, استقلاب التريبتوفان, إل-كاينورينين, سرطان القولون والمستقيم