Clear Sky Science · ar
تحويل ثاني أكسيد الكربون إلى أكسيدات متعددة الكربون بمستوى أمبير في إلكتروليز حمضي عبر إعادة بناء البيئة الدقيقة على السطح
تحويل مشكلة مناخية إلى سوائل مفيدة
ثاني أكسيد الكربون الناتج عن حرق الوقود الأحفوري يُسخّن كوكبنا، لكنه أيضاً مادة خام محتملة. تبحث هذه الدراسة كيفية تحويل CO2 إلى مواد كيماوية سائلة ذات قيمة، مثل الإيثانول وحمض الأسيتيك، باستخدام الكهرباء. يوضح الباحثون أنه من خلال إعادة تصميم المحيط المباشر لقطب نحاسي بعناية، يمكنهم جعل هذا التحول أسرع وأكثر كفاءة، ومتوافقاً مع ظروف حمضية شديدة كانت عادةً تعطل مثل هذه التفاعلات.
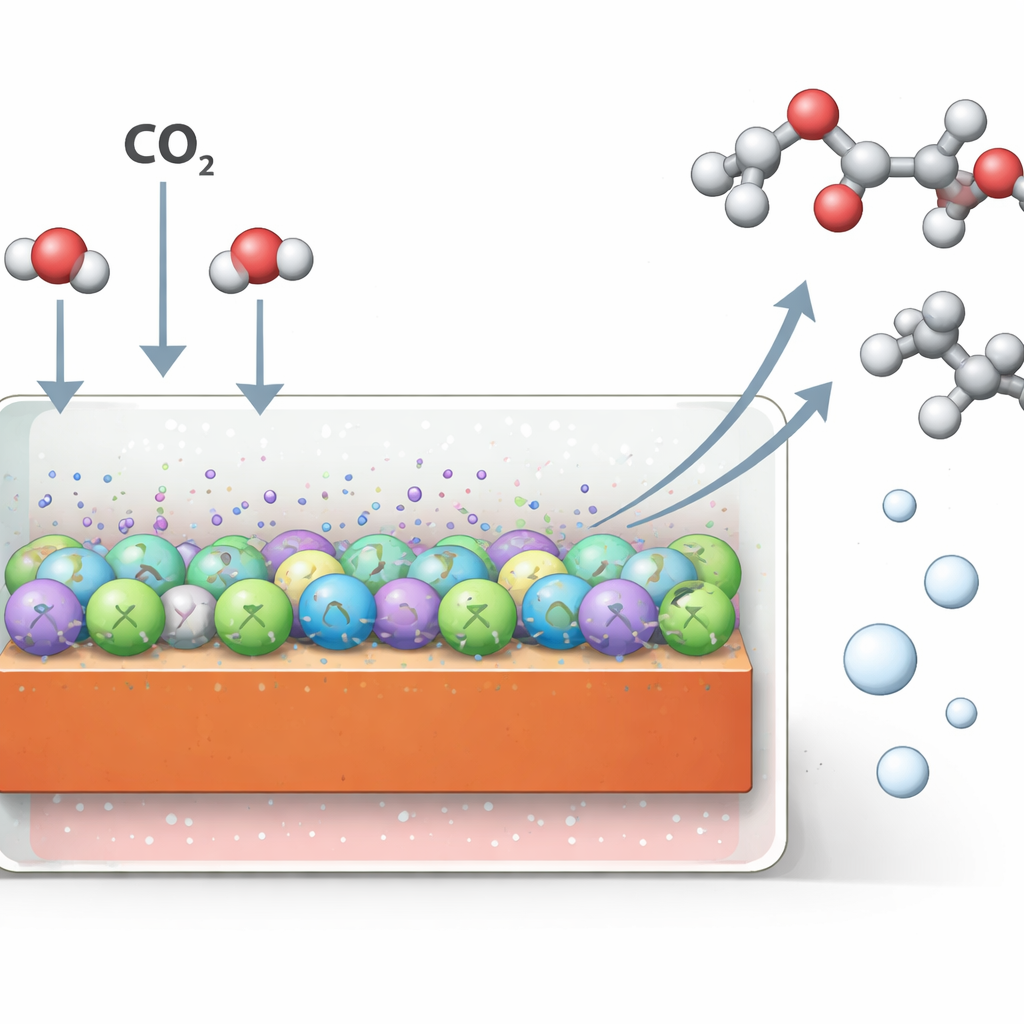
لماذا من الصعب صنع وقود سائل من CO2
يحلم العلماء منذ زمن طويل باستخدام فائض الكهرباء المتجددة لتحويل CO2 إلى منتجات غنية بالطاقة، مخزنين ضوء الشمس والرياح في صورة كيميائية. يُعد النحاس واحداً من المواد القليلة القادرة على ربط ذرات الكربون في جزيئات متعددة الكربون، بما في ذلك الكحولات والأحماض التي تستخدمها الصناعة بالفعل. ومع ذلك، اعتمد معظم التقدم حتى الآن على محاليل قلوية (قاعدية)، التي تتسبب في ضياع CO2 على شكل كربونات غير مرئية وتسد الأجهزة بأملاح. تتجنب المحاليل الحمضية هذه المشكلات، لكن في مثل هذه الظروف يميل النحاس إلى نزع الأكسجين من السلاسل المتوسطة الواعدة، مفضلاً غازات بسيطة مثل الإيثيلين والهيدروجين بدلاً من السوائل الحاوية على الأكسجين.
بناء سطح نحاسي أذكى
لتجاوز هذا المأزق، أنشأ الفريق قطباً نحابياً معدلًا أطلقوا عليه IL@Cu. شكّلوه عن طريق اختزال أكسيد النحاس في محلول مائي يحتوي على سائل أيوني محدد بعناية، وهو ملح يكون سائلاً بالقرب من درجة حرارة الغرفة. تلتصق المكونات الموجبة الشحنة لهذا السائل الأيوني، المبنية على جزيء يُدعى Bmim، بشكل موحد بجسيمات نحاسية صغيرة، مما يمنح السطح شحنة موجبة لطيفة. أكدت تقنيات الميكروسكوب المتقدم والأشعة السينية أن النحاس الأساسي يبقى معدنياً بينما يشكل السائل الأيوني طبقة رقيقة مثبتة جيداً تعدل كيفية ترتيب الأيونات والماء عند الواجهة التي يتحول عندها CO2.
دفع الأداء إلى مستويات صناعية
عندما اختبر الباحثون IL@Cu في محلول متدفق حمضي من كبريتات البوتاسيوم، حققوا تيارات كهربائية كبيرة جداً — حتى أمبيرين لكل سنتيمتر مربع، وهو ما يقارن بالإلكتروليز الصناعي. تحت هذه الظروف المتطلبة، أنتج النحاس المعدّل منتجات متعددة الكربون بكفاءة فارادية تقارب 83%، ما يعني أن معظم الإلكترونات استُخدمت لصنع الجزيئات المطلوبة بدلاً من التفاعلات الجانبية المهدرة. والأكثر إثارة للانتباه، أن نحو 60% من التيار ذهب تحديداً إلى المنتجات السائلة الحاوية على الأكسجين، وشكل الإيثانول وحده حوالي نصف ذلك. كما استُخدم CO2 الوارد بكفاءة: نحو أربعة أخماس الغاز المارّ تم تحويله في مرور واحد، وحافظ المحفز على نشاطه وتركيبه خلال أكثر من 100 ساعة من التشغيل.
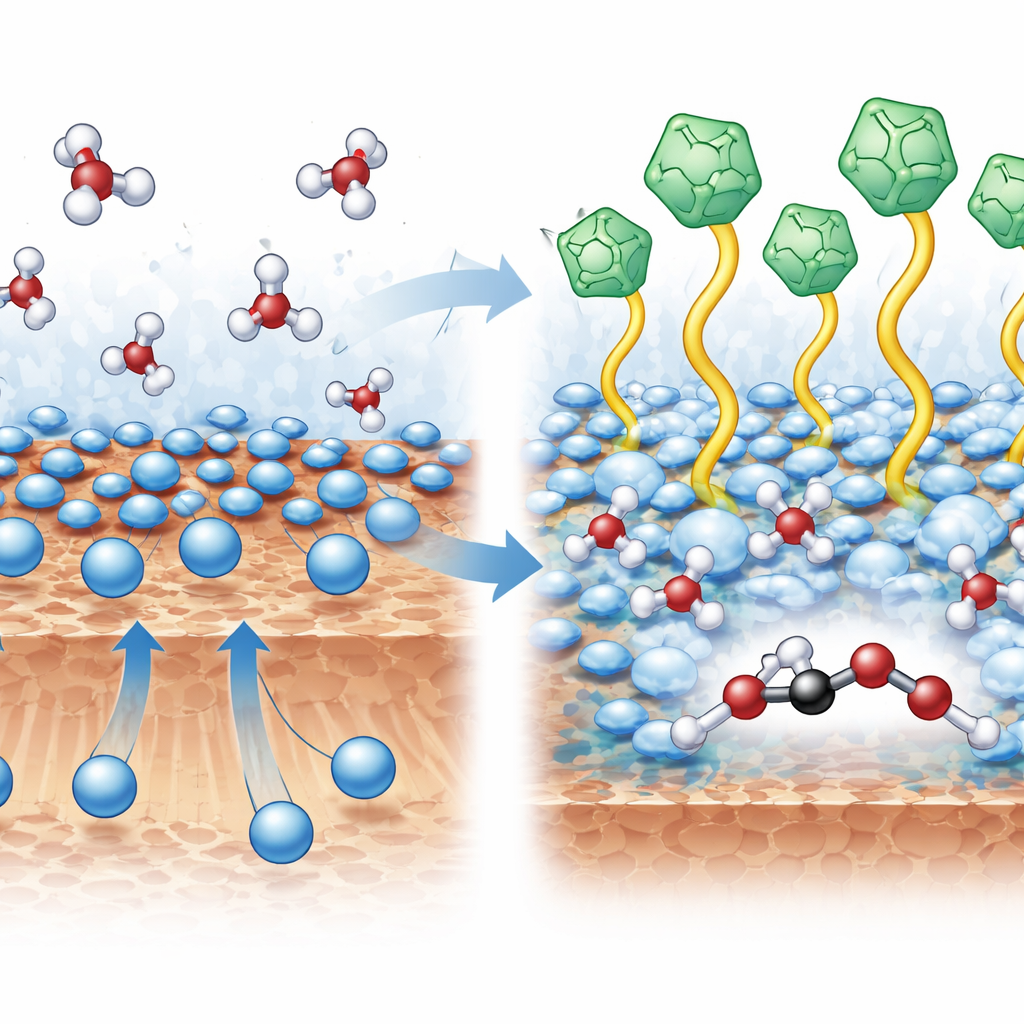
إعادة ترتيب الماء والأيونات عند السطح
يكمن جوهر التقدم في الترتيب المجهري للأيونات والماء حيث يحدث التفاعل. كشفت قياسات طيفية ومحاكاة حاسوبية أن كاتيونات السائل الأيوني تدفع أيونات البوتاسيوم القريبة بعيداً عن سطح النحاس. يفسح هذا المجال لجزيئات الماء لتقترب أكثر وتشكل شبكة روابط هيدروجينية أكثر ترابطاً حول الوسائط الثنائية الكربون الأساسية. مع إبقاء البوتاسيوم عند مسافة مثلى، يمكن لقطع الكربون أن تتحد بسهولة أكبر بدلاً من الانفصال كأول أكسيد الكربون. وفي الوقت نفسه، تساعد شبكة الماء المحيطة على حفظ الأكسجين في الجزيئات النامية بدلاً من السماح للروابط بالانكسار وإطلاق غاز الإيثيلين. أظهرت حسابات ميكانيكا الكم أن هذا الوسط المعاد تنظيمه يخفض حاجز الطاقة لتكوين رابطة كربون–كربون ويميل بمسار التفاعل نحو السوائل الغنية بالأكسجين مثل الإيثانول.
هندسة الطبقة غير المرئية التي تهم
جوهر الدراسة هو أنه من الممكن أن يكون التحكم في «البيئة الدقيقة» — ترتيب الأيونات والماء على مقياس النانومتر عند القطب — بنفس أهمية اختيار المعدن المناسب. عن طريق تثبيت جزيئات السائل الأيوني على النحاس، يعزز المؤلفون في آن واحد معدل تحويل CO2، ويُفضلون منتجات متعددة الكربون التي يسهل تخزينها ونقلها، ويحافظون على استقرار الجهاز في محاليل حمضية أكثر عملية للتشغيل طويل الأمد. قد توجه هذه الاستراتيجية المتمثلة في إعادة تصميم الطبقة الرقيقة غير المرئية حيث تحدث التفاعلات تطوير أنظمة الجيل التالي التي تحول CO2 النفاية إلى كيماويات ووقود مفيد بمقاييس ذات صلة بتخفيف تغير المناخ.
الاستشهاد: Yin, Y., Ling, Z., Liu, S. et al. Ampere-level CO2 electroreduction to multi-carbon oxygenates in acidic electrolyte through surface microenvironment reconstruction. Nat Commun 17, 2353 (2026). https://doi.org/10.1038/s41467-026-68739-z
الكلمات المفتاحية: اختزال كهربائي لثاني أكسيد الكربون, محفز النحاس, الأملاح الأيونية السائلة, إنتاج الإيثانول, إعادة تدوير ثاني أكسيد الكربون الكهروكيميائي