Clear Sky Science · ar
جيمسيتابين مع سيلينيكسور في ساركومات متقدمة انتقائية: المرحلة الأولى من دراسة المجموعة الإسبانية لأبحاث الساركومة
أمل جديد لسرطان نادر وصعب
الساركومات هي سرطانات نادرة تصيب غالبًا البالغين الشباب ويمكن أن تكون صعبة العلاج عندما تنتشر. بالنسبة للعديد من المرضى، تُبقي الأدوية الحالية المرض تحت السيطرة لفترة قصيرة فقط. تختبر هذه الدراسة تركيبًا دوائيًا جديدًا — دواء كيميائي قديم يُدعى جيمسيتابين إلى جانب حبة مستهدفة أحدث، سيلينيكسور — لمعرفة ما إن كان العمل معًا يمكن أن يبطئ أو يقلص الساركومات المتقدمة بشكل أفضل مع الحفاظ على آثار جانبية قابلة للتحكم.
لماذا قد يكون الجمع بين دوائين أفضل
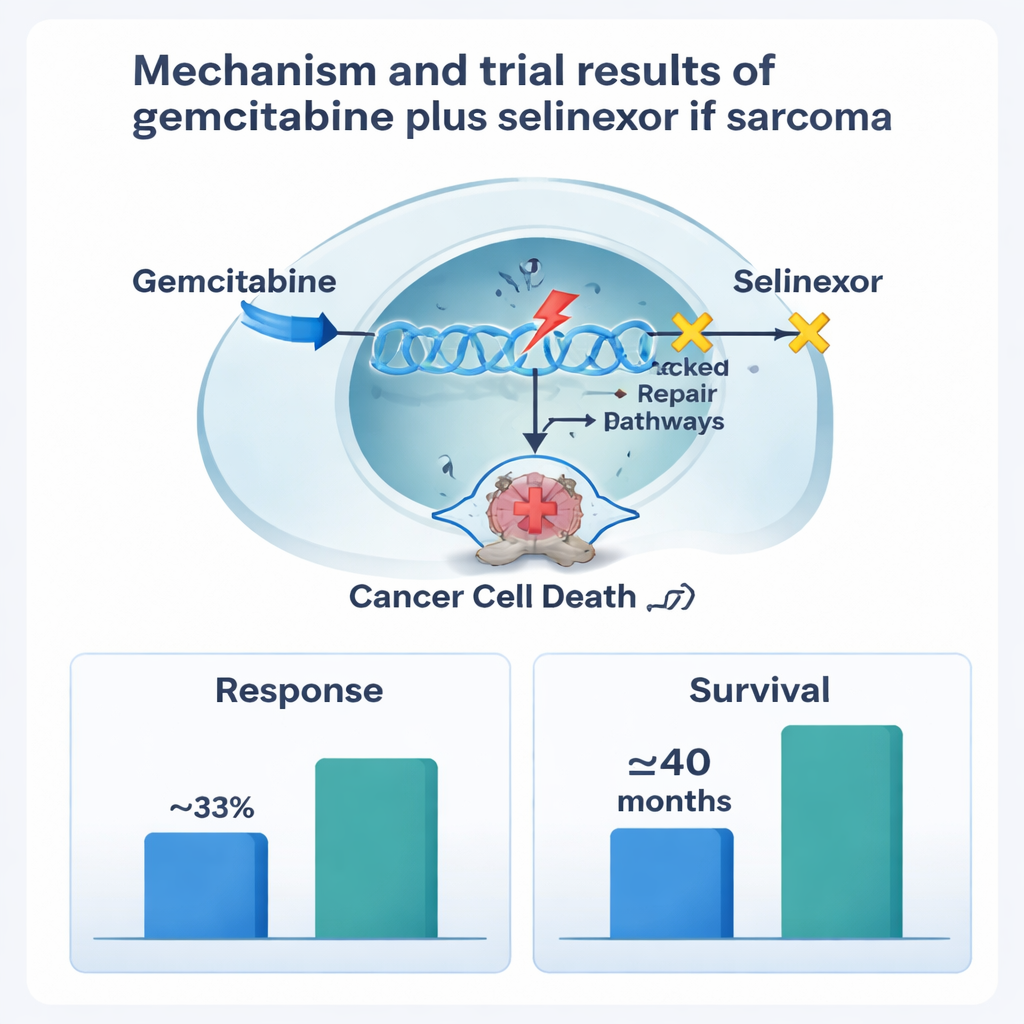
جيمسيتابين هو علاج كيميائي قياسي يتلف الحمض النووي للخلايا سريعة الانقسام، بما في ذلك الخلايا السرطانية. يعمل سيلينيكسور بطريقة مختلفة تمامًا: يمنع بروتينًا يسمى إكسبورتيـن-1، الذي يساعد عادة على نقل بروتينات التحكم المهمة خارج نواة الخلية. عندما يكون إكسبورتيـن-1 مفرط النشاط، كما في العديد من الأورام، يمكن للخلايا السرطانية أن تتجنب «إشارات الإيقاف» الداخلية وتقاوم الأدوية. بحبس بروتينات كابحة للأورام داخل النواة، يمكن لسيلينيكسور دفع الخلايا السرطانية نحو الاندثار الذاتي. أشارت الأعمال المخبرية إلى أن إعطاء جيمسيتابين أولًا لإتلاف الحمض النووي، يليه سيلينيكسور لوقف آليات الإصلاح والبقاء، قد يكون فعالًا بشكل خاص في بعض أنواع الساركومة.
إشارات واعدة في تجارب المختبر
قبل علاج المرضى، اختبر الباحثون الدوائين معًا في خلايا سرطانية مزروعة في المختبر، مع التركيز على ثلاثة أنواع من الساركومة: ليوميو ساركوما، وساركومة عظمية، وأورام الغمد العصبي الطرفية الخبيثة. في عدة خطوط خلوية من ليوميو ساركوما وأورام غمد العصب، قتلت التركيبة مزيدًا من الخلايا السرطانية مقارنة بكل دواء بمفرده، ما أظهر تآزرًا حقيقيًا. أبدت هذه الخلايا مزيدًا من تلف الحمض النووي ومعدلات أعلى من موت الخلايا المبرمج عند استخدام الدوائين معًا. درست المجموعة أيضًا بروتينات تساعد الخلايا على البقاء والانقسام، مثل بروتين يُسمى سيرفيفين. عندما خفض سيلينيكسور مستويات السيرفيفين إلى حد كبير وغير بروتينًا آخر، IκBα، كانت التركيبة فعالة بشكل خاص. في المقابل، أظهرت خلايا الساركومة العظمية غالبًا تأثيرًا معاكسًا: تداخل الدوائين مع بعضهما، ما يشير إلى أن هذا النهج قد يفيد أنواعًا معينة فقط من الساركومات.
كيفية إدارة الدراسة على المرضى
سجلت التجربة السريرية 17 بالغًا في إسبانيا يعانون ساركومات متقدمة نمت رغم خضوعهم لجولة واحدة على الأقل من العلاج القياسي. كان معظمهم يعانون ليوميو ساركوما، وكان عدد أصغر يعاني ساركوما عظمية أو نوعين نادرين آخرين من الساركومة. استخدم الأطباء تصميمًا تدريجيًا دقيقًا لتحديد أعلى جرعة يمكن للمرضى تحملها بأمان. تلقى جميع المرضى جيمسيتابين وريديًا في اليومين 1 و8 من دورة مدتها ثلاثة أسابيع، تلاها حبوب سيلينيكسور أسبوعيًا. راقبت الفريق بعناية الآثار الجانبية الشديدة في دورات العلاج الأولى لتقرير الجرعة الموصى بها للدراسات المستقبلية.
السلامة والآثار الجانبية والفوائد المبكرة
كانت أكبر الآثار الجانبية انخفاضات في خلايا الدم — خاصة خلايا الدم البيضاء والصفائح الدموية — وهي شائعة مع العلاج الكيميائي. كانت هذه الانخفاضات متكررة لكنها عمومًا قابلة للإدارة باستخدام حقن محفزات نمو الخلايا وضبط الجرعات وتأجيل العلاج. كما كانت الغثيان والقيء والتعب شائعة لكنها في الغالب خفيفة إلى متوسطة، ولم يضطر أي مريض إلى ترك الدراسة بسبب السمية. أبقت الجرعة الموصى بها النهائية الجيمسيتابين عند مستوى نسبيًا مرتفع بينما استخدمت جرعة سيلينيكسور الأسبوعية أقل قليلًا لتحسين التحمل. من بين 16 مريضًا أمكن قياس أورامهم، شهد خمسة انكماشًا واضحًا للأورام وحقق خمسة آخرون مرضًا مستقرًا، ما أدى إلى معدل استجابة إجمالي يقارب 31 بالمئة. لكامل المجموعة، ظل السرطان تحت السيطرة بوسيط يقارب 5 إلى 6 أشهر. أظهر مرضى الليوميو ساركوما أداءً جيدًا بشكل خاص، حيث استمر كبح المرض نحو 8 أشهر في المتوسط وبلغ البقاء الكلي قرابة ثلاث سنوات وربع السنة، رغم أن صغر عدد المرضى يعني وجوب تفسير هذه النتائج بحذر.
دلالات لمن قد يستفيد أكثر
لأن ليس كل المرضى استجابوا، بحث الباحثون عن مؤشرات في عينات الأورام قد تتنبأ بالفائدة. رُبطت المستويات العالية من السيرفيفين والتلوين النووي القوي لـ IκBα بفترات أقصر قبل تقدم السرطان، لا سيما في الليوميو ساركوما. يتوافق هذا مع نتيجة المختبر التي تشير إلى أن الفقدان الكامل للسيرفيفين مرتبط بتآزر أقوى بين الدوائين. إذا أكدت دراسات أكبر هذه النتائج، فقد تساعد هذه البروتينات الأطباء على تحديد المرضى الأكثر احتمالًا للاستجابة لتركيبة جيمسيتابين–سيلينيكسور ومن قد يحتاجون إلى استراتيجيات مختلفة.
ماذا يعني هذا لمرضى الساركومة
بالنسبة للأشخاص المصابين بساركومات متقدمة، الخيارات العلاجية محدودة وغالبًا ما تكون فعالة لفترة وجيزة فقط. تظهر هذه الدراسة المبكرة أن إقران جيمسيتابين مع سيلينيكسور ممكن، وأن الآثار الجانبية قابلة للتعامل مع الدعم الدقيق، وتوفر إشارات مشجعة للفائدة، خصوصًا في الليوميو ساركوما. كما يبدأ هذا العمل في الكشف عن علامات حيوية قد توجه رعاية أكثر تخصيصًا. تُجري الآن تجارب أكبر من المرحلتين الثانية والثالثة لتأكيد ما إن كانت هذه التركيبة تحسّن البقاء وجودة الحياة فعلًا، لكن بالنسبة للمرضى والأطباء، فهي تمثل مسارًا جديدًا واقعيًا في البحث عن علاجات أفضل للساركومة.
الاستشهاد: Martin-Broto, J., Casado, A., Marquina, G. et al. Gemcitabine plus selinexor in selective advanced sarcomas: a phase I of the Spanish group for research on sarcoma study. Nat Commun 17, 1873 (2026). https://doi.org/10.1038/s41467-026-68729-1
الكلمات المفتاحية: علاج الساركومة, ليوميو ساركوما, جيمسيتابين, سيلينيكسور, تجربة سريرية للسرطان