Clear Sky Science · ar
يمكن لعدّ الخلايا أن يتنبأ بدقة بمقاييس النشاط البيولوجي للجزيئات الصغيرة
لماذا يهم عدّ الخلايا ببساطة
عندما تختبر شركات الأدوية آلاف المركبات، تعتمد أكثر فأكثر على الذكاء الاصطناعي للتنبؤ بأيها سيفيد المرضى وأيها قد يكون ضارًا. تكشف هذه الدراسة نقطة مفاجئة: في العديد من مجموعات الاختبار الشائعة، يكفي أحيانًا عدّ عدد الخلايا الحية المتبقية بعد المعالجة للتنبؤ بالنتيجة تقريبًا بمستوى مماثل لطرق أكثر تعقيدًا. يعني ذلك أن بعض النجاحات المثيرة للانتباه المدعاة للذكاء الاصطناعي قد تكون في الواقع إعادة اكتشاف إشارة أساسية جدًا: هل الخلايا تموت أم لا؟
اختبارات الأدوية الحديثة والتصوير الذكي
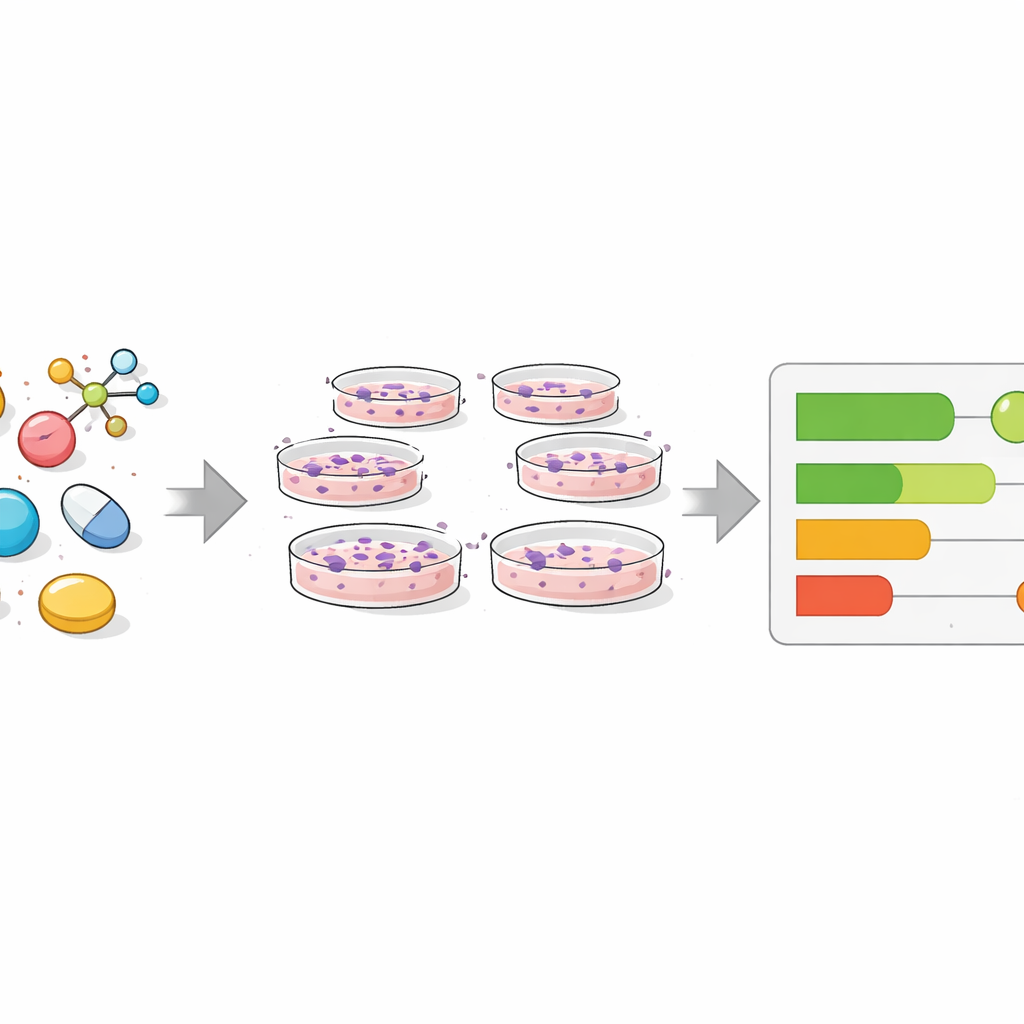
لإيجاد أدوية جديدة، يزرع الباحثون خلايا بشرية في أطباق ويعرضونها لمركبات كيميائية، ثم يقيسون استجابة الخلايا. تقليديًا، اعتمدت النماذج الحاسوبية على هياكل الجزيئات، لكن هذا النهج غالبًا ما يقصر عندما تتصرف مركبات متشابهة المظهر بشكل مختلف. تستخدم أساليب أحدث «الملف الظاهري الفينوتيبي»، حيث تُصبغ الخلايا بأصباغ فلورية وتُصوَّر. طريقة شائعة تسمى Cell Painting تخلق صورًا غنية لشكل الخلية وبنيتها وتنظيمها الداخلي. من هذه الصور يستخلص الحاسوب آلاف الميزات الرقمية التي يمكن إدخالها في نماذج التعلم الآلي جنبًا إلى جنب مع بيانات أخرى مثل نشاط الجينات.
إشارة بسيطة مخبأة في وضح النهار
أعاد المؤلفون فحص عدة مجموعات معيارية مؤثرة يستخدمها كثيرون لاختبار تقنيات التعلم الآلي الجديدة. تحتوي هذه المجموعات على نتائج من مئات الاختبارات البيولوجية، بما في ذلك فحوصات السمية وقياسات ما إذا كانت المركبات تصيب أهداف بروتينية محددة. من خلال التركيز على ميزة واحدة من صور Cell Painting — عدد الخلايا المتبقية في كل بؤرة — تساءلوا إلى أي مدى يمكن لمقياس بسيط واحد أن يتنبأ بما إذا تم وسم مركب بأنه «نشط» أو «غير نشط» في كل اختبار. وجدوا أنه في جزء كبير من الاختبارات، لا سيما تلك المتعلقة بنمو الخلايا السرطانية أو صحة الخلايا عامة، تميل المركبات النشطة إلى تقليل عدد الخلايا بشدة، بينما لا تفعل المركبات غير النشطة ذلك. في هذه الحالات، طابقت نموذج بسيط يعتمد فقط على عدّ الخلايا أداء شبكات عصبية متقدمة مدربة على آلاف ميزات الصور أو على ملفات التعبير الجيني، أو اقتربت منه.
متى يتنكر موت الخلايا في صورة بصيرة
من خلال تحليل أعمق، أظهر الفريق أن المركبات الموصوفة بالنشطة عبر اختبارات مختلفة غالبًا ما تشترك في سمة واحدة: إنها تضر الخلايا على نطاق واسع. ربطت بيانات نشاط الجينات هذه المواد الكيميائية بمسارات الإجهاد وموت الخلايا مثل الاستماتة، مما يشير إلى أن السمية العامة، وليس تأثيرًا دوائيًا دقيقًا، كانت غالبًا ما تحرك الإشارات التي تتعلمها النماذج. كما أظهروا أن بعض الطرق «متقدمة» المزعومة، بما في ذلك التعلم التبايني عبر الصور والهياكل الكيميائية والأساليب المتقدمة في التعلم المعدل، لم تتفوق بوضوح على معيار عدّ الخلايا في هذه المجموعات التي تهيمن عليها قابلية البقاء. في بعض الاختبارات، كان عكس مخرجات النموذج ببساطة — لأن الوسوم عرّفت بطريقة غير اعتيادية — كافيًا لمطابقة الأداء المبلغ عنه لأنظمة التعلم القليل العينات المعقدة.
أين يساعد التصوير الغني حقًا
من المهم أن الدراسة لا تدّعي أن عدّ الخلايا هو كل ما يهم. عندما جمع المؤلفون مجموعة معيارية مُصفّاة بعناية تركز على 24 هدفًا بروتينيًا محددًا جيدًا، وأزالوا الاختبارات شديدة السمية والمربكة، تفوّقّت النماذج التي استخدمت ملفات Cell Painting الكاملة بوضوح على تلك القائمة على عدّ الخلايا فقط. التغيرات المورفولوجية الدقيقة المتعلقة بنسيج وتوزيع هياكل الخلية، مثل الشبكة الإندوبلازمية والميتوكوندريا، التقطت بيولوجيا حقيقية لا يمكن اختزالها إلى مجرد فقدان خلايا. في تجارب الاستجابة للجرعة، ظهرت تغييرات شكلية مفصّلة عند تراكيز كيميائية أقل من تلك التي سببت موتًا واضحًا للخلايا، مما يبيّن أن بيانات الصور الغنية يمكنها كشف تأثيرات مبكرة ومحددة الآلية التي يفشل عدّ الخلايا الخام في كشفها.
كيف نبني اختبارات أفضل لنماذج أذكى
من هذه النتائج، يقدم المؤلفون إرشادات عملية لمجتمع اكتشاف الأدوية. ينبغي فحص مجموعات المعايير وتقليصها بحيث لا تهيمن عليها اختبارات تعكس أساسًا ما إذا كانت الخلايا حية أم ميتة. يجادلون أنه يجب أن يتضمن كل دراسة نموذجًا أساسيًا بسيطًا قائمًا على عدّ الخلايا، حتى يمكن تقييم أي تحسّن مدّعى من طرق أكثر تطورًا مقابل أبسط تفسير ممكن. كما يوصون باستخدام مقاييس مقاومة لعدم توازن البيانات، وضمان وجود أمثلة كافية نشطة وغير نشطة في مجموعات الاختبار، والنظر دائمًا في السياق البيولوجي لكل اختبار.
ما يعنيه هذا لمستقبل اكتشاف الأدوية
لغير المتخصصين، الرسالة الأساسية مطمئنة لكنها مقلقة: قد تكون بعض الأرقام المثيرة للانطباع المبلّغ عنها للذكاء الاصطناعي في اكتشاف الأدوية ناتجة عن تعلم اختصارات سهلة أكثر من بصيرة بيولوجية عميقة. من خلال الكشف عن مدى ما يمكن أن يحققه مقياس بسيط مثل عدّ الخلايا، يساعد هذا العمل في إعادة ضبط التوقعات ويشجع على مقارنات أكثر نزاهة بين النماذج. في الوقت نفسه، يبرز المكان الذي تضيف فيه تقنيات التصوير المتقدمة والتعلم الآلي قيمة حقيقية — كشف تغيرات دقيقة ومحددة في الخلايا لا تستطيع قراءات النجاة أو الموت البسيطة رصدها. على المدى الطويل، ينبغي أن تساعد مجموعات معيارية مصممة بعناية أفضل في ضمان أن تتحرك الأدوات الحاسوبية إلى ما هو أبعد من عدّ الضحايا نحو فهم حقيقي لكيفية عمل الأدوية المحتملة.
الاستشهاد: Seal, S., Dee, W., Shah, A. et al. Counting cells can accurately predict small-molecule bioactivity benchmarks. Nat Commun 17, 2436 (2026). https://doi.org/10.1038/s41467-026-68725-5
الكلمات المفتاحية: بقاء الخلايا, الملف الظاهري الفينوتيبي, طَلاء الخلايا (Cell Painting), اكتشاف الأدوية, معايير التعلم الآلي