Clear Sky Science · ar
تحديد تراكم الجزيئات في الإشريكية القولونية باستخدام تفاعل النقرة
لماذا تكافح الأدوية الصغيرة للوصول إلى البكتيريا الخطيرة
تعتمد الطب الحديث على المضادات الحيوية، ومع ذلك أصبحت بعض أخطر البكتيريا الآن محمية بجدران خارجية قوية تمنع دخول العديد من الأدوية. تمتلك البكتيريا سالبة الغرام مثل الإشريكية القولونية حاجز غشاء خارجي فعالاً بشكل خاص، مما يصعّب تصميم أدوية تدخل الخلية وتصل إلى أهدافها. يقدم هذا البحث اختباراً مخبرياً جديداً يُدعى اختبار CHAMP يسمح للعلماء بقياس مدى قدرة آلاف الجزيئات الصغيرة على تجاوز هذه الدفاعات والتراكم داخل خلايا الإشريكية القولونية الحية بسرعة.
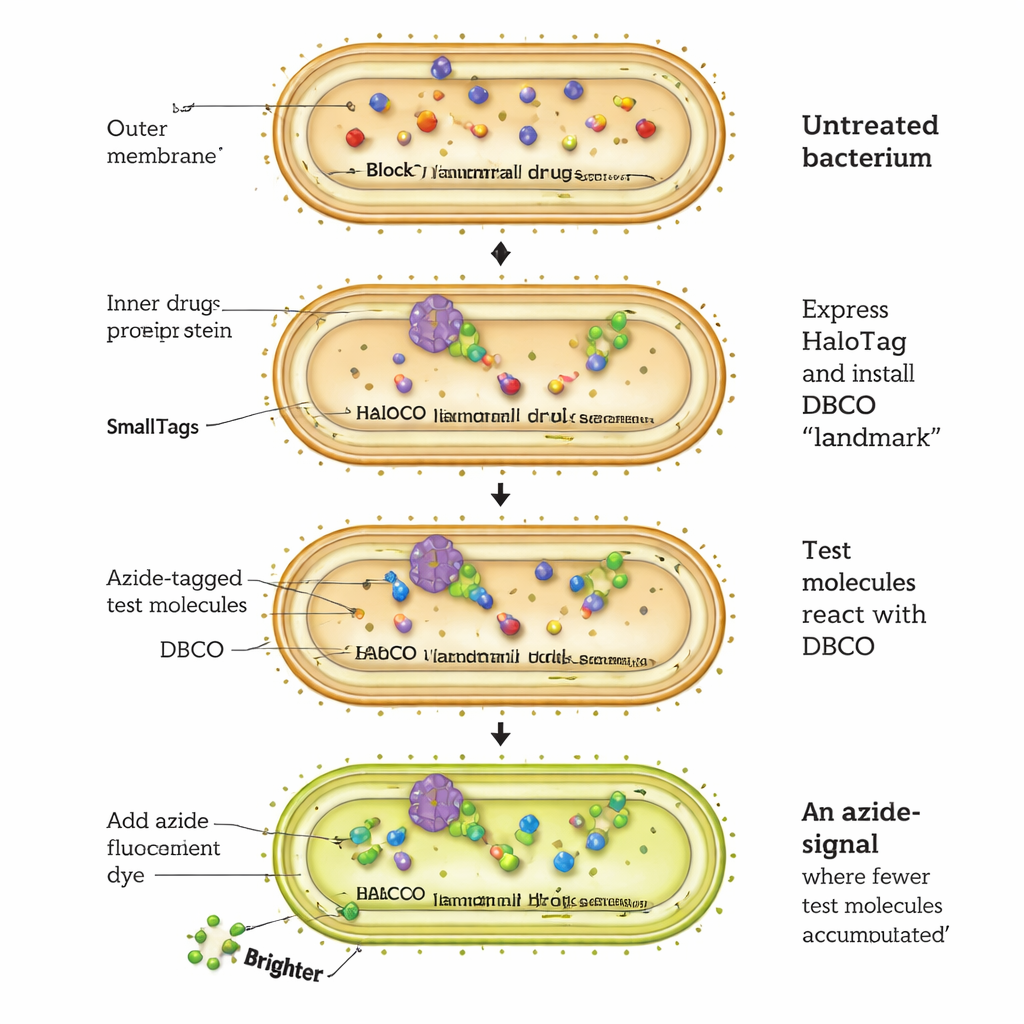
طريقة جديدة لمراقبة دخول الدواء إلى الخلايا البكتيرية
اعتمد اكتشاف المضادات الحيوية التقليدي على مركبات طبيعية واختبارات نمو بسيطة لمعرفة ما إذا كانت البكتيريا تبقى حية أو تموت. تلك الاختبارات لا تكشف عن كمية الدواء التي دخلت الخلية فعلاً، ولا عن مصيره داخلها. هدف المؤلفون كان بناء طريقة مباشرة وقابلة للتطبيق على نطاق واسع لتتبع دخول الدواء إلى السيتوسول البكتيري — السائل الداخلي حيث توجد العديد من أهداف المضادات الحيوية. سعوا لتجاوز مقاييس خام مثل الحد الأدنى للتركيز المثبط التي تخلط بين تأثيرات امتصاص الدواء وربطه بالهدف والآثار البيولوجية اللاحقة، والحصول بدلاً من ذلك على قياس نقي للتراكم داخل الخلية.
تحويل البكتيريا إلى مسجلات كيميائية صغيرة
يعمل اختبار CHAMP عن طريق إعادة توجيه بروتين بكتيري يسمى HaloTag ليصبح بمثابة منصة استقبال جزيئية. تُهندس خلايا الإشريكية القولونية لإنتاج HaloTag في السيتوسول الخاص بها. يربط الباحثون أولاً مقبضاً كيميائياً خاصاً، ألكين مقوس يُسمى DBCO، بـ HaloTag عبر رابط كلوروألكان قصير. بعد ذلك، يعرضون البكتيريا لجزيئات اختبار كل منها يحمل وسم أزيد صغير جداً. فقط تلك الجزيئات التي تعبر الغشاء الخارجي وتخترق الغشاء الداخلي وتصل إلى السيتوسول يمكنها التفاعل مع مقبض DBCO في تفاعل "نقرة" انتقائي للغاية، مما يعلّم HaloTag بشكل دائم. أخيراً، تُعالج الخلايا بصبغة فلورية مؤشَّدة بالأزيد يمكنها الارتباط فقط بأي DBCO غير مشغول. كلما كانت الإشارة الفلورية أكثر سطوعاً، قل عدد جزيئات الاختبار التي وصلت إلى السيتوسول؛ والخلايا الأضعف ضياءً تشير إلى تراكم أفضل.
استكشاف كيف تشكل الكيمياء والبيولوجيا دخول الدواء
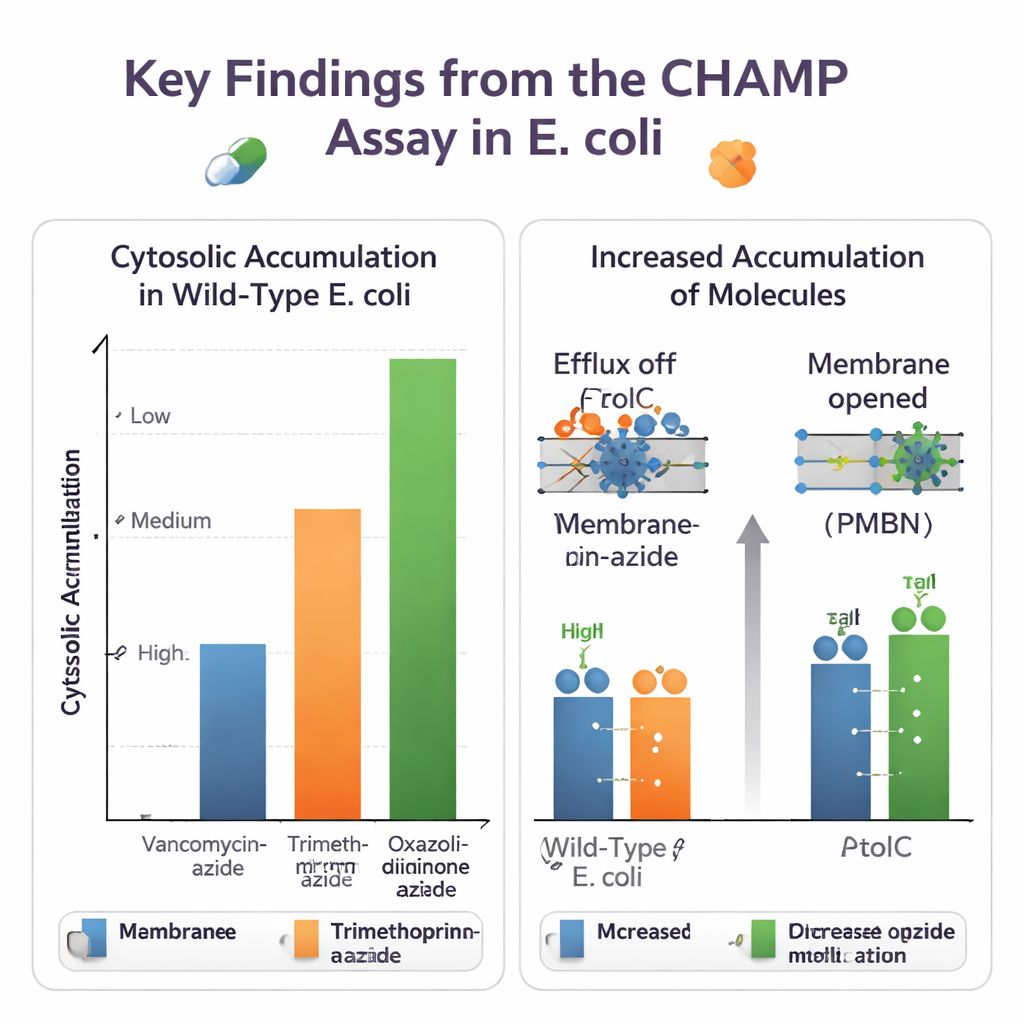
باستخدام CHAMP، قام الفريق أولاً بضبط تعبير HaloTag، وكمية مرسى DBCO، واختيار الأصباغ الفلورية للحصول على نافذة إشارة كبيرة وموثوقة. ثم استخدموا مجموعات من الجزيئات الصغيرة القريبة لرؤية كيف تؤثر التعديلات الكيميائية على الدخول. تحويل الأحماض الكربوكسيلية إلى أميدات، وإضافة أو إزالة مجموعات أمينية قاعدية، يمكن أن يغير مستويات السيتوسول بشكل ملحوظ. في كثير من الحالات عززت الأمينات الأولية التراكم، مما يتوافق مع قواعد "eNTRy" المستقلة التي طورتها مجموعات أخرى. تعامل الاختبار أيضاً مع نسخ مؤشرة بالأزيد من مضادات حقيقية، كاشفاً فروقاً كبيرة: أدوية ضخمة مثل فانكوميسين بالكاد وصلت إلى السيتوسول، بينما دخلت مضادات أصغر مثل مشتقات التريميثوبريم وبعض الأوكسازوليدينونات بسهولة أكبر.
كشف دفاعات بكتيرية تطرد الدواء إلى الخارج
لأن الطريقة تعمل في بكتيريا حية قابلة للبرمجة جينياً، يمكنها فصل أدوار دفاعات خلوية مختلفة. قارن المؤلفون الإشريكية القولونية الطبيعية بسلالات تفتقد TolC، وهو مكوّن رئيسي لمضخة طرد متعددة الأدوية، أو بخلايا عُولجت بمثبط صغير لجزيء TolC. بالنسبة للنوبيوسين وعدد من المضادات المؤشرة بالأزيد الأخرى، أظهر CHAMP تراكمًا سيتوسولياً أعلى بوضوح عندما تعطّل TolC، مؤكداً أن هذه المركبات هي ركائز للطرد. كما اختبروا طرقاً لتفكيك حاجز الغشاء الخارجي، إما كيميائياً بواسطة الببتيد PMBN أو جينياً عبر فرط التعبير لقناة بورين واسعة مفتوحة. أظهرت العديد من الجزيئات التي تراكمت سابقاً بشكل ضعيف زيادات كبيرة عند تسبيب نفاذية الغشاء، ما يسلط الضوء على كيفية تعاون الدخول والطرد لتحديد مستويات الدواء الداخلية.
التوسع ليشمل آلاف الجزيئات لاستخلاص أنماط وقواعد
لإظهار قدرة الحقاقة العالية الحقيقية، فحص الباحثون مجموعة تجارية مكونة من 404 مركبات مؤشرة بالأزيد ومكتبة مخصصة تضم 1,152 جزيئاً حاملاً للأزيد. قاسوا التراكم في عدة سياقات بكتيرية، بما في ذلك الخلايا غير المعالجة، والخلايا المعالجة بـ PMBN، والخلايا فائقة النفاذية، والخلايا فائقة النفاذية الخالية من TolC. بمقارنة نفس الجزيء عبر هذه الظروف، تمكنوا من تحديد التغييرات الناتجة عن البيولوجيا الخلوية بدلاً من خصائص سرعة تفاعل النقرة. وبالربط بين بيانات CHAMP والتحليل الحاسوبي، ربطوا ميزات فيزيائية‑كيميائية معينة — مثل مساحة السطح القطبية، وقدرة ربط الروابط الهيدروجينية، وهياكل حلقية محددة — بالتعرّف الأقوى بواسطة طرد يعتمد على TolC. يبدأ هذا النوع من التحليل واسع النطاق في رسم قواعد تصميم لجزيئات إما تتجنب المضخات أو تستغل البورينات بشكل أكثر فعالية.
ما يعنيه هذا للمضادات الحيوية المستقبلية
بعبارات بسيطة، يحول هذا العمل الإشريكية القولونية إلى حساس عالي الإنتاج يبلغ بدقة عن كمية المركب المختبرية التي تدخل الجزء من الخلية حيث توجد العديد من أهداف الدواء. لا يحل CHAMP محل اختبارات ما إذا كانت البكتيريا تُقتل، لكنه يملأ فجوة حاسمة بفصل "دخول المركب" عن "إحداث الضرر". مع القدرة على قياس أكثر من ألف جزيء في سلالات معدلة جينياً أو كيميائياً خلال أيام، يمكن للباحثين الآن تعلم أي الميزات الكيميائية تعزز الدخول، تقلل الطرد، أو تستفيد من شركاء يخلخلون الغشاء بشكل منهجي. من المفترض أن تُسرّع هذه المعرفة تصميم مضادات حيوية جديدة ومواد مساعدة قادرة على اختراق دفاعات ممرضات سالبة الغرام الشرسة قبل أن تزداد مقاومة ترسانة المضادات الحيوية.
الاستشهاد: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
الكلمات المفتاحية: مقاومة المضادات الحيوية, الإشريكية القولونية, نفاذية الدواء, مضخات الطرد, كيمياء النقرة