Clear Sky Science · ar
الانتقال الجغرافي لمقاومة المضادات الحيوية نتيجة التوزيع الجماعي للأزيثروميسين
لماذا هذا يهم لصحة الأطفال
يُستخدم الأزيثروميسين، وهو مضاد حيوي شائع، في حملات دوائية جماعية لإنقاذ حياة الأطفال الصغار في أجزاء من أفريقيا جنوب الصحراء، بما في ذلك النيجر. أدت هذه الحملات إلى خفض وفيات الأطفال لكنها أثارت قلقًا مهمًا: هل قد تُسهم أيضًا في انتشار بكتيريا مقاومة للأدوية من القرى المعالجة إلى مجتمعات مجاورة لم تتلق الدواء؟ تبحث هذه الدراسة فيما إذا كان هناك "تسرب" لمقاومة المضادات الحيوية بين القرى، وهو سؤال أساسي للدول التي تزن فوائد ومخاطر توسيع هذه البرامج.
حملات منقذة للحياة ومخاطرها الخفية
أظهرت تجارب واسعة سابقة أن إعطاء الأزيثروميسين مرتين في السنة لجميع الأطفال الصغار في مناطق ذات معدل وفيات مرتفع يقلل الوفيات بنحو 14–18 بالمئة. دفعت هذه النتيجة منظمة الصحة العالمية وحكومات مثل حكومة النيجر إلى التفكير في توسيع استخدام هذه الاستراتيجية. ومع ذلك، لا تقتصر آثار المضادات الحيوية على قتل البكتيريا الضارة فحسب؛ بل تُفضّل أيضًا بقاء السلالات التي تطورت مقاومة لها. في أعمال سابقة، رصدت نفس مجموعة الباحثين علامات واضحة لبكتيريا مقاومة للأزيثروميسين لدى الأطفال المعالجين. وما لم يكن واضحًا هو ما إذا كانت هذه الميكروبات المقاومة تبقى محصورة في القرى المعالجة أم تنتقل إلى الخارج، مما يضعف فعالية المضادات الحيوية للآخرين.
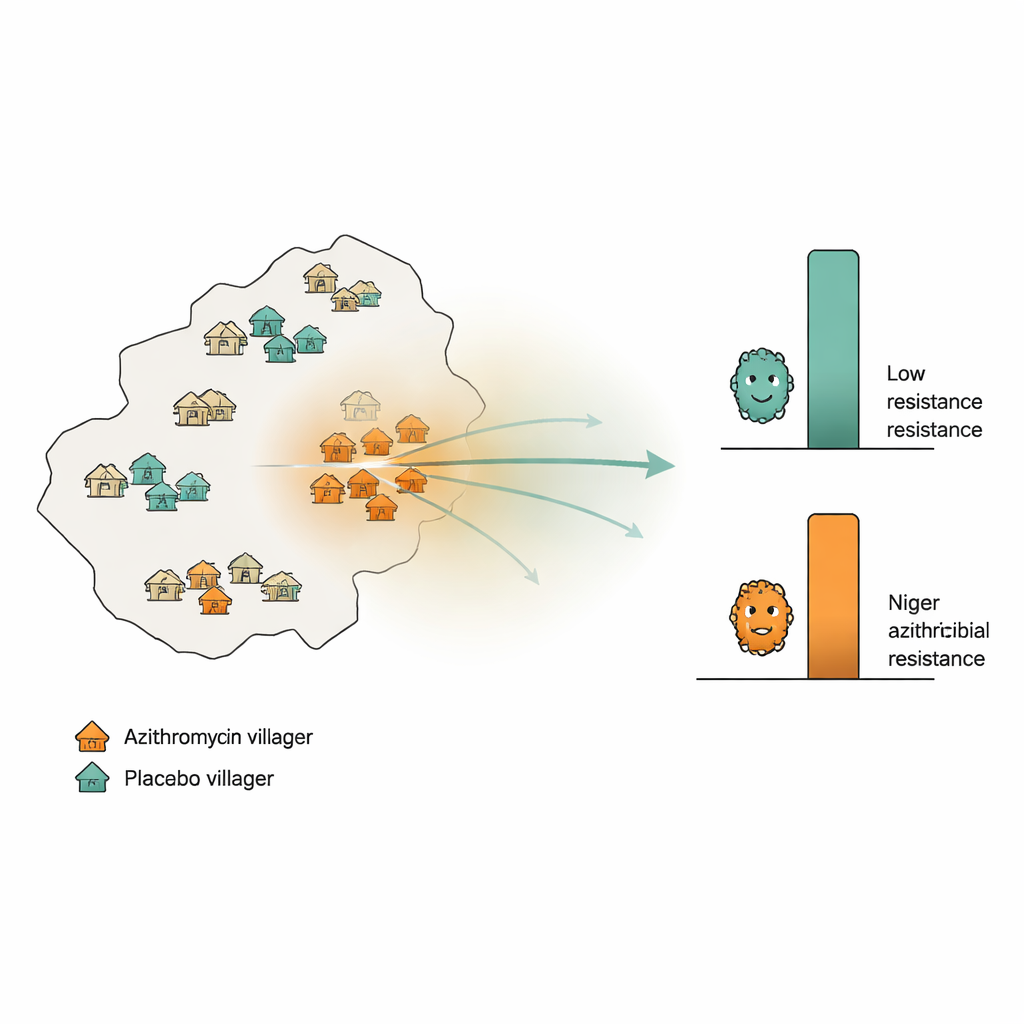
تتبع المقاومة عبر المشهد الريفي
استفاد الباحثون من تجربة كبرى لنجاة الأطفال في منطقة دوسّو بالنيجر، حيث تم توزيع 594 قرية عشوائيًا لتلقي الأزيثروميسين أو دواء وهمي غير نشط مرتين سنويًا لمدة عامين. بالإضافة إلى ذلك، أُختيرت 30 قرية "مراقبة" بشكل عشوائي: تلقت نصفها أزيثروميسين والنصف الآخر دواء وهميًا. من هذه القرى المراقبة، جمعت الفريق مسحات شرجية من 10 أطفال في كل قرية عند بداية التجربة ومرة أخرى بعد 24 شهرًا. باستخدام تسلسل الحمض النووي العميق، قاسوا متوسط عدد الجينات المرتبطة بمقاومة مضادات الماكروليد (الفئة التي تشمل الأزيثروميسين) في كل قرية. كما حسبوا، لكل قرية مراقبة، مدى شدة استخدام الأزيثروميسين في المنطقة المحيطة — عبر عد كل الجرعات المعطاة في القرى المجاورة وإعطاء وزن أكبر للقرى الأقرب.
البحث عن علامات انتشار بين القرى
إذا كانت المقاومة تنتشر جغرافيًا، توقع الباحثون رؤية مستويات أعلى من جينات المقاومة في القرى التي تلقت دواء وهميًا ولكنها محاطة بجيران عولجوا بكثافة، مقارنة بقرى الدواء الوهمي في مناطق استخدم فيها الأزيثروميسين قليلًا. اختبروا هذه الفكرة بعدة طرق: عبر فحص ارتباطات بسيطة مرتبة بين شدة المعالجة المحيطة والمقاومة؛ وإعادة التحليل عبر نطاقات مسافة مختلفة (ضمن 10 أو 20 أو 30 كيلومترًا)؛ وباستخدام استراتيجية تبديل صارمة أُجريت من خلال خلط ملصقات العلاج في التجربة الأكبر لرؤية ما إذا كانت أي أنماط ظاهرة قد تنتج عن المصادفة. كما أجروا تحليلًا "لضبط سلبي" كرر نفس الحسابات باستخدام جرعات الدواء الوهمي بدل جرعات الأزيثروميسين؛ إذ إن وجود نمط مماثل هناك قد يشير إلى وجود متغيرات مربكة بدل تسرب حقيقي.
ما كشفت عنه البيانات عن المقاومة
عبر كل هذه الاختبارات، أظهرت قرى الدواء الوهمي مستويات منخفضة من جينات مقاومة الماكروليد ظلت قريبة من مستوياتها الأساسية، بغض النظر عن مقدار استخدام الأزيثروميسين حولها. لم تكشف الاختبارات الإحصائية عن رابط ذي دلالة بين استخدام الدواء المحيط والمقاومة في هذه المجتمعات غير المعالجة. بالمقابل، أظهرت القرى التي عولج أطفالها بالأزيثروميسين ارتفاعًا ملحوظًا في جينات المقاومة خلال فترة العامين، وهو ما يتوافق مع الانتقاء المباشر الناتج عن العلاج — لكن هذا الارتفاع لم يزد بخلاف منهجي في المناطق التي كان فيها الاستخدام المحيط أعلى. وعند فحص البكتيريا الرئوية الحية من أنوف الأطفال، لم يُلاحظ أيضًا أي ارتباط بين كثافة المعالجة الجغرافية والمقاومة. وبلغت الاستنتاجات ذاتها عند إعادة التحليل باستخدام نماذج رياضية مختلفة وتعريفات بديلة لشدة المعالجة.
الحدود، التحفظات، والصورة الأوسع
لا تستطيع الدراسة استبعاد وجود تأثيرات تسرب صغيرة تمامًا، لا سيما بالنظر إلى أن 30 قرية مراقبة فقط خضعت لاختبارات مكثفة، ولم تفحص الانتشار على نطاق دقيق جدًا داخل الأسر أو داخل القرية الواحدة. كما تفترض أن المسافة وعدد الجرعات هما المحركان الرئيسيان لأي انتشار، وتركز على نافذة زمنية مدتها عامان؛ قد تُظهر الفترات الأطول أو تصاميم برامج مختلفة، مثل تلك التي تعالج مجتمعات بأكملها لمرض يُصيب العين، أنماطًا أخرى. ومع ذلك، تشير الأدلة إلى أنه في هذا السياق، يتركز معظم ضغط المقاومة الناتج عن حملات الأزيثروميسين الجماعية داخل المجتمعات التي تتلقى الدواء فعليًا، بدلاً من الانتشار الصامت عبر المشهد.
ماذا يعني هذا لحملات المضادات الحيوية المستقبلية
بالنسبة للمسؤولين الصحيين في دول مثل النيجر، تقدم هذه النتائج طمأنة متأنية. فبينما تزيد العلاجات الجماعية بالأزيثروميسين من مقاومة المضادات الحيوية داخل القرى المعالجة، لم يجد هذه الدراسة دلائل قوية على تسرب تلك المقاومة إلى القرى المجاورة غير المعالجة على مدى 24 شهرًا. يعني ذلك أن تقديرات المخاطر المترتبة على المقاومة من هذه التجارب المتعلقة بإنقاذ الأطفال من غير المرجح أن تكون مشوشة بشدة بسبب تسرب جغرافي غير معروف. ومع ذلك، لا بد لصانعي السياسات من موازنة الفوائد المنقذة للحياة لهذه الحملات مع الارتفاع المحلي في المقاومة، لكنهم يستطيعون القيام بذلك بثقة أكبر بأن المشكلة، على الأقل على المدى المتوسط وعلى مستوى قرية إلى قرية، لا تنتشر بسرعة إلى الخارج.
الاستشهاد: Srivathsan, A., Arzika, A.M., Maliki, R. et al. Geographic spillover of antimicrobial resistance from mass distribution of azithromycin. Nat Commun 17, 2152 (2026). https://doi.org/10.1038/s41467-026-68691-y
الكلمات المفتاحية: مقاومة المضادات الحيوية, الأزيثروميسين, التوزيع الدوائي الجماعي, وفيات الأطفال, النيجر