Clear Sky Science · ar
رؤى وظيفية وبُنيَة حول التداخلات بين β-أريستين 1 وGαs أو Gαi1
لماذا هذا مهم للصحة والطب
تعمل كثير من الأدوية الحالية، من أقراص الحساسية إلى أدوية القلب والعلاجات النفسية، عبر استهداف عائلة كبيرة من بروتينات سطح الخلية تُسمى مستقبلات مقترنة ببروتين G (GPCRs). تنقل هذه المستقبلات الرسائل إلى داخل الخلية بمساعدة عنصرين رئيسيين، بروتينات G وبروتينات تُدعى بيتا-أريستينات. تدرس هذه الدراسة كيف يتواصل أحد بروتينات بيتا-أريستين (بيتا-أريستين 1) مباشرة مع نوعين من بروتينات G داخل الخلية. فهم هذه المحادثة المخفية قد يساعد العلماء على تصميم أدوية أكثر دقة وأقل آثارًا جانبية عن طريق ضبط كيفية تدفق الإشارات داخل خلايانا.
رسّالان رئيسيان داخل خلايانا
عندما يرتبط هرمون أو دواء بمستقبل GPCR على سطح الخلية، فإنه يطلق مسارين عامين للتواصل. يستخدم أحد المسارين بروتينات G، التي تعمل كمؤقتات جزيئية تشغل وتطفئ عبر مبادلة سوى كيميائي صغير (GDP) بآخر (GTP). والمسار الآخر يستخدم بيتا-أريستينات، التي يمكنها كلٌّ من إيقاف إشارات بروتين G وبدء مسارات إشارية خاصة بها. لفترة طويلة، ركز العلماء أساسًا على كيفية تواصل المستقبلات منفصلة مع بروتينات G أو مع بيتا-أريستينات. أشارت أعمال أحدث إلى أن بروتينات G وبيتا-أريستينات قد ترتبطان ببعضهما البعض أو تشكلان حتى «مجاميع ضخمة» مع المستقبل. لكن تفاصيل كيفية ارتباط هذه البروتينات وما يعنيه ذلك للإشارة ظلت غير واضحة.
قياس من يرتبط بمن
ركزت هذه الدراسة على بيتا-أريستين 1 واثنين من وحدات «ألفا» الفرعية لبروتينات G: Gαs، الذي عادةً ينشط نشاط الخلية، وGαi1، الذي يُثبّط النشاط عمومًا. باستخدام تقنية قياس ارتباط حساسة، اختبر الباحثون مدى قوة التلاصق بين بيتا-أريستين 1 المنقى وكلٍ من بروتينات G تحت ظروف مختلفة. وجدوا أن العامل الحاسم ليس ما إذا كان بروتين G في حالة "تشغيل" أو "إيقاف"، بل ما إذا كان بيتا-أريستين 1 في شكل أكثر نشاطًا ومرونة. نسخة من بيتا-أريستين 1 مفقودة الذيل — والتي تتصرف كمجموعة أشكال مرنة ونشيطة — ارتبطت بقوة بكلٍ من Gαs وGαi1. في المقابل، الشكل الساكن لبيتا-أريستين 1، أو شكل مُقفل بواسطة ببتيد شبيه بذيل المستقبل، ارتبط بصورة ضعيفة أو لم يرتبط على الإطلاق. وهذا يقترح أن بروتينات G تميز بيتا-أريستين 1 عندما يجرب أشكالًا تشبه الشكل النشط الذي قد يظهر بعد تنشيط المستقبل. 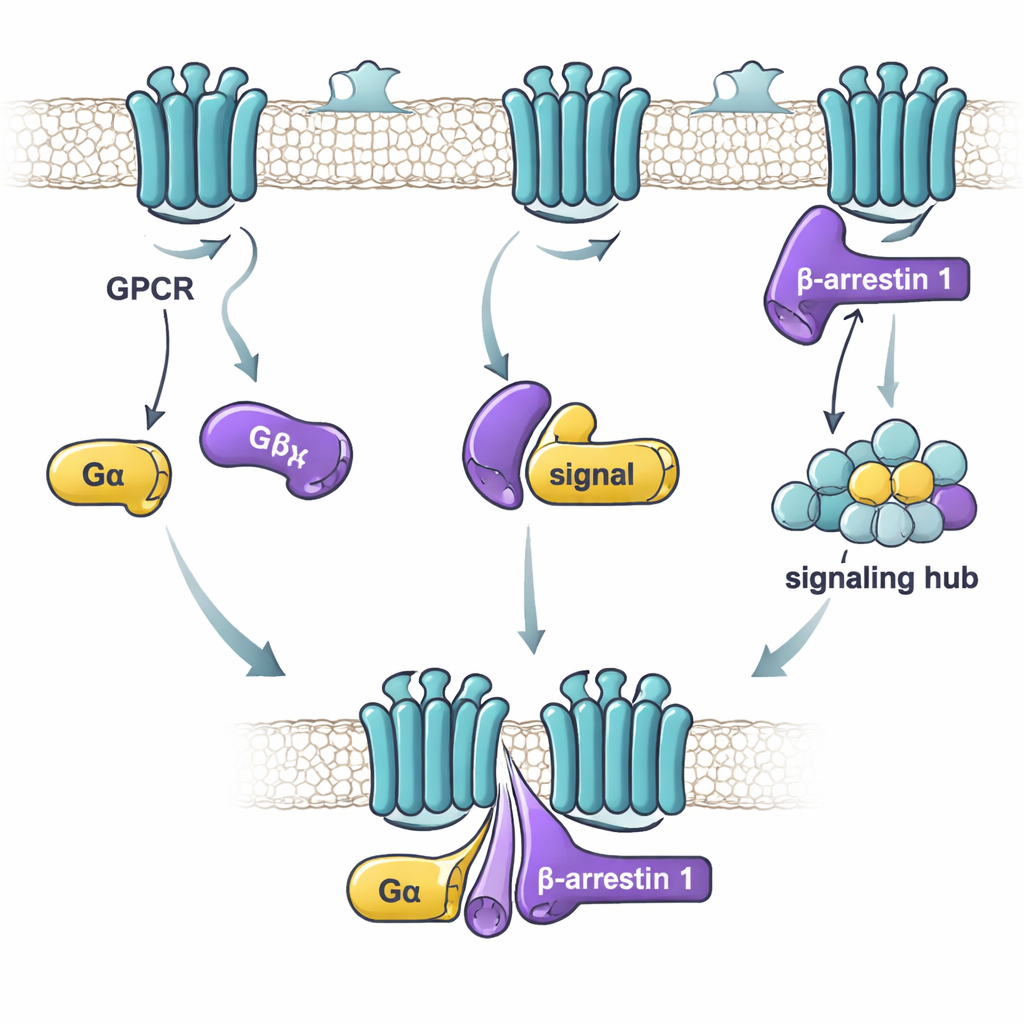
مراقبة تغيّرات شكل دقيقة
لرؤية كيف يؤثر الارتباط على شكل البروتين، استخدمت المجموعة طريقة تتتبع مدى سرعة تبادل ذرات الهيدروجين على العمود الفقري للبروتين مع هيدروجين أثقل من المذيب. التبادل البطيء عادةً يعني أن المنطقة أصبحت أكثر محمية أو أكثر صلابة؛ والتبادل الأسرع يعني أنها أصبحت أكثر مرونة أو تعرضًا. عندما ارتبط شظية بيتا-أريستين 1 الشبيهة بالشكل النشط بـGαs أو Gαi1، أظهرت كلا بروتينَي G أنماطًا واضحة من التغير في عدة مناطق، مما يدل على أنهما يعيدان تشكيل بنيتهما حول المركب. بالمقابل، تغير بيتا-أريستين 1 نفسه بشكل طفيف فقط، أساسًا في الحلقات المرنة. عبر العمل بمناطق معزولة من بروتينات G، أظهر الباحثون أيضًا أن كلًا من الجزء الكاتاليني الرئيسي "الشبيه بـRas" والجزء المحاط الحلزوني ألفا يساهمان في الارتباط. بالنسبة لـGαs، يلعب الجزء الحلزوني دورًا قويًا بشكل خاص؛ أما بالنسبة لـGαi1، فكلا الجزئين لهما أهمية متقاربة تقريبًا.
وظيفة دون قلب المفتاح الرئيسي
كان السؤال التالي عمّا إذا كان هذا الاتصال المباشر يغير كيفية تشغيل بروتينات G. استخدمت المجموعة مسبارًا فلوريسنتيًا يحاكي GTP ويتوهج عندما ينتقل بروتين G من GDP إلى GTP، وهو قراءة معيارية للتنشيط. بشكل مفاجئ، إضافة بيتا-أريستين 1 لم تغير سرعة أو مدى هذا التبادل النووكليوتيدي لأي من Gαs أو Gαi1. بعبارة أخرى، لا تتصرف بيتا-أريستين 1 كإنزيم "مفتاح تشغيل" كلاسيكي لبروتينات G. بدلًا من ذلك، يظهر تأثيرها على بنيتها الخاصة. باستخدام بيتا-أريستين 1 مُهندَسًا ذكيًا يمكن تتبّع حركة ذيله عبر الفلورسنة، وجدوا أن Gαs النشط، لكن ليس Gαi1، يعزز تحرير الذيل الطرفي C لبيتا-أريستين عند وجود ببتيد مستمد من المستقبل. في خلايا حية، أكدت تصاوير إضافية ومستشعرات نقل الطاقة أن Gαs وبيتا-أريستين 1 يقتربان من بعضهما عند تحفيز بالهرمون وأن Gαs يساعد في دفع بيتا-أريستين 1 نحو حالة أكثر نشاطًا. 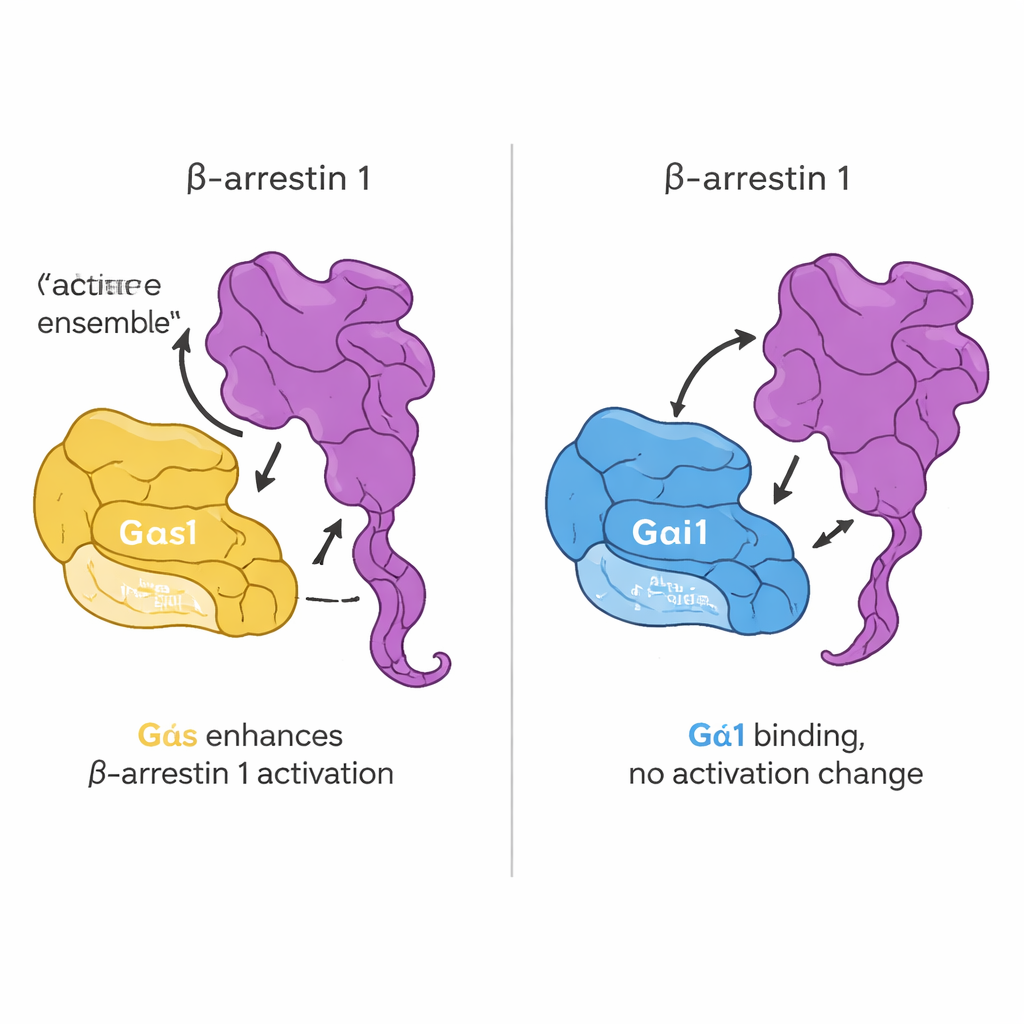
طبقة جديدة من التحكم في إشارات الخلية
عند تجميع هذه النتائج، تقترح الدراسة أن Gαs وGαi1 يرتبطان مباشرة ببيتا-أريستين 1، لكن بطرق متباينة قليلًا وبتبعات مختلفة. لا يتغير السلوك الأساسي "تشغيل/إيقاف" لأي من بروتينَي G بسبب هذا الاتصال. وبدلاً من ذلك، وخصوصًا بالنسبة لـGαs، يعمل التفاعل أكثر كقرص ضبط دقيق على بيتا-أريستين 1، يدفعه أو يستقرّه في شكل أكثر نشاطًا مع تحرير الذيل. هذا يضيف طبقة كانت غير مقدَّرة سابقًا لإشارة مستقبلات GPCR: فالمستقبلات لا تنسق فقط بروتينات G وبيتا-أريستينات، بل يمكن لبروتينات G وبيتا-أريستينات أيضًا أن تضبط بعضها البعض مباشرة. وعلى المدى الطويل، قد يساعد رسم خرائط هذه التداخلات الدقيقة مصممي الأدوية على توجيه الإشارات على مسارات مفيدة — تعزيز المسارات المرغوبة وتجنب تلك التي تسبب آثارًا جانبية.
الاستشهاد: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
الكلمات المفتاحية: المستقبلات المقترنة ببروتين G, بيتا-أريستين, إشارة بروتين G, آليات إشارات الخلايا, علم الأحياء البنيوي