Clear Sky Science · ar
تحليل واسع للحمض النووي فوق الجيني يحدد مثبطات ميثلة الـDNA لمخاطر القلب والأيض المتعلقة بالعلاج لدى الناجين من سرطان الطفولة
لماذا تستمر آثار السرطان في الجسم
بفضل تحسّن العلاجات، يكبر معظم الأطفال المصابين بالسرطان اليوم ويصبحون بالغين. لكن العديد من هؤلاء الناجين يواجهون مشاكل صحية جديدة بعد عقود، بما في ذلك السمنة وارتفاع ضغط الدم وحالات شبيهة بالسكري. يطرح هذا البحث سؤالاً ملحاً: كيف تترك العلاجات الممنوحة في مرحلة الطفولة مثل هذه الآثار الطويلة الأمد على القلب والأيض؟ من خلال فحص العلامات الكيميائية على الـDNA في خلايا الدم، يكشف الباحثون عن دلائل تشير إلى أن العلاج الكيميائي والإشعاعي السابق قد “يعيد برمجة” الجسم بطرق تزيد من مخاطر القلب والأيض على المدى الطويل.
تعقّب المخاطر الخفية لدى الناجين البالغين
دَرَس الفريق ما يقرب من 3000 بالغ ناجٍ من سرطان الطفولة يتابعون ضمن مجموعة متابعة مدى الحياة في مستشفى سانت جود. تلقى هؤلاء الناجون أثناء الطفولة أنواعاً مختلفة من العلاج الكيميائي وإشعاعات إلى الدماغ أو جذع الجسم (الصدر والبطن والحوض)، ثم عادوا بعد سنوات للفحوصات الصحية المفصّلة واختبارات الدم. ركز العلماء على خمسة مشاكل قلبية أيضية رئيسية معروفة بزيادة خطر أمراض القلب والوفاة المبكرة: السمنة، اضطراب سكر الدم، ارتفاع الثلاثي غليسريدات، ارتفاع الكوليسترول، وارتفاع ضغط الدم. بمقارنة الناجين المصابين بهذه الحالات وغير المصابين، بحثوا في ملايين المواضع عبر الجينوم عن اختلافات في ميثلة الـDNA—مفاتيح كيميائية دقيقة تساعد في التحكم في تشغيل أو إيقاف الجينات.
العلامات الكيميائية على الـDNA كتذكير بالعلاج
عبر الجينوم، وجد الباحثون ما يقرب من 1900 موضع DNA ارتبطت مستويات الميثلة فيها بواحدة على الأقل من الحالات الخمس للقلب والأيض. ارتبطت معظم هذه المواضع بمشكلة واحدة فقط، لكن مجموعة صغيرة بدا أنها “محاور” مرتبطة بعدة مشاكل. خمسة مواضع رئيسية، تقع بالقرب من جينين يُدعيان CPT1A وLMNA، ارتبطت بالخمس مخاطر القلبية الأيضية في آن واحد. تُعرف هذه الجينات بتأثيرها على كيفية تعامل الجسم مع الدهون وكيف تحافظ الخلايا على بنيتها، ما يوحي بأن العلاج قد يزعزع مسارات أيضية وقلبية مشتركة. تداخلت العديد من تغييرات الميثلة مع إشارات رُصِدت سابقاً في عامة السكان، لا سيما تلك المتعلقة بالالتهاب، بينما بدا أن بعضها فريد لدى الناجين من السرطان—مشيراً إلى أن للعلاج بصمته البيولوجية المميزة الخاصة.
ربط العلاج وتغيّرات الـDNA والمرض
كانت الخطوة التالية اختبار ما إذا كانت هذه التغيّرات في الميثلة تفسّر بالفعل كيف يؤدي العلاج إلى المرض لاحقاً، بدلاً من كونها مجرد علامة مرافقة. ركز الباحثون على المشكلات القلبية الأيضية الجديدة أو المتفاقمة التي ظهرت فقط بعد أخذ عينة الدم، محافظين بذلك على التسلسل الزمني من العلاج إلى تغيّر الـDNA ثم المرض. باستخدام تحليلات وسيطة إحصائية، حددوا 24 موضع ميثلة فسّرت معاً ما يصل إلى حوالي ربع الارتباط بين علاجات محددة والمشكلات القلبية الأيضية اللاحقة. أظهرت الإشعاعات إلى الدماغ وجذع الجسم أنماطاً قوية بشكل خاص: مجموعات من مواضع الميثلة فسرت نحو 10–20% من تأثير هذه العلاجات الإشعاعية على اضطراب سكر الدم. أحد المواضع البارزة، بالقرب من جين يُدعى ANTXR2، بدا أنه يوسّط نحو 20% من تأثير إشعاع الجذع على مشاكل الغلوكوز اللاحقة.
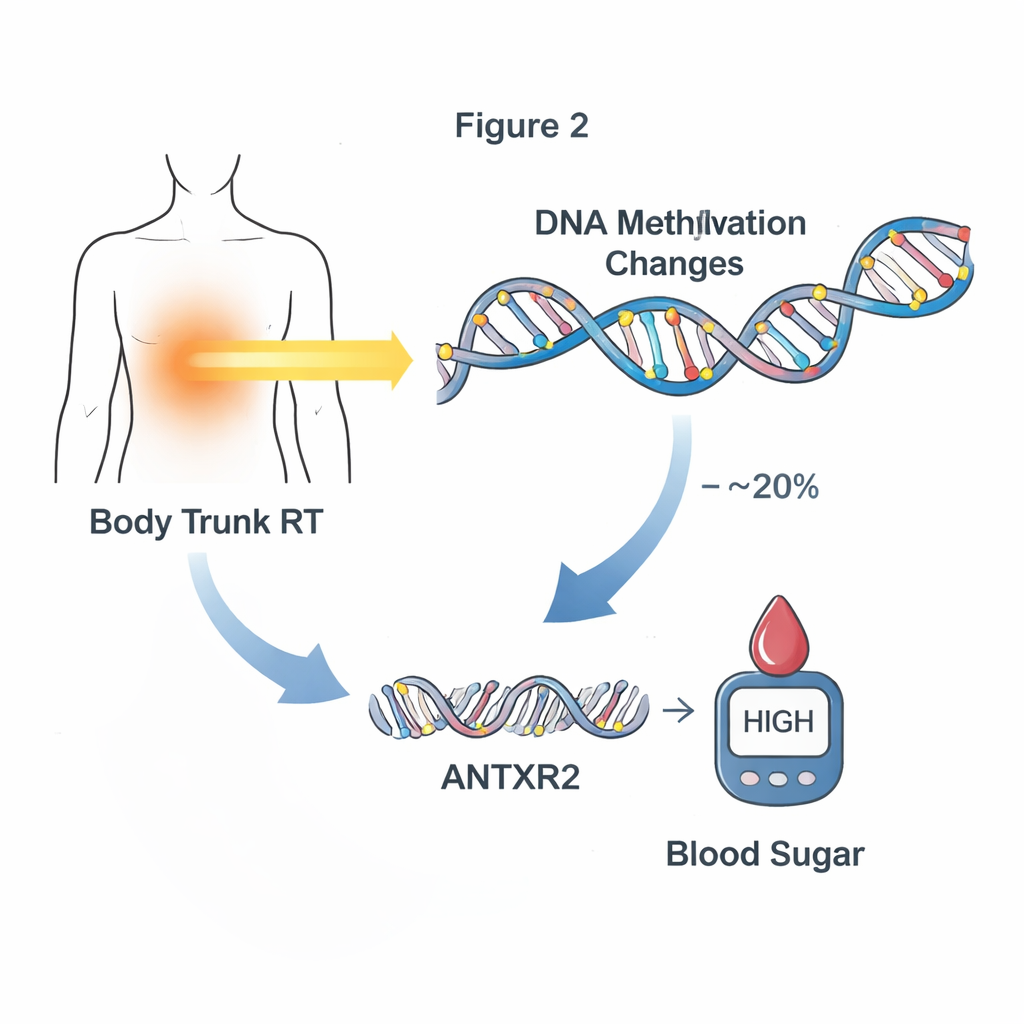
من علامات الـDNA إلى نشاط الجين
لفهم كيف قد تغير هذه العلامات الميثلية البيولوجيا، فحص الفريق نشاط الجينات في مجموعة فرعية من الناجين الذين كان لديهم بيانات لكل من الـDNA وRNA من دمهم. وجدوا عشرات مواضع الميثلة التي ارتبطت فيها مستويات أعلى أو أقل من الميثلة بتغيرات في التعبير الجيني القريب. من بينها كان موضع الوساطة الرئيسي بالقرب من ANTXR2، حيث ارتبطت مستويات الميثلة بقوة بكمية تعبير هذا الجين، خاصة لدى الناجين الذين تلقوا إشعاع الجذع. يساعد ANTXR2 في تنظيم الأوعية الدموية والإطار النسيجي المحيط—وهي أنظمة تؤثر في كيفية مرور الغلوكوز والأنسولين عبر الجسم. يقترح هذا النمط سلسلة من الأحداث التي قد تبدأ بتأثير الإشعاع على الميثلة، يتبعه تغيير في نشاط الجين، مما قد يدفع الجسم نحو اضطراب سكر الدم.
ما يعنيه ذلك للناجين والرعاية المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن علاجات سرطان الطفولة لا تضر الأنسجة لحظةً فحسب؛ بل قد تترك أيضاً «ملاحظات» طويلة الأمد على الـDNA تشكل الصحة لعقود. في هذه الدراسة، بعض تلك الملاحظات—تغيّرات في ميثلة الـDNA—تساعد في تفسير سبب تعرض بعض الناجين لمخاطر أكبر للإصابة بالسمنة أو ارتفاع الدهنيات في الدم أو مشاكل الغلوكوز المرتبطة بالسكري وأمراض القلب. ومع أن هذه العلامات الكيميائية تُمثّل جزءاً فقط من القصة، فقد تخدم مستقبلاً كعلامات حيوية في الدم لتحديد الناجين الأكثر عرضة للخطر وللاختبار ما إذا كانت تغييرات نمط الحياة أو علاجات جديدة قادرة على إعادة كتابة بعض هذا التاريخ فوق الجيني بأمان. يدفع هذا العمل رعاية الناجين خطوة نحو الطب الدقيق: استخدام آثار جزيئية للعلاج السابق لتوجيه الوقاية المبكرة والأكثر تخصيصاً من أمراض القلب والأيض.
الاستشهاد: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
الكلمات المفتاحية: ناجون من سرطان الطفولة, ميثلة الـDNA, مخاطر القلب والأيض, العلاج الإشعاعي, علم فوق الجينات