Clear Sky Science · ar
ProteoAutoNet: تحليل البروتينات المشتركة عالي الإنتاجية باستخدام الروبوتات وتعلم الآلة
لماذا فهم شراكات البروتين مهم
داخل كل خلية، نادراً ما تعمل البروتينات بمفردها. تتعاون في تحالفات متغيرة لبناء الهياكل ونسخ الحمض النووي وتدمير الأجزاء التالفة وتغذية النمو. العديد من السرطانات تختطف هذه الشراكات، لكن رسم خرائطها بتفصيل دقيق كان بطيئاً ويتطلب جهوداً مضنية. تقدم هذه الدراسة ProteoAutoNet، نظاماً مدفوعاً بالروبوتات وتعلم الآلة يسرّع بشكل كبير طريقة اكتشاف شراكات البروتين في الخلايا، ويظهر كيف يمكن لهذا النهج أن يكشف نقاط ضعف خفية في سرطانات الغدة الدرقية.
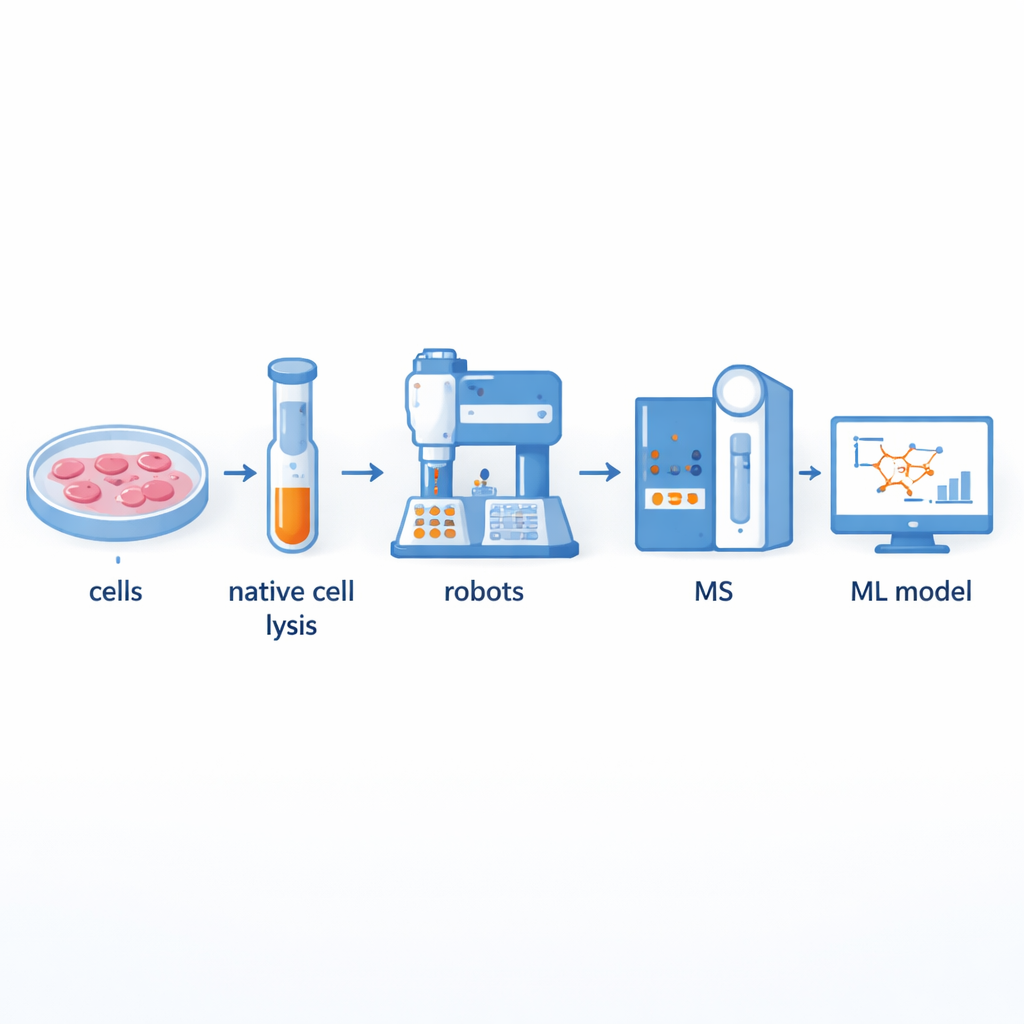
بناء مصنع أسرع لشراكات البروتين
تقليدياً يستخدم العلماء طريقة تسمى مطيافية الكتلة بالتجزئة المشتركة لفصل المجمعات البروتينية الكبيرة ثم تحديد مكوناتها. رغم قوتها، فإن هذه الطريقة مرهقة وتعمل بمعدل منخفض: إعداد مئات الكسور يدوياً قد يستغرق أياماً عدة. بنى المؤلفون منصة مساعدة بالروبوتات تؤتمت معظم سير العمل هذا. تُكسر محتويات الخلايا برفق أولاً حتى تبقى المجمعات البروتينية الطبيعية سليمة، ثم تُمرر عبر أعمدة تعتمد على الحجم لتُقسم إلى عشرات الكسور. تتولى روبوتات معالجة السوائل وأذرع روبوتية إضافة المواد الكيميائية، وهضم البروتينات إلى أجزاء أصغر، وتنقية العينات، وتوصيلها إلى مطياف الكتلة للقياس. يمكن لهذا الإعداد معالجة ما يصل إلى 540 كسراً من عدة خطوط خلايا درقية في يومين إلى ثلاثة أيام فقط، ما يُضاعف تقريباً الإنتاجية مقارنة بالأنظمة نصف المؤتمتة السابقة.
روبوتات ليست أسرع فحسب، بل أكثر موثوقية
السرعة وحدها لا تكفي إذا كانت النتائج صاخبة أو غير متسقة. تحقق الفريق بعناية ما إذا كانت سلسلة الروبوتات تنتج جودة مساوية أو فائقة لمعالجة اليدوية التقليدية. باستخدام عينات مراقبة الجودة، أظهروا أن النظام الآلي تحدد مراراً ما يقارب 3000 بروتين لكل خط خلية درقية مع تراكب عالٍ بين التكرارات واتفاق قوي في كميات البروتين المقاسة. عندما قارنوا مباشرة المعالجة الروبوتية واليدوية لنفس العينات، اكتشف كلا الأسلوبين أعداداً متشابهة من البروتينات، لكن الطريقة الروبوتية أظهرت تبايناً أقل قليلاً في العدادات وقياسات وفرة بروتينية أكثر استقراراً. هذا يعني أن المنصة الجديدة لا توفر الوقت والجهد فحسب، بل تدعم أيضاً تجارب أكثر قابلية للتكرار — وهو مطلب حاسم للدراسات الكبيرة والتطبيقات السريرية.
تعليم الحواسيب على تمييز الروابط ذات المغزى
حتى مع الأجهزة السريعة، تبقى تحدٍ مركزي: تحديد أي البروتينات تتفاعل فعلاً وأيها تظهر معاً بالصدفة. لمواجهة هذا، جمع المؤلفون قواعد بيانات مجمعة للمجمعات البروتينية مع نموذج تعلم آلي يعتمد على خوارزمية XGBoost. قاموا أولاً بتنظيف ودمج ثلاث مصادر رئيسية للمجمعات البروتينية، فتوصلوا إلى 96,635 تداخلاً معروفاً بين البروتينات. ثم استخدموا ملفات تعريف كيفية ظهور البروتينات عبر الكسور كميزات إدخال، وعلموا الأزواج على أنها شركاء محتملون أو غير شركاء استناداً إلى قواعد البيانات. وبما أن الشراكات الحقيقية عالية الثقة نادرة نسبياً، استخدموا استراتيجية تكبير بيانات مستهدفة: صنعوا نسخاً عديدة معدلة قليلاً من الأمثلة الإيجابية المعروفة لتعليم النموذج التعرف على الأنماط المتينة بدلاً من حفظ آثار محددة. مدرَّب على عشرات الملايين من هذه الأمثلة من ثلاثة خطوط خلايا درقية، حقق النموذج أداءً قوياً، حيث صنف التفاعلات الحقيقية فوق العشوائية بشكل جيد في الاختبارات الداخلية وفي خط خلية مستقل للتقييم.
رؤى جديدة عن آلية خلوية للسرطان
بواسطة هذا سير العمل، رسم الباحثون شبكات التفاعل في خط خلية درقية طبيعي وخطين سرطانيين: خط سرطان درقي حليمي وخط سرطان جريبي قادر على الانتقال إلى الرئتين. عبر هذه الخلايا، حددوا أكثر من 25,000 تفاعل بروتيني محتمل ووجدوا إشارات قوية من آلات خلوية معروفة مثل الريبوسومات (التي تبني البروتينات) والبروتيازومات (التي تكسرها)، مؤكداً أن الطريقة تستعيد البيولوجيا المألوفة. بمقارنة الخلايا السرطانية مع الخلية الطبيعية، كشفوا شبكات تم تنشيطها في المرض. في خلايا السرطان الجريبي المنتشرة، كانت مكونات البروتيازوم ومجمع شابرون يُسمى بريفولدين أكثر ارتباطاً ووفرة بشكل ملحوظ. رُبطت عدة وحدات فرعية من بريفولدين سابقاً بأنواع سرطانية أخرى، لكن المسوحات البروتينية العامة فاتتها سلوكها المنسق في سرطان الغدة الدرقية، ربما لأن هذه البروتينات تُضبط بشدة عبر التحلل. كشفت طريقة التجزئة المشتركة تغيراتها المنسقة على مستوى المجمعات.
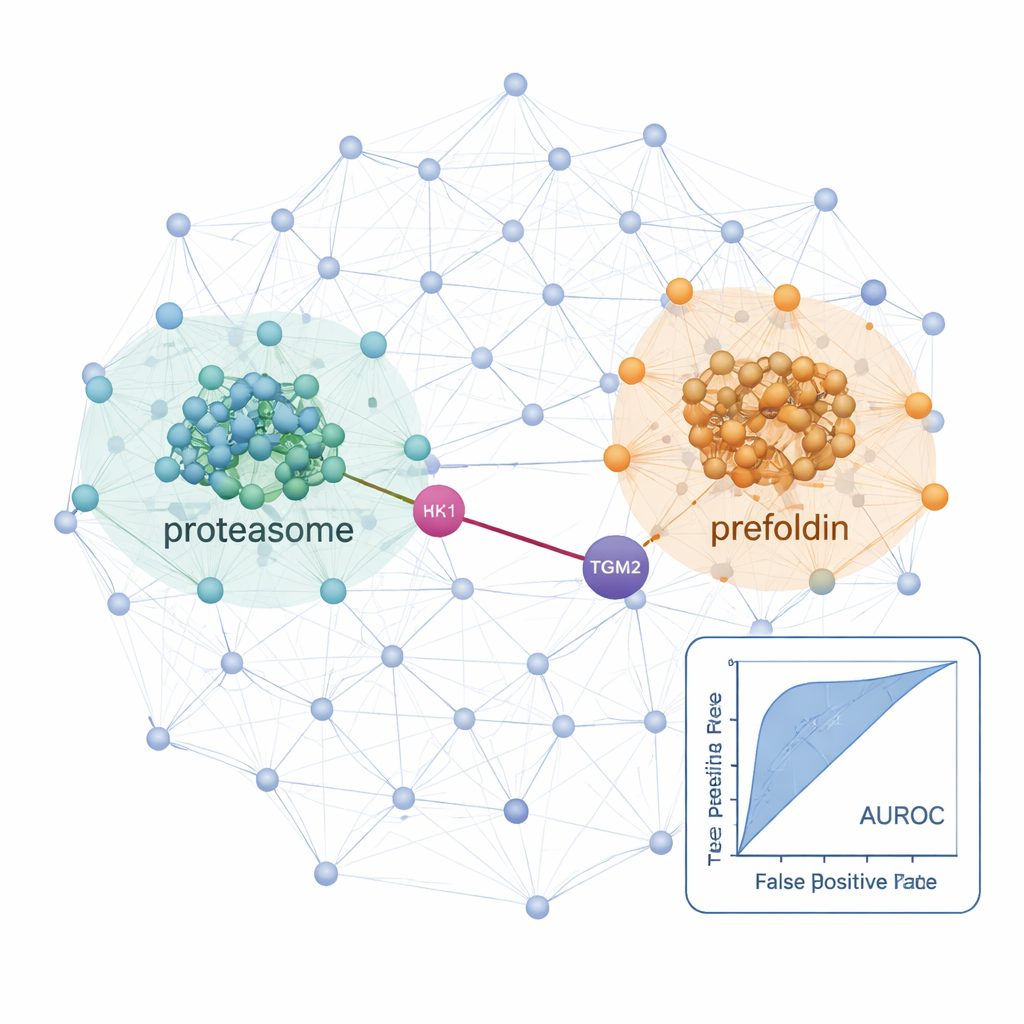
روابط خفية قد توجه علاجات مستقبلية
سلَّطت الدراسة أيضاً الضوء على تفاعلات محددة قد تكون مهمة في كيفية نمو سرطانات الغدة الدرقية وانتشارها. من الأمثلة شراكة متوقعة بين HK1، إنزيم يبدأ مسار الأيض الرئيسي للسكريات في الخلية، وTGM2، بروتين معروف بتشجيع الغزو والنقائل في أورام الغدة الدرقية. هذا الاتصال بين HK1 وTGM2، الغائب عن قواعد البيانات الحالية للتفاعلات، تدعمه نمذجة هيكلية وظهر نشطاً بشكل خاص في خط السرطان الحليمي، مما يوحي بأن إعادة برمجة الأيض والسلوك الغازي قد تكون مرتبطة فعلياً. مجتمعة، تظهر ProteoAutoNet كيف يمكن لدمج الروبوتات وتعلم الآلة تحويل رسم خرائط شبكات البروتين البطيء والخاضع للخبراء إلى عملية أكثر قابلية للتوسع. للقراء غير المتخصصين، الرسالة الأساسية هي أن هذه التكنولوجيا يمكن أن تكشف كل من التحولات الواسعة في الآليات الخلوية وشراكات بروتينية غير متوقعة قد تساعد مستقبلاً الأطباء على التنبؤ أي سرطانات الغدة الدرقية ستكون عدوانية أكثر وتقترح أهدافاً علاجية جديدة.
الاستشهاد: Lyu, M., Hu, P., Zhang, G. et al. ProteoAutoNet: high-throughput co-eluted protein analysis with robotics and machine learning. Nat Commun 17, 1949 (2026). https://doi.org/10.1038/s41467-026-68686-9
الكلمات المفتاحية: تفاعلات البروتين, مطيافية الكتلة, تعلم الآلة في علم الأحياء, سرطان الغدة الدرقية, البروتيازوم وبريفولدين