Clear Sky Science · ar
خلايا NK موجبة لـ ZNF683 تتحكم في حساسية العلاج الكيميائي في سرطان البلعوم الباطن المتقدم عبر إعادة تشكيل البيئة المناعية الدقيقة
لماذا ينجح العلاج الكيميائي مع بعض سرطانات الحلق أكثر من غيرها
يصادف مرضى سرطان البلعوم الباطن المتقدم — الورم الكامن عميقًا في الحلق — عادة بروتوكولات علاج كيميائي قاسية مع نتائج غير مؤكدة. تذوب بعض الأورام، بينما تكاد أخرى لا تتأثر. تسأل هذه الدراسة سؤالًا بسيطًا لكنه حاسم: ما المختلف داخل الأورام التي تستجيب جيدًا؟ من خلال فحص الخلايا المناعية فردًا فردًا، يكشف الباحثون عن نوع معين من الخلايا «الحارسة» التي قد توازن بين نجاح أو فشل العلاج الكيميائي التقليدي.
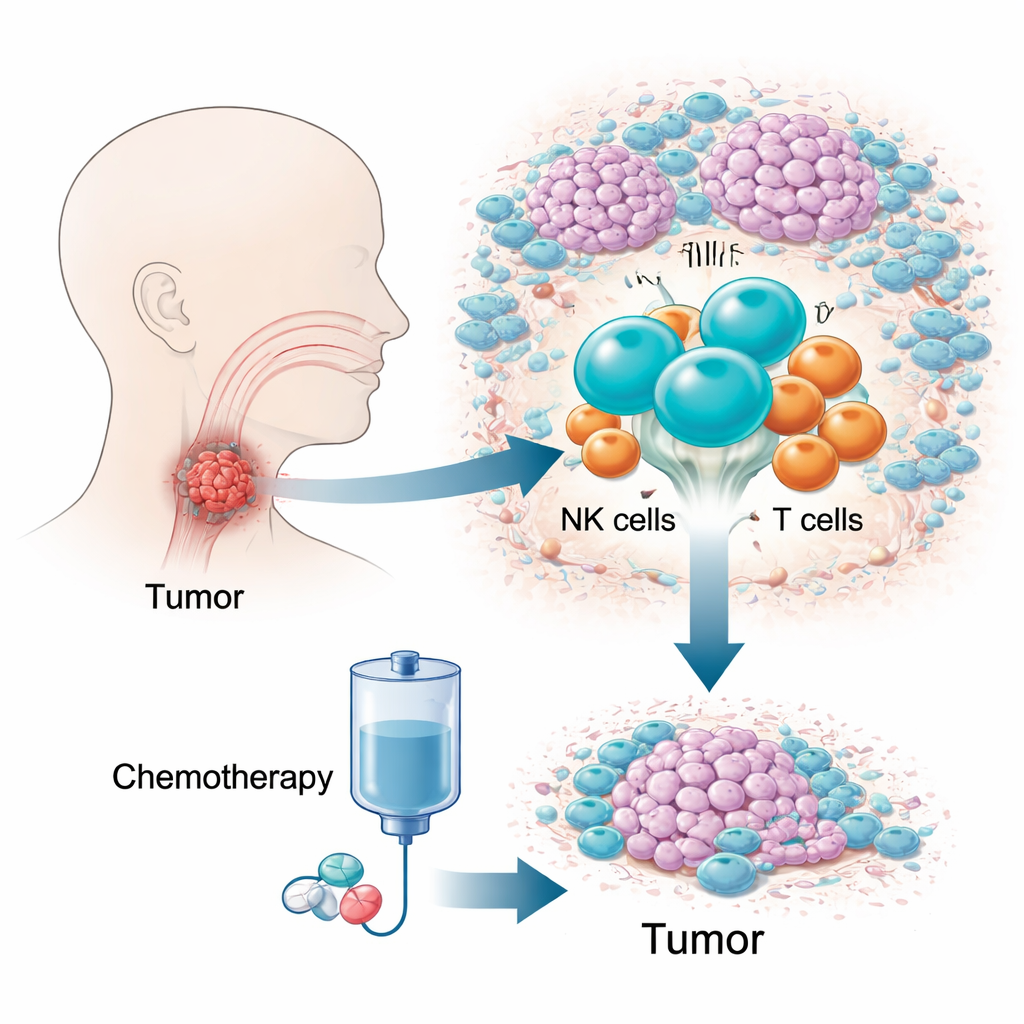
تحدي سرطان مخفي وصعب العلاج
سرطان الخلايا الحرشفية للبلعوم الباطن يعد واحدًا من أخطر سرطانات الرأس والرقبة، جزئيًا لأنه ينمو في منطقة ضيقة يصعب فحصها ويتسبب بقليل من الأعراض في المراحل المبكرة. يُشخَّص كثير من المرضى في مراحل متأخرة، حيث تكون الخيارات محدودة ومعدل البقاء لخمس سنوات منخفضًا. يُستخدم مزيج دوائي يعرف باسم علاج TPF على نطاق واسع لأنه يمكن أن يتحكم في المرض مع الحفاظ على صندوق الصوت. ومع ذلك، يُظهر 10–20 بالمئة من المرضى استجابة ضئيلة أو معدومة، ما يهدر وقتًا ثمينًا. لقد كافحت الاختبارات الجينية التقليدية، التي تجمع الإشارات عبر ملايين الخلايا، لتفسير هذا الاختلاف، ما دفع المؤلفين للتركيز بدلًا من ذلك على نظام الأورام الحي المكوّن من خلايا مناعية.
قراءة المشهد المناعي للورم خلية بخَلَية
فئة مميزة من خلايا NK تمهد نجاح خلايا T
بتعمق أكبر، قسم الفريق خلايا NK إلى ثلاث مجموعات بناءً على ميزاتها الجزيئية. لم ترتبط إلا واحدة منها، الموسومة بعامل النسخ ZNF683 والمتمركزة إلى حد كبير في الأنسجة المحيطة بعشّ الورم، ارتباطًا قويًا جيدًا باستجابة العلاج الكيميائي. كان المرضى الذين تحوي أورامهم المزيد من هذه الخلايا NK موجبة ZNF683 عند الخط الأساسي أكثر احتمالًا بكثير للاستفادة من TPF. في تجارب الفئران، أدى استئصال خلايا NK إلى زوال الفائدة الناتجة عن العلاج الكيميائي تقريبًا بالكامل، مما يؤكد أن نشاط NK ليس مجرد علامة بل ضرورة للمعالجة الفعالة. ومن المثير أن هذه الخلايا لم تكن تعمل ببساطة كقاتلات مباشرة للسرطان؛ بل كانت برامج جينية فيها مُثرية لإرشاد وتفعيل خلايا T.
كيف تمنح خلايا NK تفويضًا لخلايا T القاتلة للأورام
لفهم أي خلايا T كانت الأكثر أهمية، تعقّب العلماء نسائل مستقبلات T الفردية قبل وبعد العلاج. وجدوا أنه في المستجيبين، توسعت مجموعة محددة من خلايا CD8 من نوع «الذاكرة الفعالة» والمُثبَّطة بـ GZMK بشكل كبير بعد العلاج الكيميائي. أنتجت هذه الخلايا مستويات عالية من السيتوكاينات السامة TNF والإنترفيرون-غاما دون إظهار إرهاق عميق، مما جعلها قاتلة قوية ودائمة. كشف التصوير المكاني أنه بعد العلاج، تجمعت خلايا GZMK+ CD8 بقوة في أورام المستجيبين لكن ليس في أورام غير المستجيبين. في اختبارات التعايش الخلوي في المختبر باستخدام خلايا بشرية، دفع التلامس المباشر مع خلايا NK موجبة ZNF683 نمو زمرة خلايا CD8 GZMK+ هذه، وهو تأثير اختفى عندما فصلت الخلايا بحاجز.
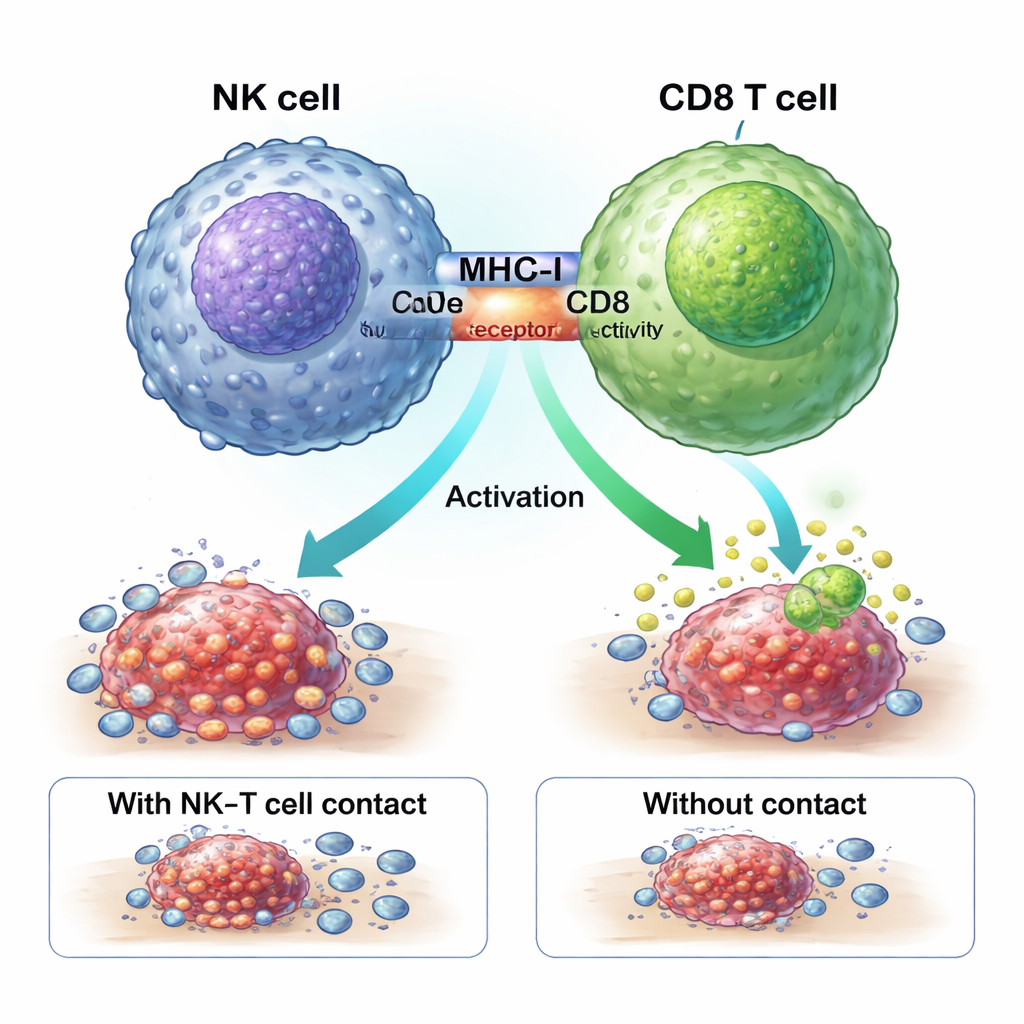
مصافحة فعلية تُشغّل مقاتلي الورم
تظهر الدراسة أن خلايا NK موجبة ZNF683 تعزز استجابة العلاج الكيميائي عبر «مصافحة» فعلية مع خلايا CD8 T. جزيئات تسمى MHC-I على سطح خلايا NK تتفاعل مع مستقبلات CD8 على الخلايا T في منطقة اتصال وثيق تُعرف بالمشْبك المناعي. أدى حجب MHC-I إلى إيقاف قدرة خلايا NK على توليد خلايا CD8 القوية GZMK+. في فئران مهندسة خصيصًا تفتقر إلى ZNF683 فقط في خلايا NK، عبرت هذه الخلايا عن مستويات أقل من MHC-I وكانت أضعف بكثير في تنشيط خلايا CD8، مما يعزز الفكرة أن ZNF683 يبرمج خلايا NK لتصبح مدربين فعّالين لخلايا T المقاتلة بدلًا من أن تكون مجرد منفذين.
ماذا يعني هذا للمرضى
للقراء العامين، الرسالة الأساسية هي أن كل الخلايا المناعية داخل الورم ليست متساوية. تحدد هذه الدراسة فئة محددة من خلايا NK ككاشف متقدم يهيئ ساحة المعركة قبل بدء العلاج الكيميائي. الأورام الغنية بهذه الخلايا مستعدة لإطلاق موجات من خلايا CD8 القوية عندما تؤثر الأدوية، ما يؤدي إلى انكماش أكبر بكثير. قد يساعد قياس وفرة محور NK–T هذا قبل العلاج الأطباء على التنبؤ بمن سيستفيد من علاج TPF ومن قد يحتاج إلى علاجات بديلة أو إضافية. في المستقبل، قد تحول العلاجات التي تعزز أو تحاكي هذه الخلايا NK موجبة ZNF683 سرطانات البلعوم الباطن المقاومة إلى سرطانات أكثر حساسية للعلاج الكيميائي القياسي.
الاستشهاد: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
الكلمات المفتاحية: سرطان البلعوم الباطن, مقاومة العلاج الكيميائي, خلايا القاتل الطبيعي, البيئة المناعية الدقيقة للأورام, خلايا CD8 T