Clear Sky Science · ar
تنظيم تجميع محول AP1 بواسطة الشيفر المزدوج الأذرع MEA1
لماذا يهم هذا المساعد الخلوي المخفي
داخل كل خلية بشرية، تعمل آلاف الطرود الصغيرة على نقل البروتينات إلى المكان الذي تحتاجه أو إلى "مركز إعادة التدوير" الخلوي لتحللها. تحافظ هذه الحركة على صحة خلايانا وتضبط دفاعاتنا المناعية. الورقة الملخّصة هنا تكشف عن بروتين كان غامضًا سابقًا يُدعى MEA1، والذي يتبيّن أنه أساسي لبناء أحد الآلات الفرزية الرئيسية التي تحمّل هذه الطرود. فهم كيفية عمل MEA1 يساعد على توضيح كيفية تحكم الخلايا في حمولات مهمة، بما في ذلك جزيئات تُشغِّل أو تُطفئ الاستجابات المناعية المضادة للفيروسات.
ضبط المرور في مركز شحن الخلية
تجري الكثير من عمليات الشحن داخل الخلية عبر تركيب يُدعى جهاز جولجي، وهو تتابع من الأكياس المسطحة يعمل بمثابة مكتب بريد مركزي. من جهاز جولجي يمكن إرسال الحمولات إلى سطح الخلية للاستخدام أو توجيهها إلى حجيرات داخلية للتحلل. يقع مركب بروتيني يعرف باسم AP1 في قلب هذا المسار. يتعرف AP1 على وسمات على بروتينات الحمولة، ويساعد على انحناء الغشاء، ويجنّد غطاء خارجي من كلاترِين لتشكيل حويصلات نقل صغيرة. من دون تجميع صحيح لـ AP1، تتراكم حمولات حيوية في أماكن خاطئة وقد تختل مسارات الإشارة الطبيعية، بما في ذلك تلك المرتبطة بالمناعة. 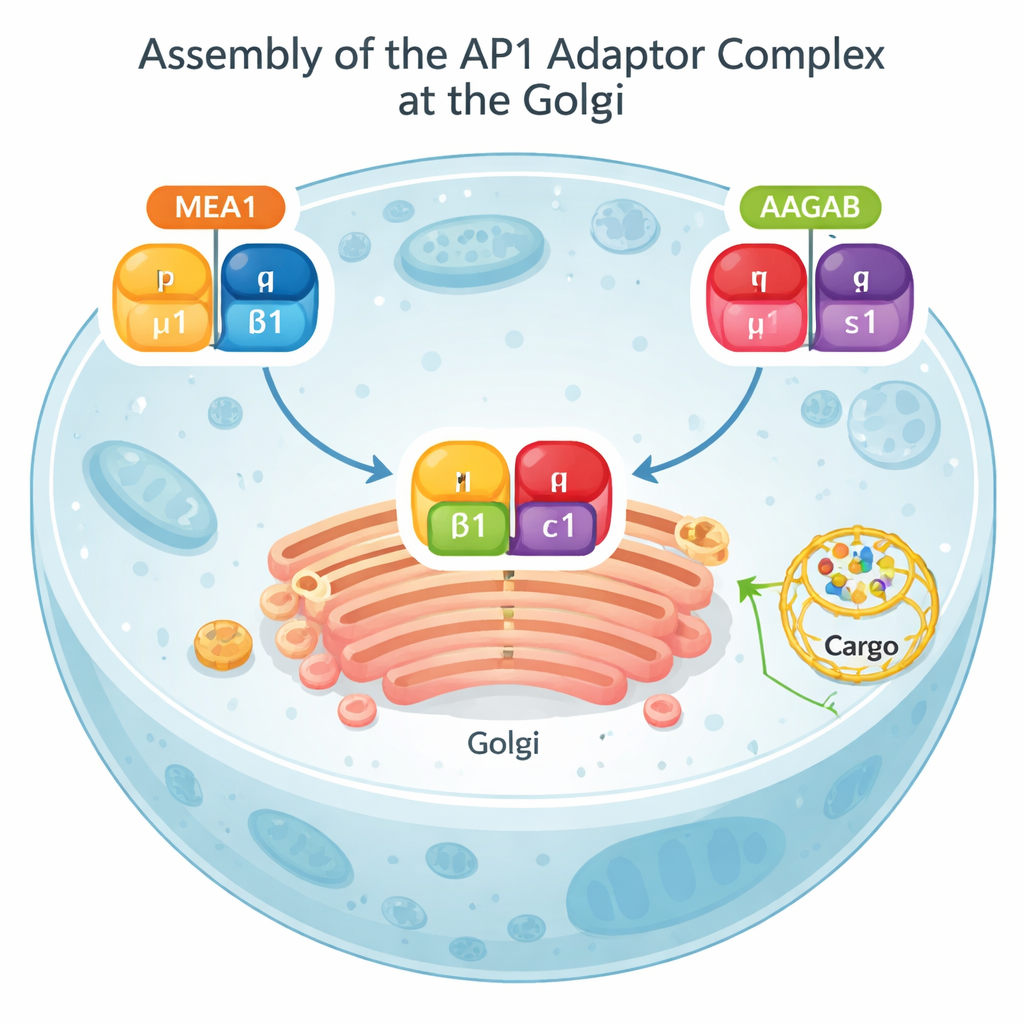
البحث عن عامل تجميع مفقود
سعى المؤلفون إلى تحديد البروتينات التي ترتبط فعليًا بـ AP1 وقد تساعده على التجميع. استعرضوا قاعدة بيانات ضخمة لتفاعلات البروتين، واستبعدوا المرشحين غير المرجحين للعمل مع AP1، ثم استخدموا أداة ذكاء اصطناعي، AlphaFold، للتنبؤ بكيفية اتصال البروتينات المتبقية بأجزاء AP1 الفردية. أظهر هذا البحث أن MEA1، وهو بروتين صغير لم تُوصَف خصائصه سابقًا ويوجد في أنسجة عديدة، بارز كمشارك محتمل. أكدت تجارب لاحقة في خلايا بشرية أن MEA1 يرتبط جزئيًا فرعين محددين من AP1 يُعرفان بـ μ1 وβ1، سواء عند اختباره كل منهما بمفرده أو في أشكالهما الطبيعية غير المُعدَّلة.
MEA1 يحافظ على تماسك AP1 وحركة الحمولة الخلوية
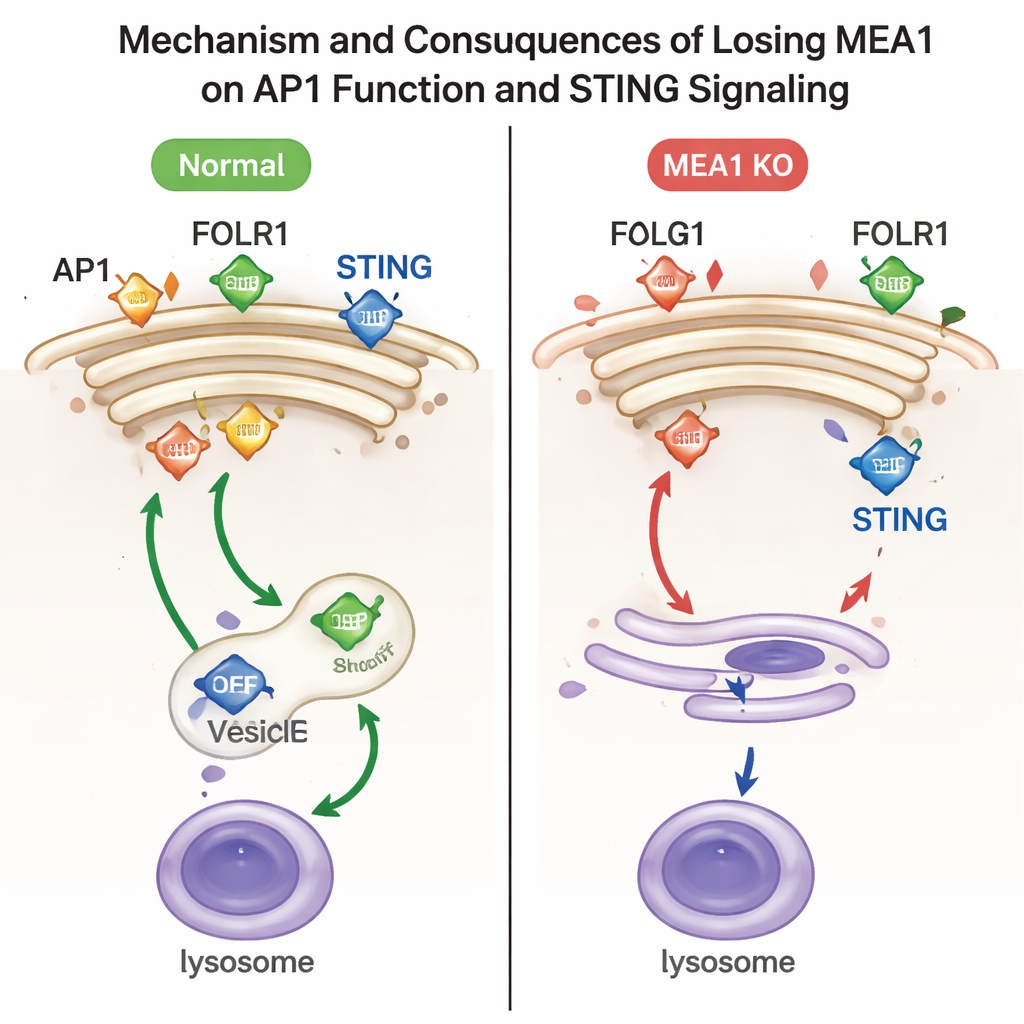
لاستكشاف وظيفة MEA1، حذفت الباحثون جين MEA1 في خطوط خلايا بشرية. عندما غاب MEA1، انخفضت مستويات جميع القطع الأربع لـ AP1 بشكل كبير، وكادت بقع AP1 المميزة قرب جهاز جولجي أن تختفي. كان لهذا الفقدان عواقب وظيفية واضحة. تراكم مستقبل الفولات FOLR1، وهو حمولة معروفة لـ AP1، على سطح الخلية بدلًا من إرساله إلى الداخل، وهو علامة مميزة لخلل في فرز AP1. حمولة أخرى، بروتين الإشارة المناعية STING، لم تُحزم بفعالية في الحويصلات المتجهة إلى الجسيمات الحالّة (الليزوزومات)، مراكز إعادة التدوير الخلوية. نتيجة لذلك، ظل STING المنشط وشريكه الكينازي TBK1 بمستويات مرتفعة، مما يشير إلى أن "مفتاح الإيقاف" لهذا المسار المضاد للفيروسات لم يكن يعمل بشكل صحيح. إعادة إدخال MEA1 استرجعت مستويات AP1 وصححت هذه العيوب في حركة الشحن.
شيفر ذو يدين وعملية بناء قائمة على التصادم
كشفت الاختبارات الكيميائية الحيوية ونماذج AlphaFold أن MEA1 يتصرف مثل شيفر تجميع "ذي يدين": الجزء الأمامي منه يقبض على وحدة μ1، بينما الجزء الخلفي يقبض على β1. بمفردهما، تكون μ1 وβ1 غير مستقرتين وتميلان إلى التكتل أو التحلل؛ مرتبطتان مع MEA1، تصبحان قابليتين للذوبان وجاهزتين للتجميع. شيفر معروف آخر، AAGAB، يؤدي وظيفة موازية لوحدتي AP1 المتبقيتين، γ وσ1. عندما تلتقي مركبات MEA1–μ1–β1 وAAGAB–γ–σ1، تتحد وحداتها لتكوّن محول AP1 الكامل المكوّن من أربعة أجزاء. عند هذه النقطة، يترك كلا الشيفرين تركيبهما ويعودان إلى السائل الخلوي، بينما يتحرك AP1 المُشكل حديثًا إلى الأغشية ليقوم بعمله في الفرز. يوضح هذا الآلية "التصادمية ثنائية الشيفر" أن تجميع AP1 مُنسق بعناية بدلًا من تركه لالتقاءات عشوائية.
دروس أوسع عن مراقبة الجودة الخلوية
خارج إطار AP1، تلمّح الدراسة إلى استراتيجية أوسع قد تستخدمها الخلايا لبناء العديد من الآلات البروتينية الكبيرة. يمكن لـ MEA1 أيضًا أن يساعد بشكل ضعيف في دعم محول آخر يُسمى AP2، ومع AAGAB وشيفر ثالث اسمه CCDC32، يجسد مسارًا أوسع سمّاه المؤلفون "تجميع بروتين المحول بمساعدة الشيفرات". في هذا المخطط، تُثبّت الشيفرات المتخصصة الوحدات الهشة، وتقرب الأزواج الصحيحة معًا، وتمنع مؤقتًا مواقع ارتباط الحمولة حتى يكتمل تكوين المركب ويصبح آمنًا للنشر.
ماذا يعني هذا للصحة والمرض
لغير المتخصصين، الخلاصة الأساسية أن MEA1 هو عامل خلف الكواليس حاسم يساعد في تجميع AP1، آلة فرز مركزية في خلايانا. عند غياب MEA1، ينهار AP1، تتكوّن اختناقات مرورية، ولا تُطفأ منظّمات مهمة مثل STING بشكل صحيح. قد يساعد هذا الفهم الجديد في نهاية المطاف على تفسير بعض الاضطرابات المناعية أو أمراض أخرى المرتبطة بخلل في حركة البروتين، ويكشف مبدأ عامًا لبناء الخلايا لآلات جزيئية معقدة من أجزاء غير مستقرة.
الاستشهاد: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
الكلمات المفتاحية: نقل البروتين, بروتين المحول AP1, الشيفرات الجزيئية, إشارة STING, بيولوجيا الخلية