Clear Sky Science · ar
التعرف الجزيئي على الثيروغلوبولين بواسطة السورتيلين
كيف تقرر خلايا الغدة الدرقية متى تُطلِق الهرمون
تُساعد هرمونات الدرقية في ضبط «منظم الحرارة» الأيضي لدينا، مؤثرة في كل شيء من معدل ضربات القلب إلى درجة حرارة الجسم. تُبني هذه الهرمونات وتُخزن داخل بروتين ضخم يُسمى الثيروغلوبولين. تكشف هذه الدراسة كيف يساعد بروتين آخر، السورتيلين، خلايا الغدة الدرقية على اختيار شكل الثيروغلوبولين الذي يجب سحبه مرة أخرى إلى داخل الخلية حتى يُفرَج عن الهرمون في مجرى الدم — قرار يؤثر في النهاية على كمية هرمون الدرقية المتاحة في أجسامنا.
بروتين مخزن ينتظر المعالجة
الثيروغلوبولين هو بروتين هائل على شكل حرف Y تُنتجه خلايا الغدة الدرقية وتفرزه إلى بركة هلامية تُسمى السائل الكولودي. هناك يعمل كمادة خام ومستودع لهرمون الدرقية: أجزاء محددة من الأحماض الأمينية داخل الثيروغلوبولين تُعدّل كيميائياً باليُود لتتحول إلى هرمونات الدرقية، وهي لا تزال مدمجة داخل البروتين الأكبر. لتحرير هذه الهرمونات فعلياً، يجب أخذ الثيروغلوبولين مرة أخرى إلى داخل الخلية، وتفتيته داخل حُويصلات إعادة التدوير المسماة الليسوزومات، ونقل قطع الهرمون إلى الدم.
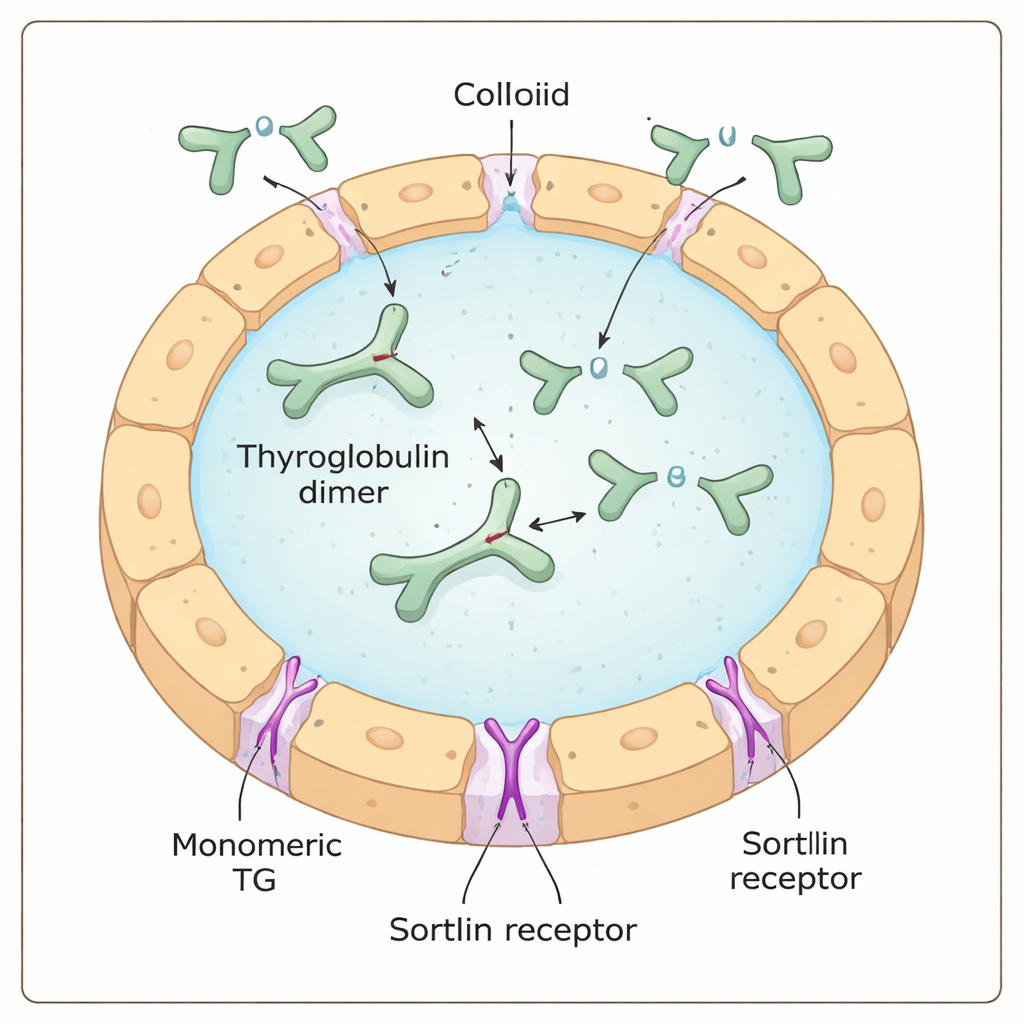
حارس بوابة خلوي ذو تفضيل خفي
اقترح أن مستقبل السورتيلين هو واحد من «حراس البوابة» الذين يرتبطون بالثيروغلوبولين على سطح الخلية ويُوجّهونه إلى الداخل. أشارت أعمال سابقة إلى أن السورتيلين يفضّل الثيروغلوبولين المشبع باليُود بدرجة عالية، ما يوحي بأن المستقبل قد يحسّ بمحتوى اليُود بشكل مباشر. باستخدام مزيج من الاختبارات الكيميائية الحيوية، وقياسات الكتلة على مستوى جزيء منفرد وتجارب التقاط خلوية، وجد الباحثون بدلاً من ذلك أن السورتيلين يفضّل بقوة الشكل أحادي الوحدة (المونوميري) من الثيروغلوبولين على الشكل الزوجي الأكثر شيوعاً (الديimer). كلما زادت نسبة المونوميرات في العينة، زادت كفاءتها في تكوين مركبات مع السورتيلين وابتلاعها بواسطة خلايا الدرقية، بغض النظر عن كمية اليُود التي تحمّلها.
تكبير نقطة التماس
لفهم هذا التفضيل على المستوى الذري، لجأ الفريق إلى الميكروسكوب الإلكتروني بالتبريد عالي الدقة وطيفية الكتلة بعد الربط المتقاطع. أظهرت هذه الطرق أن السورتيلين يتعرف على ذيل قصير ومرن في النهاية C-طرفية (نهاية واحدة) من الثيروغلوبولين المونوميري. ينسدل هذا الذيل داخل تجويف مركزي في السورتيلين مُشَكَّل كدافع مكوّن من عشر شفرات، ويترسخ عند نقطتين صغيرتين «ساخنتين» داخله. بشكل لافت، في الشكل الديميري يكون جزء من المنطقة المحيطة بهذا الذيل مدفوناً بحيث لا يمكن للسورتيلين الوصول إليه، مفسراً لماذا يكون الديمير شريكاً ضعيفاً. تشير البيانات إلى أن تشذيب الثيروغلوبولين خارج الخلية أو ارتخاؤه — عبر تحلل البروتين الطبيعي — يساعد على تحويل الديميرات إلى مونوميرات يمكن للسورتيلين الإمساك بها.
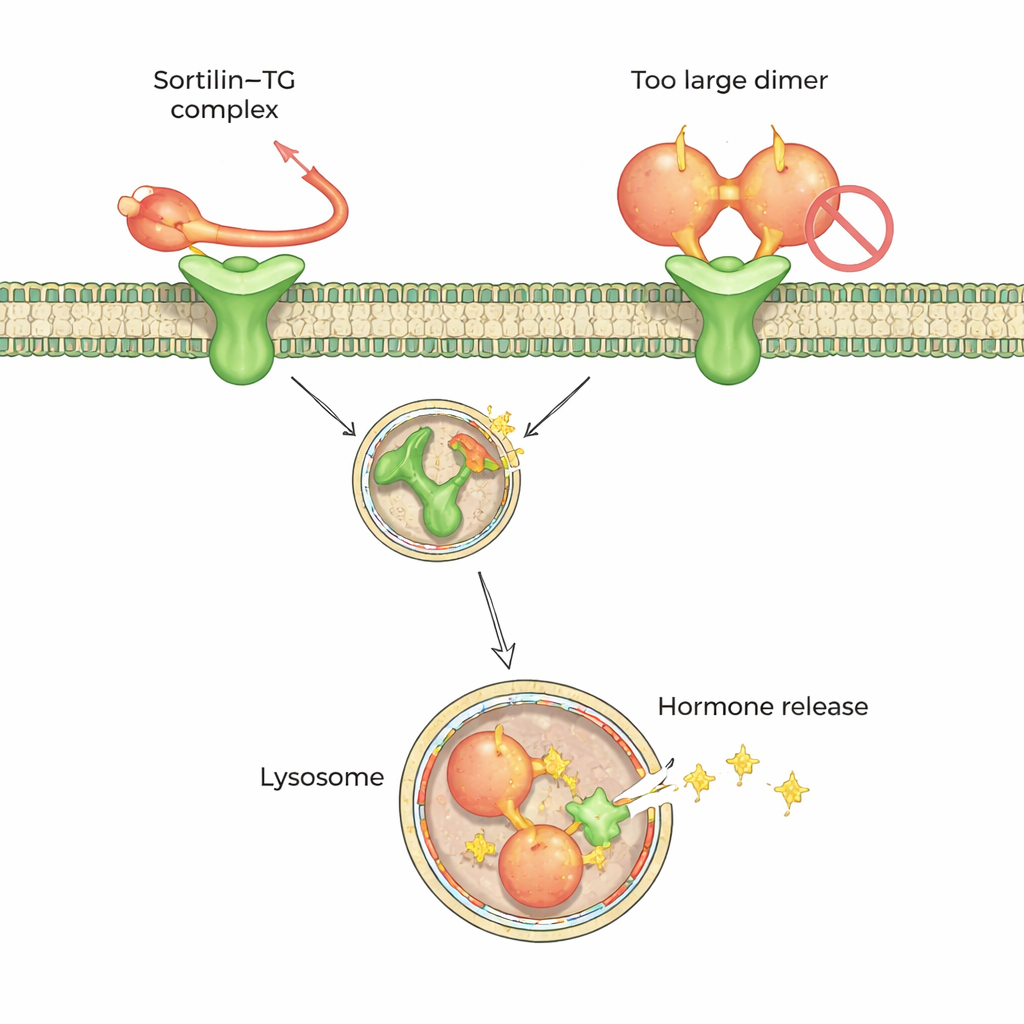
رمز إرساء مشترك للعديد من بروتينات البضائع
السورتيلين ليس بروتيناً خاصاً بالغدة الدرقية فحسب؛ بل يساعد في توجيه العديد من الجزيئات المختلفة في أنحاء الجسم، بما في ذلك عوامل مرتبطة بأمراض القلب والاضطرابات العصبية. من خلال دمج عملهم البنيوي مع أدوات توقع البنى المتقدمة مثل AlphaFold وAlphaPulldown، قارن الباحثون كيف قد يرتبط عشرات الشركاء المعروفين للسورتيلين بتجويف دافعه. وجدوا نمطاً متكرراً: تقدّم العديد من البضائع قطعة ببتيد غير منظمة بطول حوالي عشرين حمضاً أمينياً تناسب نفس الجيب الذي يشغره ذيل الثيروغلوبولين، أحياناً بنفس اتجاه ببتيد دماغي معروف يُدعى نيوترُوستين، وأحياناً بالعكس. على الرغم من الاتجاه المعكوس، تشترك هذه الببتيدات في خواص مماثلة — مجموعة حمضية أو سالبة الشحنة عند أحد الطرفين، وبقاية عطرية كبيرة عند الطرف الآخر، ومقطع مرن غالباً غني بالبرولين في الوسط.
لماذا يهم اليُود أقل من الشكل
بما أن التماس الأساسي بين السورتيلين والثيروغلوبولين هو هذا الذيل المرن، اختبر المؤلفون ما إذا كانت إضافة يود إضافي إلى التيروسين المكوّن للهرمون في الذيل ستغير الارتباط. لم يحدث ذلك: ببتيد اصطناعي يحمل حرفي هرمون الدرقية المكتمل التصنيع تصرف بشكل مطابق تقريباً للنسخة غير المعدَّلة. أظهرت النمذجة أن الحلقة المؤيّدة باليود تبرز إلى المحلول دون إنشاء تلامسات ضيقة جديدة. مع تجارب الالتقاط، يدعم هذا رؤية مُنقَّحة: السورتيلين لا «يعدّ» ذرات اليود على الثيروغلوبولين. بل يحسّ ما إذا كان البروتين قد ارتخى أو تُحلّل جزئياً لدرجة كشف شكله المونوميري وذيله بالشكل المناسب.
ما دلالة هذا لصحّة الغدة الدرقية
لغير المتخصص، الرسالة الأساسية هي أن إطلاق هرمون الدرقية يتحكم به شكل البروتين ومرونته أكثر من كونه بمستشعر يود مدمج. يعمل السورتيلين كقارئ على سطح الخلية، يبحث عن جزيئات ثيروغلوبولين أُرخيت أو شُذّبت إلى مونوميرات، ثم يسحبها إلى الداخل لإتمام إطلاق الهرمون وإعادة تدوير اليود. يوضح هذا العمل خطوة رئيسية في بيولوجيا هرمونات الدرقية ويشير إلى أن الأدوية المصممة لحجب السورتيلين — والتي تُستكشف الآن لأمراض أخرى — قد تغير عن غير قصد معالجة هرمون الدرقية عبر تعطيل هذه خطوة التعرف.
الاستشهاد: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
الكلمات المفتاحية: هرمون الغدة الدرقية, ثيروغلوبولين, سورتيلين, توزيع البروتينات داخل الخلية, الابتلاع الخلوي