Clear Sky Science · ar
حلزون الجسر في Cas12a هو منظم كلوسي للتشكّل الحلقوي وتنشيط RuvC
لماذا يهم هذا لتحرير الجينات
تعتمد العديد من أدوات تحرير الجينات القوية، بما في ذلك تلك المستخدمة في العلاجات الناشئة والاختبارات التشخيصية السريعة، على بروتينات CRISPR التي تقصّ الحمض النووي في مواقع محددة. لكن إذا قطعت هذه المقصات الجزيئية في المكان الخطأ، فقد تتسبب في آثار جانبية ضارة. تفحص هذه الدراسة جزءًا متحركًا صغيرًا داخل مُحرّر Cas12a يُدعى حلزون الجسر، وتظهر كيف تعمل تغيرات شكله كمفتاح أمان داخلي يربط بين التعرف الصحيح على الهدف وقطع الحمض النووي. وفهم هذا المفتاح يوفر خريطة طريق لهندسة أدوات CRISPR أكثر دقة وأمانًا للتطبيقات الطبية والبيوتكنولوجية.
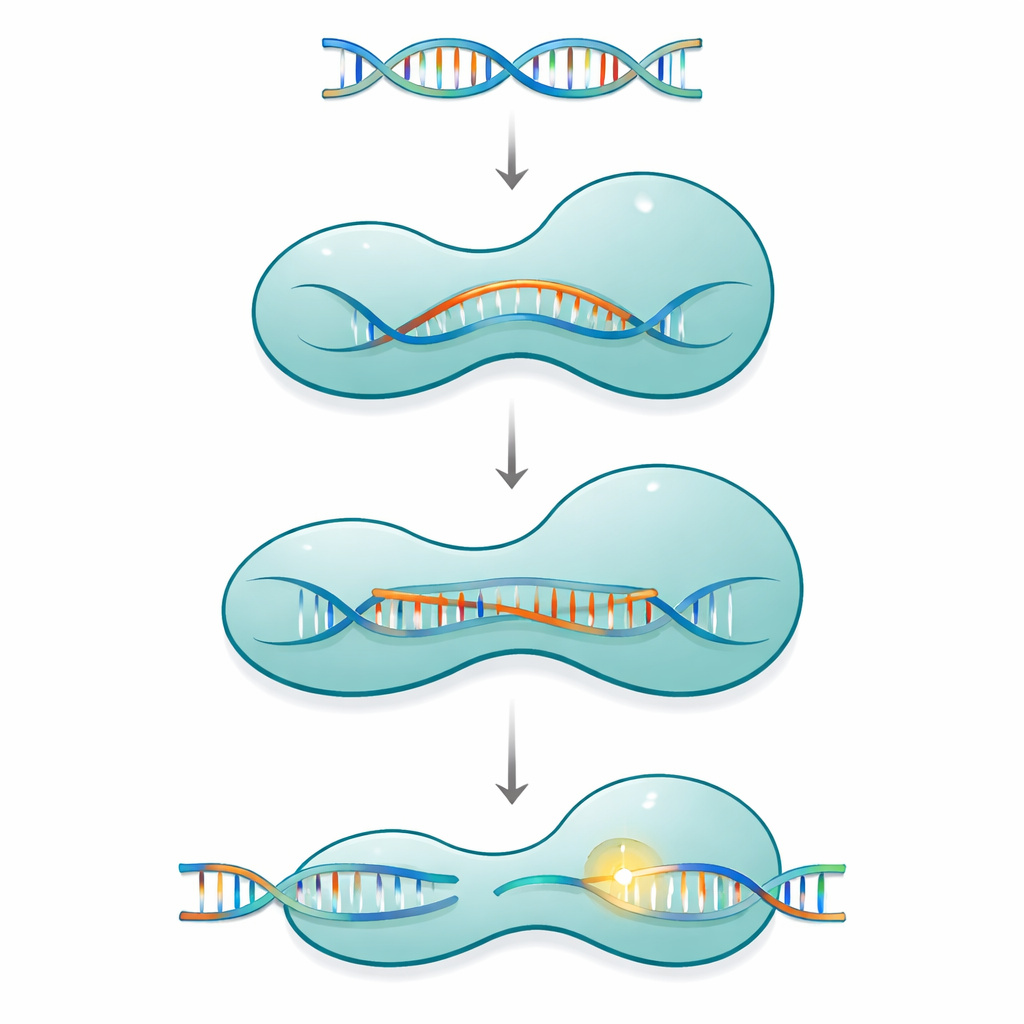
مشبك جزيئي بأجزاء متحركة
ينتمي Cas12a إلى عائلة من أنظمة CRISPR أحادية البروتين التي تستخدم حمضًا نوويًا مرشديًا قصيرًا للعثور على الحمض النووي المطابق وقطعه في فيروسات أو في جينوم الخلية. يتخذ البروتين شكل مشبك ذا ذراعين: طرف للتعرف يتفحص التسلسل، وطرف للقطع يضم الآلية الكيميائية. هذان الجزآن متصلان بشريحة رفيعة مشحونة إيجابيًا تُدعى حلزون الجسر. عندما يرتبط Cas12a بالدليل الريبي ثم بالهدف الحمضي النووي، لا يتصرف البروتين كأداة جامدة، بل يتحرك عبر سلسلة من تغيّرات الشكل الكبيرة والصغيرة التي تغلق تدريجيًا حول هيكل هجين RNA–DNA المتنامي المعروف بحلقة R، ولا ينشط موقع القطع بالكامل إلا بعد تكوّن زوج قواعد صحيح وطويل بما يكفي.
استكشاف مفتاح الأمان المدمج
ركز الباحثون على Cas12a من البكتيريا Francisella novicida ونظروا إلى نسخة مُهندسة سابقًا استُبدلت فيها حمضتا أمينية في حلزون الجسر بالبروالين، وهو تغيير معروف بتقوية أو كسر الهياكل الحلزونية. تقطع هذه المتغيرية، المسماة FnoCas12aKD2P، الحمض النووي بشكل أكثر انتقائية لكن أبطأ من البروتين الطبيعي. باستخدام المجهر الإلكتروني بالتبريد، التقطوا خمس لقطات بنيوية مميزة لهذه المتغيرية وهي مرتبطة بدليلها الريبي وقطعة من الحمض النووي الهدف. تُظهر هذه اللقطات البروتين في مراحل مختلفة على طول مسار تنشيطه، من التعرف الابتدائي المبكر على الحمض النووي إلى الحالات اللاحقة حيث يتكوّن جزء من الهجين RNA–DNA لكن لم تتحقق بعد الجاهزية الكاملة للقطع.
كيف تقود تغيرات الشكل إلى قطع دقيق
أظهر المقارنة بين المتغيرية والهياكل المحددة سابقًا لـCas12a الطبيعي نمطًا واضحًا. في البروتين الطبيعي، يتحول جزء من حلزون الجسر من حلقة مرتخية إلى حلزون أطول مستقيم وينحني نحو الهجين RNA–DNA النامي ليقترب منه. في الوقت نفسه، يترخى حلزون مجاور في مجال القطع، ومنطقة صغيرة تسمى «الغطاء» التي عادةً ما تسد الموقع النشط، تتحول من حلقة إلى حلزون وتدور لتفتح. معًا، تفتح هذه الحركات المنسقة جيبًا يسمح بدخول خيط DNA واحد ويُقصّ. في المتغيرية المحتوية على البروالين، لا يستطيع حلزون الجسر إجراء هذا الانتقال من حلقة إلى حلزون بالكامل أو الانحناء بشكل صحيح. نتيجة لذلك، يبقى الهجين RNA–DNA مشوّهًا وأبعد، ويظل الغطاء في حالة مغلقة شبيهة بالحلقة، ونادرًا ما يصل المجمع إلى حالة قبل-تحفيز كاملة. يبطئ هذا الاختناق الميكانيكي القطع على الهدف ويجعل من الصعب على الحمض النووي غير المتطابق التسلل عبر نقاط التفتيش الداخلية.
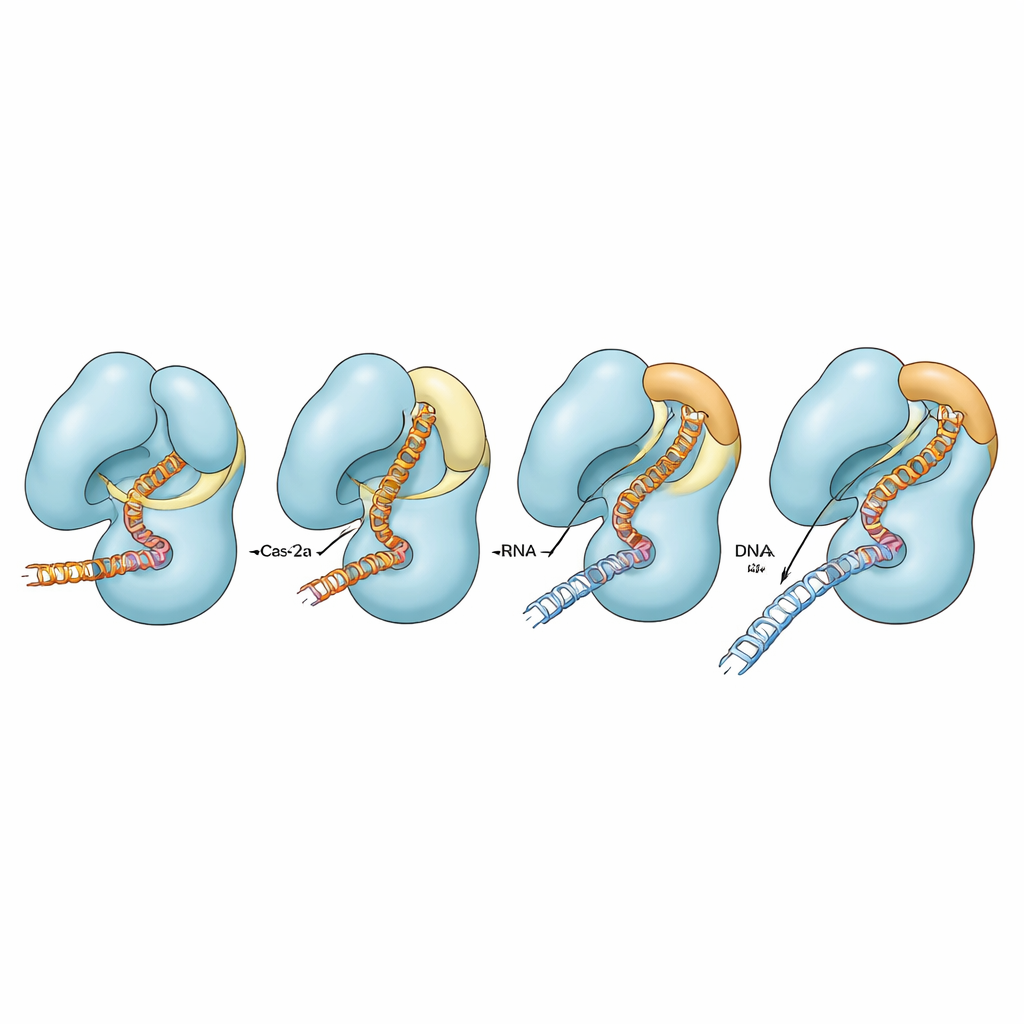
تحسين الدقة عن طريق تعديل التلامسات
لاختبار كيفية مساهمة التلامسات المختلفة حول الغطاء وحلزون الجسر في النشاط، غيّر المؤلفون بقايا مشحونة محددة تربط هذه المناطق. في Cas12a الطبيعي، كان لتفكيك هذه التلامسات تأثيرات طفيفة فقط على قطع الحمض النووي المطابق تمامًا، رغم أن بعض الحالات أثرت على كفاءة قطع السلسلة الثانية من الحمض النووي عندما وُجدت اختلافات. في خلفية حلزون الجسر المتضررة، قلّلت نفس الاستبدالات بشكل حاد أو كادت تُلغي قطع كلا السلسلتين، خاصة عندما لم يتطابق الدليل والحمض النووي تمامًا. دعمت المحاكاة الحاسوبية هذه النتائج، مبينة أنه فقط عندما يستطيع حلزون الجسر تبنّي شكله الحلزوني الكامل تتحرك الجسر والحلزون المجاور والغطاء والمواد النووية بطريقة منسقة بقوة. عندما يتعرض الحلزون للتلف، تصبح هذه الحركات مفصولة جزئيًا أو كليًا، ويكافح الإنزيم لإكمال دورة التحفيز.
دليل تصميم لأدوات CRISPR من الجيل التالي
بشكل عام، تكشف هذه الدراسة أن حلزون الجسر يعمل كرافعة تحكم داخلية تربط طول وجودة هجين RNA–DNA بفتح جيب القطع في Cas12a. بفرض أن يُكمل البروتين سلسلة محددة من تغيّرات الشكل قبل أن يقطع الحمض النووي، يفرض هذا الآلية بشكل طبيعي تمييز الاختلافات في التسلسل. تساعد النتائج على تفسير سبب قدرة التغييرات المستهدفة في هذه المنطقة الصغيرة على إنتاج متغيرات Cas12a تقلل القطع خارج الهدف وتخفف النشاط «التبعي» للحمض النووي، وهي خصائص مرغوبة لتحرير الجينات والتشخيصات الآمنة. وعلى نطاق أوسع، تبرز الدراسة كيف أن التحولات الطفيفة في هياكل حلزونية قصيرة يمكن أن تنسق اتصالات بعيدة المدى في الآلات الجزيئية الكبيرة، مما يقدم مبادئ عامة لهندسة إنزيمات معالجة الأحماض النووية عالية الدقة.
الاستشهاد: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
الكلمات المفتاحية: CRISPR-Cas12a, دقة تحرير الجينات, حلزون الجسر, تشكّل حلقة R, تنظيم كلوسي