Clear Sky Science · ar
نيوبريسيس: تحسين توقع استجابة العلاج المناعي من خلال دمج حدة المناعية والوعي بالتغايرية اللمسية لمشهد النيوأنتيجينات
لماذا تستجيب بعض السرطانات للعلاج المناعي وأخرى لا تستجيب
غيّر العلاج المناعي علاج السرطان جذرياً، لكنه ما يزال لا يفيد كثيراً من المرضى ويعرض بعضهم لآثار جانبية خطيرة. سؤال كبير هو لماذا تُرى بعض الأورام وتُدمر بواسطة الجهاز المناعي بينما تتسلّل أخرى دون أن تُكشف. تُقدّم هذه الدراسة طريقة حسابية تسمى نيوبريسيس، تَفحَص عن كثب «العلامات» التي يعرضها الورم على الجهاز المناعي — والمعروفة بالنيوأنتيجينات — وتستخدم تلك المعلومات للتنبؤ بشكل أدق بمن المرجح أن يستجيب للعلاجات المناعية الحديثة.
علمات جديدة على خلايا السرطان
تتراكم طفرات في الحمض النووي لخلايا السرطان يمكن أن تغير البروتينات التي تصنعها. أجزاء صغيرة من هذه البروتينات المتغيرة، المعروفة بالنيوأنتيجينات، يمكن عرضها على سطح الخلية ويُدركها الخلايا التائية باعتبارها أجنبية. لسنوات اعتمد الأطباء والباحثون على مقاييس غليظة مثل عبء الطفرات في الورم — العدد الكلي للطفرات — لتقدير مدى احتمال استجابة السرطان لمثبطات نقاط التفتيش المناعية. لكن هذا مقياس تقريبي: ليست كل طفرة تُنتج هدفاً مرئياً أو جذاباً للخلايا التائية، والأورام قد تكون عبارة عن خليط من أنواع خلوية متعددة. صُمِّم نيوبريسيس لينتقل إلى ما هو أبعد من عد الطفرات ويقيّم بدلاً من ذلك كم منها يعتبر هدفاً واعداً بالفعل عبر الورم بأكمله.
النظر في ثلاثة مكوّنات رئيسية معاً
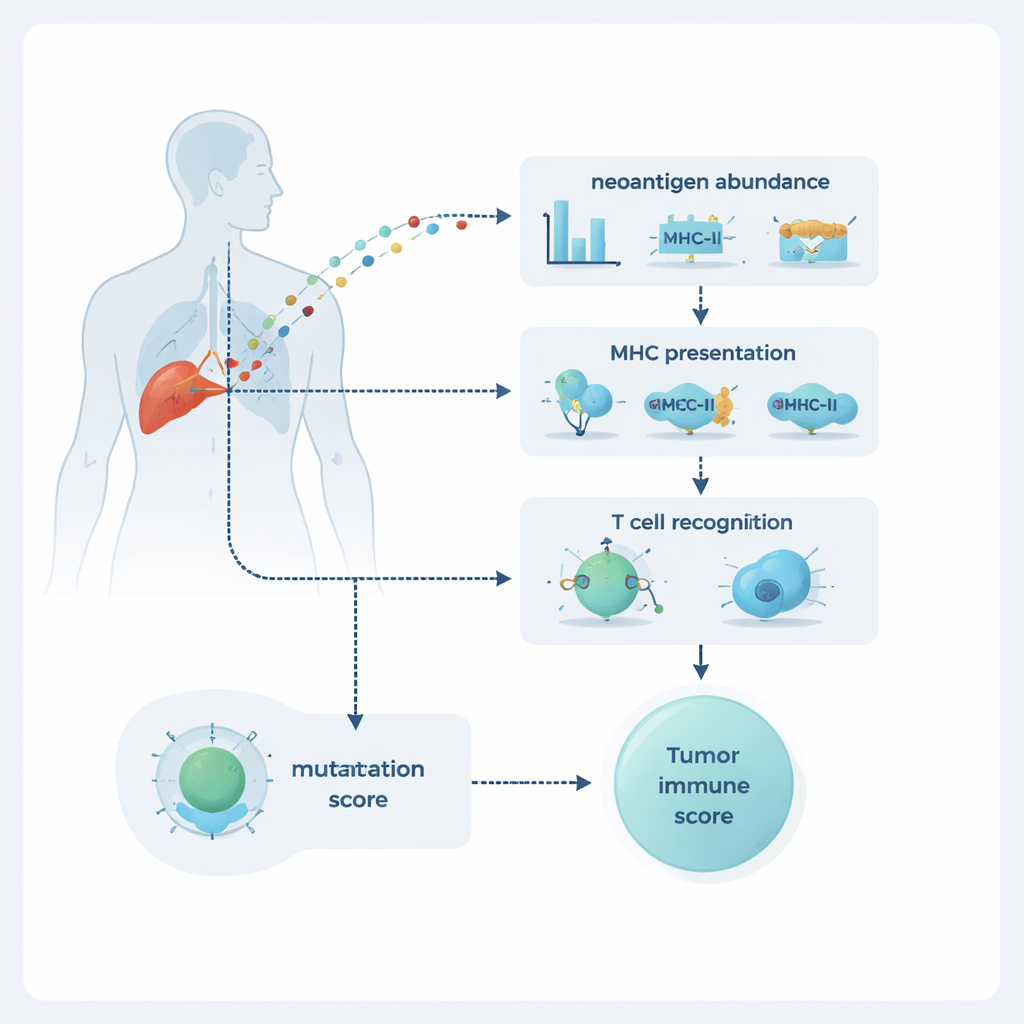
يقيم نيوبريسيس كل طفرة عبر ثلاثة أبعاد: مدى وفرتها في الورم، وما إذا كانت مرجّحَة أن تُعرض على سطح الخلية، ومدى احتمالية أن تُلاحظها الخلايا التائية. تُقدَّر الوفرة من خلال تسلسل الحمض النووي والحمض النووي الريبي، الذي يكشف مدى شيوع الطفرة ومدى تعبيرها. يُنمذج العرض عبر الارتباط بجزيئات تُسمى MHC من الصنف الأول والثاني، التي تعمل كلوحات إعلانية تعرض شظايا البروتين للخلايا التائية. الجزء الأكثر حداثة هو مكوّن تعرف الخلايا التائية، NeoPrecis-Immuno. يتعلم هذا النموذج من قواعد بيانات كبيرة للتفاعلات المعروفة بين الخلايا التائية والببتيدات ليقيس مدى اختلاف الشظية المطوِّرة عن نظيرتها الطبيعية بطريقة تهم تعرف الخلايا التائية، مع الأخذ بعين الاعتبار أيضاً أنواع MHC المحددة التي يحملها كل شخص.
تعليم الحاسوب ما «تراه» الخلايا التائية
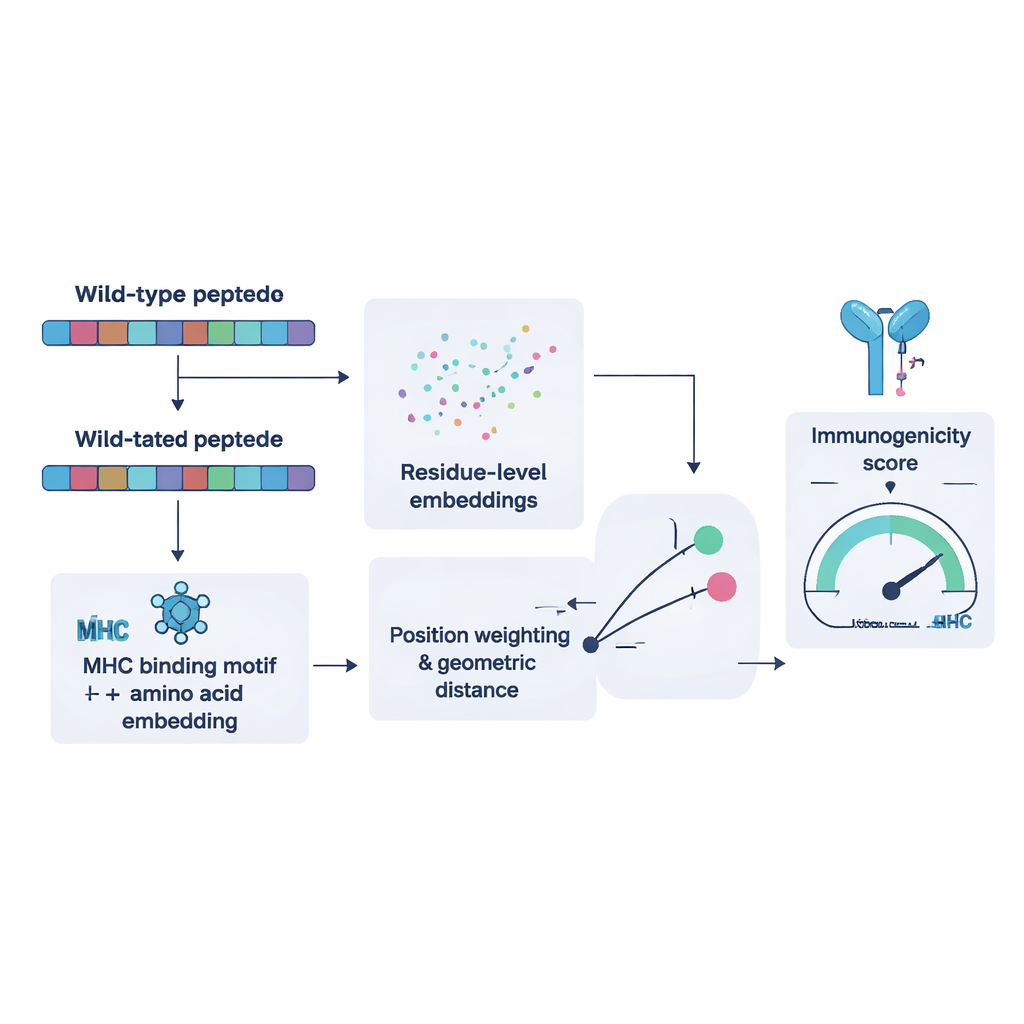
لتدريب NeoPrecis-Immuno، جمع الباحثون أولاً آلاف الأمثلة حيث تتعرف نفس الخلية التائية على ببتيدات متشابهة متعددة وأمثلة أخرى لا تتعرف عليها. استخدموا هذه الأمثلة ليعلّموا النموذج أن الشظايا المطوَّرة التي تشبه كثيراً الشظايا الطبيعية أقل احتمالاً أن تثير هجوماً مناعياً، لأن الأهداف الشبيهة بالذات عادةً ما تُستبعد خلال تطور الخلايا التائية. يمثل النموذج كل ببتيد كنقطة في فضاء رياضي يتشكّل بواسطة التسلسل الأميني وتفضيلات الارتباط لجزيئات MHC لدى الشخص. ثم يقيس مدى بُعد الببتيد المطوَّر عن الأصلي. المسافات الأكبر، المستنيرة بالنمط، تتوافق مع احتمال أعلى لأن تكون المناعية. عند اختباره مقابل أدوات موجودة على مجموعات بيانات مستقلة للسرطان، وطأ NeoPrecis-Immuno مثيلاتها أو تفوّق عليها، خصوصاً عند العمل مع MHC من الصنف الثاني، الذي يعرض للمساعدات التائية التي تدعم وتستدام الاستجابات المضادة للورم.
من الطفرات الفردية إلى الورم بأكمله
الطفرات المفردة جزء من القصة فقط؛ فطريقة توزيعها داخل الورم مهمة أيضاً. بعض الطفرات «نسيلية» (كلونية)، توجد في قرابة كل خلية سرطانية، في حين أن أخرى «فرعية النَمُو» (تحت كلونية)، حاضرة فقط في جيوب محددة. يبني نيوبريسيس «مشهد النيوأنتيجينات» بجمع درجات قابليتها المناعية عبر الطفرات وإضافة معلومات عن أي تفرعات خلوية تنتمي إليها وما مدى شيوع تلك التفرعات. هذا ينتج درجات على مستوى الورم تُبرز السرطانات الغنية بنيوأنتيجينات قوية ومشتركة على نطاق واسع — خاصة تلك التي يمكن عرضها على كل من MHC من الصنف الأول والثاني وقد تحفز استجابات منسقة من خلايا المساعدة والقاتلة التائية. في مجموعات المرضى المصابين بالميلانوما وسرطان الرئة غير صغير الخلايا المعالجين بمثبطات نقاط التفتيش، فصلت الدرجات المستندة إلى نيوبريسيس المستجيبين عن غير المستجيبين بدقة أكبر من عد الطفرات القياسي، وكانت مفيدة بشكل خاص في أورام الرئة المعقدة والمتغايرة.
ماذا يعني هذا للمرضى
بالنسبة للمرضى، تكمن وعد نيوبريسيس في مطابقة أكثر دقة للعلاج المناعي مع من المرجح أن يستفيدوا منه، وفهم أوضح لماذا تقاوم بعض الأورام العلاج. من خلال التركيز على جودة وتوزيع النيوأنتيجينات — وليس فقط كميتها — يساعد الإطار على تفسير سبب اختلاف سلوك الأورام التي لديها أحمال طفرية متشابهة. في المستقبل، قد تُوجّه مثل هذه الخرائط المفصّلة للمشهد المرئي مناعياً للورم ليس فقط لاستخدام مثبطات نقاط التفتيش، بل أيضاً لتصميم لقاحات سرطانية مخصصة تُعطي الأولوية لأقوى الأهداف والأكثر شيوعاً داخل كل سرطان لدى كل شخص.
الاستشهاد: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
الكلمات المفتاحية: العلاج المناعي للسرطان, النيوأنتيجينات, تغايرية الورم, مثبطات نقاط التفتيش, الأونكولوجيا الحاسوبية