Clear Sky Science · ar
تعزيز Stenotrophomonas لتقدم أورام الجهاز الهضمي عبر تحلل STING في الخلايا الورمية وتخفيف الاستجابة المناعية
جراثيم خفية داخل الأورام
سمع معظم الناس أن الميكروبات في أمعائنا يمكن أن تؤثر على الهضم وحتى المزاج، لكن قلة يدركون أن بكتيريا حية قد تستقر فعليًا داخل الخلايا السرطانية نفسها. تكشف هذه الدراسة كيف أن بكتيريا بيئية شائعة، Stenotrophomonas، تختبئ داخل أورام الجهاز الهضمي وتساعدها بهدوء على النمو، بينما تُضعف في الوقت نفسه دفاعات الجسم المناعية وتجعل العلاجات المناعية الحديثة أقل فعالية.
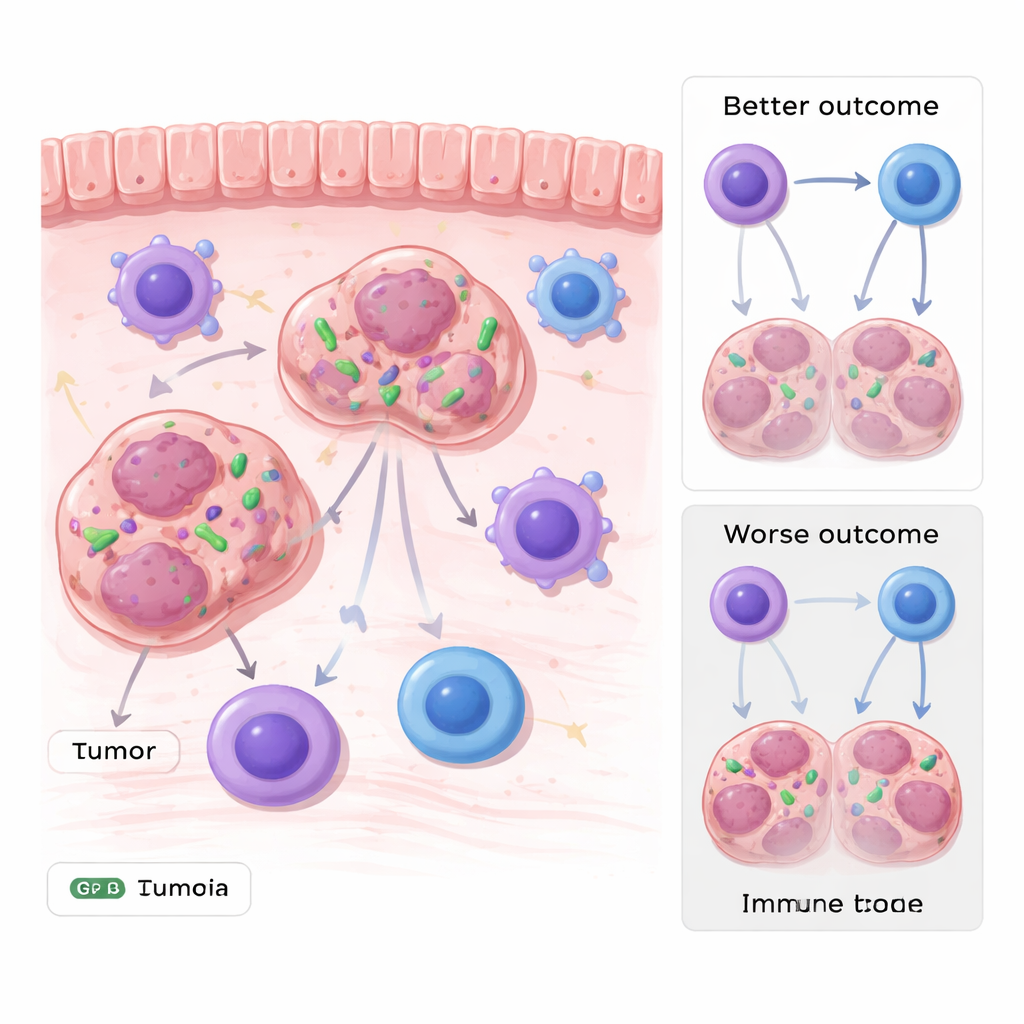
بكتيريا تعيش داخل الخلايا السرطانية
تنمو أورام الجهاز الهضمي، مثل سرطانات المعدة والقولون والمستقيم، على تماس دائم مع مجتمعات بكتيرية غنية في القناة الهضمية. من خلال تحليل مجموعات بيانات جينية متعددة من مرضى والتحقق من النتائج في عينات أورامية، وجد الباحثون أن حمضًا نوويًا من Stenotrophomonas كان وفيرًا بشكل غير اعتيادي داخل عدة أنواع من أورام الجهاز الهضمي. والأهم من ذلك أن وجودها لم يكن مجرد تلوث سطحي: كشفت طرق التصوير، بما في ذلك المجسات الفلورية والمجهر الإلكتروني، عن بكتيريا كاملة جالسة داخل سيتوبلازم الخلايا الورمية. المرضى الذين احتوت أورامهم مستويات أعلى من هذه البكتيريا كانوا يميلون إلى نتائج أسوأ مع مرور الوقت، مما يربط الميكروب بتوقع أسوأ للمآل.
كيف يزيح ميكروب ميزان المناعة
سأل الفريق بعد ذلك ما إذا كانت هذه البكتيريا المخفية مجرد مصادفة مع أورام عدوانية أم أنها تساهم فعليًا في دفع المرض. في نماذج الفئران، أصابوا الخلايا الورمية بـ Stenotrophomonas الموسومة فلوريًا قبل زرعها في الحيوانات. نمت الأورام التي حملت البكتيريا أسرع وأكبر من تلك التي بدونها، عبر عدة أنواع من الخلايا السرطانية. عند فحص المشهد المناعي المحيط، وجدوا أن الأعداد الإجمالية للخلايا المناعية، بما في ذلك الخلايا التائية والبلعمية، كانت متشابهة. الاختلاف الحاسم كان في مجموعة متخصصة من البلعمات التي تُظهر جزيئًا يسمى MHC-II، وهو ما يساعدها على عرض شظايا الورم لخلايا T القاتلة. في الأورام المحتوية على Stenotrophomonas، انخفضت البلعمات موجبة MHC-II بشكل ملحوظ، وأظهرت الخلايا التائية نشاطًا قاتلًا أقل للسرطان.
اختصار نظام إنذار خلوي
لفهم الآلية، ركز الباحثون على مسار إنذار رئيسي داخل الخلايا يعرف باسم STING، الذي يكتشف عادةً الحمض النووي الأجنبي ويحفز إفراز إشارات «الخطر» المضادة للفيروسات المسماة الإنترفيرونات من النوع الأول. في تجارب المختبر، أنتجت الخلايا الورمية المصابة بـ Stenotrophomonas كمية أقل بكثير من الإنترفيرون بيتا، وكانت الجينات التي يُفترض أن يُشغلها هذا المسار أخف نشاطًا. أظهرت الدراسة أن البكتيريا تتسبب في إجهاد لـمَصنع طي البروتينات داخل الخلية، الشبكة الإندوبلازمية، ثم تختطف مسار مراقبة الجودة المسمى التحلل المرتبط بالشبكة الإندوبلازمية (ER-associated degradation). عبر مساعد بروتيني يُدعى SEL1L، يوسم هذا المسار بروتين STING للتدمير في مُحطِّم البروتينات الخلوية، البروتيازوم. مع استنزاف مستويات STING، ترسل الخلية الورمية إنذارًا أضعف، ما يؤدي إلى انخفاض الإنترفيرون وبشكل تبعي ضعف تنشيط البلعمات موجبة MHC-II.
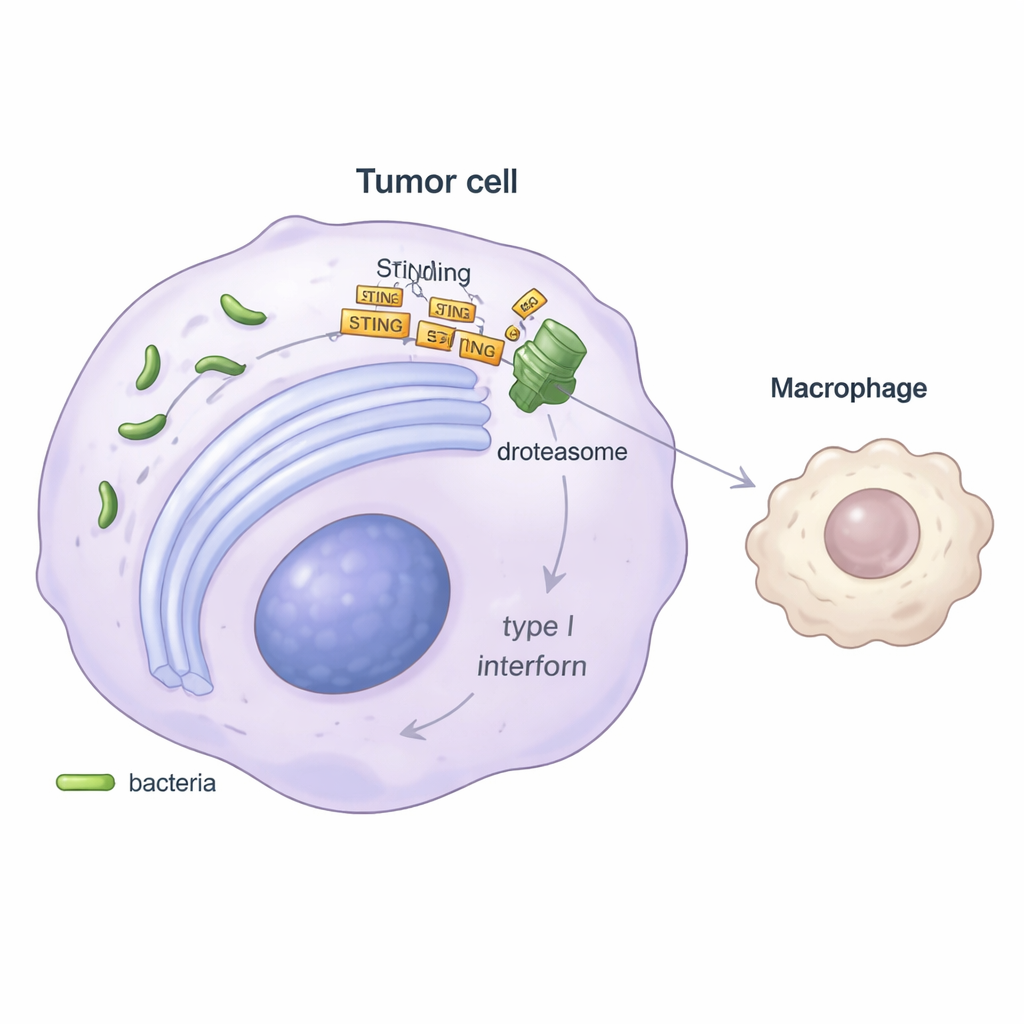
تقويض العلاج المناعي—وحل محتمل
نظرًا لأن العلاجات المناعية الحديثة مثل أدوية مضادة لـ PD-1 تعتمد على استجابات قوية للخلايا التائية، اختبر الفريق كيف تؤثر Stenotrophomonas داخل الخلايا على العلاج. في الفئران، استجابت الأورام الحاملة للبكتيريا بشكل سيئ للعلاج بمضاد PD-1 مقارنة بالأورام الخالية من البكتيريا، حتى عند الجمع مع العلاج الكيميائي. أظهرت الخلايا التائية في هذه الأورام علامات نشاط وانقسام أقل، بما يتوافق مع تحفيز مناعي ضعيف. واللافت أنه عندما عالج الباحثون الحيوانات بالمضاد الحيوي ليفوفلوكساسين، الذي يقتل Stenotrophomonas بفعالية، تباطأ نمو الورم وتحسَّنت الاستجابة لعلاج مضاد PD-1. كما أن استعادة إشارة الإنترفيرون عبر دواء إنترفيرون سريري تمكنت أيضًا من إنعاش مجموعة البلعمات مفيدة الوظيفة موجبة MHC-II وإعادة فاعلية قتل الخلايا التائية في بعض الحالات، مما يؤكد الدور المحوري لهذا المسار.
ماذا يعني هذا للمرضى
للقارئ غير المختص، الرسالة الأساسية هي أن بعض سرطانات الجهاز الهضمي قد تكون «مسلحة» بميكروبيوم داخلي يساعدها على الهروب من الهجوم المناعي. تقوم Stenotrophomonas، عبر تحلل نظام إنذار STING داخل الخلايا الورمية، بتخفيف الإشارات المناعية التي عادة ما تستدعي البلعمات والخلايا التائية القاتلة. هذا لا يسرع نمو الورم فحسب، بل قد يفسر أيضًا لماذا يفشل بعض المرضى في الاستفادة من علاجات مناعية قوية. على الرغم من الحاجة إلى مزيد من العمل قبل أن يغير ذلك الممارسة السريرية، تثير النتائج احتمال اختبار الأورام بحثًا عن مثل هذه البكتيريا—وعلاجها انتقائيًا بمضادات حيوية مستهدفة أو أدوية تثبت STING—كوسيلة قد تحسّن نتائج المرضى المصابين بسرطان المعدة والقولون والمستقيم في المستقبل.
الاستشهاد: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
الكلمات المفتاحية: ميكروبيوم الورم, سرطان الجهاز الهضمي, Stenotrophomonas, مسار STING, العلاج المناعي للسرطان