Clear Sky Science · ar
هندسة نظام MmeFz2-ωRNA لتحرير الجينوم بكفاءة عبر إطار متكامل حاسوبي-تجريبي
مقصات جينية أصغر لمشكلات طبية كبيرة
غيّر تحرير الجينات بالفعل طريقة دراسة العلماء للأمراض، لكن تحويله إلى دواء آمن وعملي لا يزال تحدياً كبيراً. إحدى العوائق الرئيسية أن أقوى «مقصات» الحمض النووي الحالية، مثل CRISPR-Cas9، كبيرة جسدياً ويصعب تعبئتها داخل ناقلات التوصيل الصغيرة المستخدمة في المرضى. تُقدّم هذه الدراسة أداة جديدة ومضغوطة لتحرير الجينات مبنية على عائلة إنزيمات أقل شهرة تُسمى Fanzor2، وتُظهر كيف يمكن للذكاء الاصطناعي إعادة تصميمها بسرعة لتصبح مرشحاً قوياً للعلاجات الجينية المستقبلية.
فئة جديدة من محررات الجينوم المدمجة
معظم محررات الجينوم الحالية، مثل Cas9 وCas12a، هي بروتينات ضخمة تتألف من أكثر من ألف وحدة بناء. وهذا الحجم يجعل من الصعب ضغطها داخل الفيروسات المرتبطة بالكبادرة (AAV)، وهي نظام التوصيل الرائد للعلاجات الجينية. بالمقابل، بروتينات Fanzor2 أصغر بكثير وتوجد طبيعياً في حقيقيات النوى، فرع الحياة الذي يشمل الحيوانات والبشر. ركز المؤلفون على عضو واحد من هذه العائلة، MmeFz2، الذي يستخدم جزيئاً RNA قصيراً يسمى ωRNA لتحديد وقطع تسلسلات DNA محددة. على الورق بدا MmeFz2 مثالياً للعلاج: مدمج وقابل للبرمجة. لكن عملياً، كان نشاطه في الخلايا البشرية ضعيفاً للغاية، حيث عدّل أقل من واحد بالمئة من المواقع المستهدفة. انطلق الفريق لتحويل هذا الإنزيم غير الفعال إلى أداة عملية.
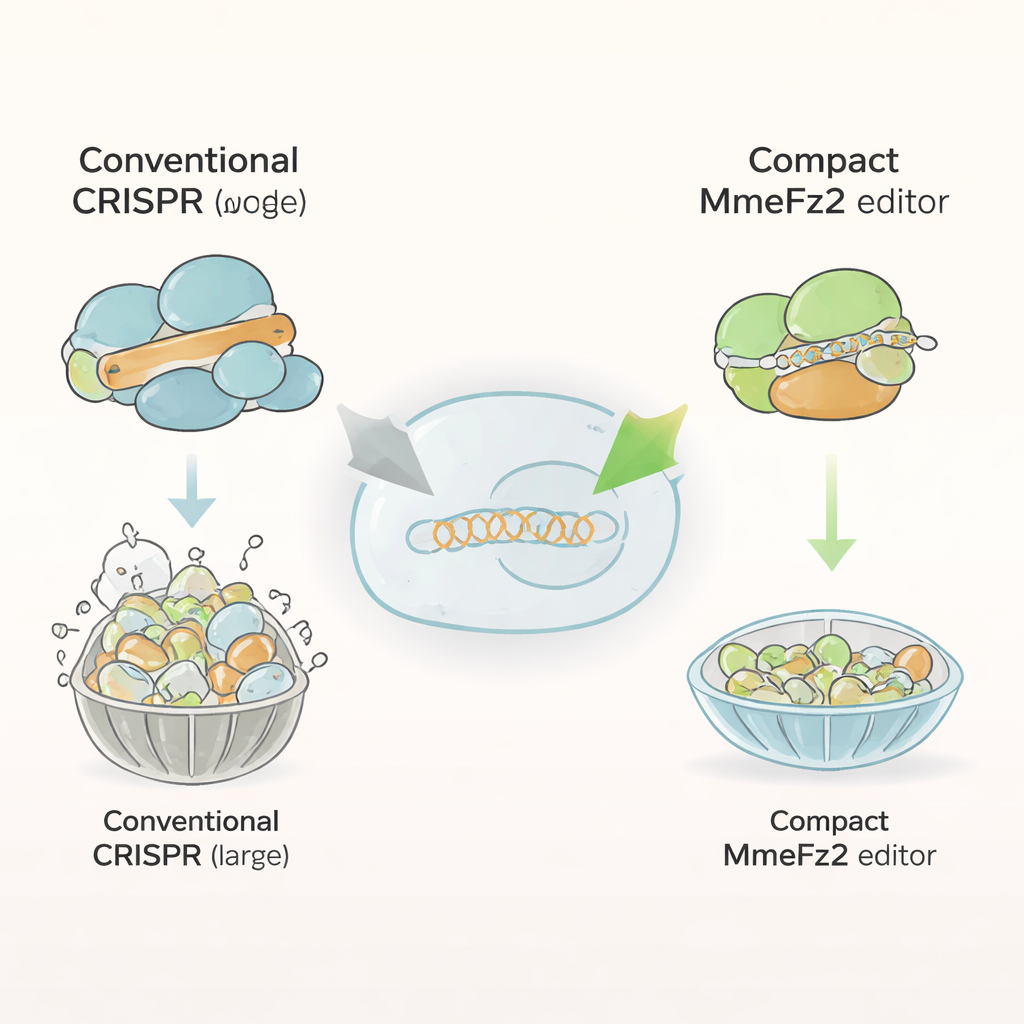
استخدام الذكاء الاصطناعي لإعادة تصميم جزيء الدليل
كان الهدف الأول هو ωRNA، الدليل الذي يخبر MmeFz2 أين يقطع. باستخدام AlphaFold3، برنامج متقدم يتنبأ بالهياكل ثلاثية الأبعاد لمجمعات البروتين–RNA–DNA، بنى الباحثون نموذجاً لـ MmeFz2 مرتبطاً بـ ωRNA وبتسلسل DNA مستهدف. كشفت هذه البنية الافتراضية أن أجزاءً من ωRNA كانت مرنة، ضعيفة الاقتران، ولا تلامس البروتين إلا بشكل طفيف. مسترشدين بهذه المعلومات، استبدل الفريق بشكل منهجي الوصلات غير المستقرة في الـ RNA وأزال سلاسل قواعد اليوريدين التي يمكن أن تتداخل مع النسخ. ثم اختبروا العشرات من المتغيرات في خلايا بشرية. من خلال تجميع أفضل التعديلات وتقليص منطقة سيخ غير ضرورية، أنشأوا ωRNA مختصراً أصغر بحوالي 30% ومع ذلك قدّم زيادة تقارب عشرين ضعفاً في كفاءة التحرير عبر مواقع DNA عديدة.
ضبط دقيق للبروتين باستخدام تعلم الآلة
بعد ذلك حسّن الفريق البروتين نفسه. استخدموا مرة أخرى AlphaFold3 لتخطيط مواضع تلامس MmeFz2 مع RNA وDNA وصمموا أكثر من مائة تغيير في حمض أميني واحد بهدف تقوية تلك التلامسات أو تحسين المرونة. بعد فحص هذه الطفرات في الخلايا، أدخلوا بيانات الأداء إلى EVOLVEpro، نظام تعلم آلي مبني على نماذج لغة البروتينات المدربة على ملايين التسلسلات الطبيعية. تعلّم هذا الأداة أي الميزات تميل إلى زيادة النشاط واقترحت تراكيب جديدة من الطفرات يُتوقع أن تعمل بشكل أفضل. من خلال عدة جولات من حلقة الحوسبة–التجريب هذه، توصل العلماء إلى متغيرين محسّنين للإنزيم، اللذين، عند اقترانهما مع ωRNA المحسّن، رفعا نشاط التحرير بأكثر من 60 ضعفاً مقارنة بالنظام الابتدائي.
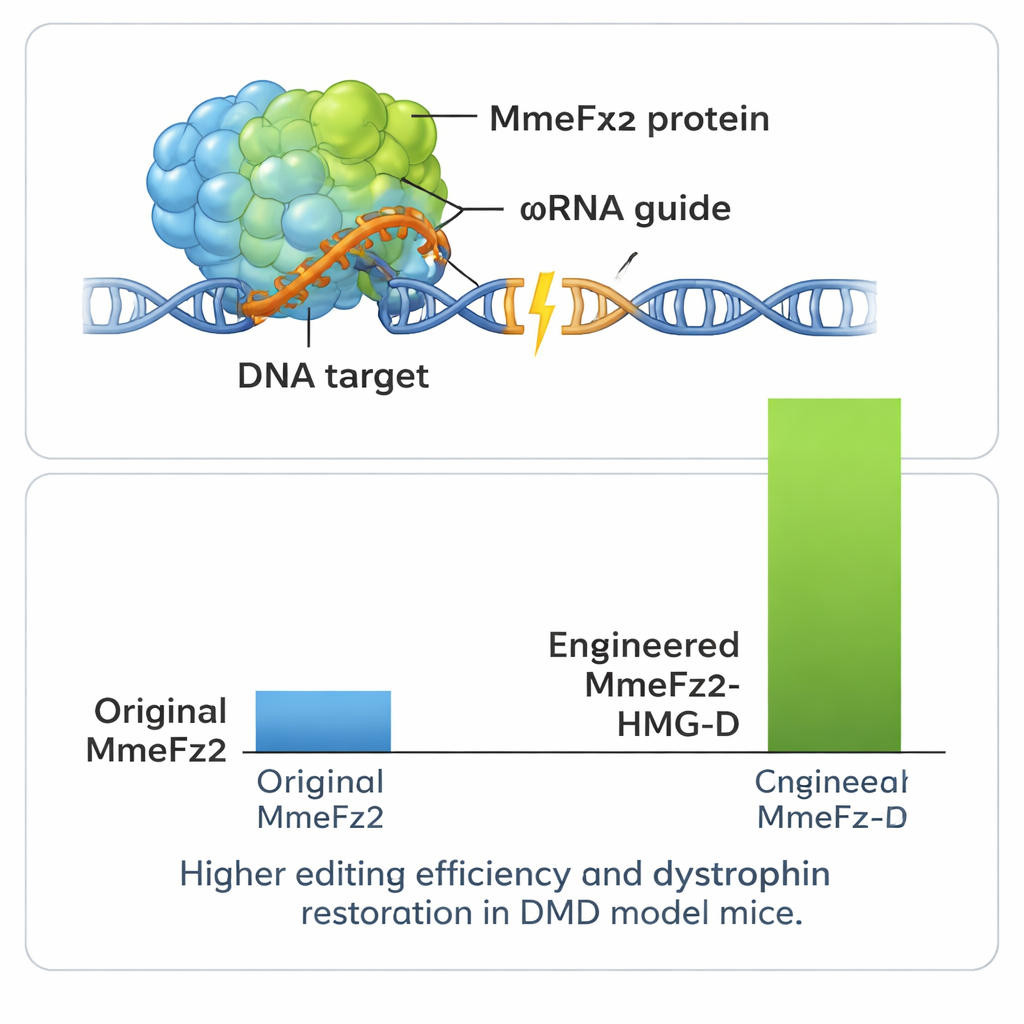
زيادة القوة والاختبار في نموذج مرضي
لاستخراج أداء أكبر من النظام، لُصق الباحثون MmeFz2 إلى نطاقات ربط DNA صغيرة تساعد البروتينات على الالتصاق بالمادة الوراثية. أثبت أحد هذه النطاقات، المسمى HMG-D، فعاليته بشكل خاص عند ربطه في نهاية الإنزيم المهندَس، مما أدى إلى مستويات تحرير تجاوزت 80% في بعض المواقع. والأهم أن الاختبارات في مواقع محتملة خارج الهدف في الجينوم أظهرت أن هذه القوة الإضافية لم تُرافقها خسارة كبيرة في الدقة. وبما أن محرر الجين بأكمله — بما في ذلك البروتين وRNA الدليل — صغير جداً، فإنه يتسع بسهولة داخل ناقل AAV واحد، وهو ما لا يمكن تحقيقه مع معظم أنظمة CRISPR. استغل الفريق هذه الميزة في نموذج فأر لمرض حثل الضمور العضلي دوشن، وهو اضطراب قاتل يسبب ضمور العضلات ناجم عن طفرات في جين الديسترُوفين. أدى حقن واحد للعضل بسائل AAV المحمول بالمحرر إلى تصحيحات قابلة للكشف في RNA الجيني واستعادة بروتين الديستروفين في جزء كبير من ألياف العضلات.
ما معنى هذا لعلاجات الجينات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن المؤلفين حولوا إنزيم قطع جيني ضعيفاً وغير معروف إلى محرر مدمج عالي الأداء يمكن توصيله في عبوة فيروسية واحدة ويمكنه إصلاح مرض وراثي خطير في نموذج حيواني واقعي. ولا تقل أهمية الطريقة المستخدمة عن النتيجة نفسها: عبر الجمع الوثيق بين التنبؤ الهيكلي المعتمد على الذكاء الاصطناعي وتعلم الآلة مع تجارب مخبرية مركزة، حسّنوا كلاً من البروتين وRNA الدليل بكفاءة أكبر بكثير من الأساليب التقليدية القائمة على التجربة والخطأ. قد تسرّع هذه الإستراتيجية المتكاملة إنشاء العديد من محررات الجينوم من الجيل القادم، مما يقرب علاجات جينية أكثر دقة وأمناً للمرضى المصابين بحثل الضمور العضلي وحالات وراثية أخرى.
الاستشهاد: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
الكلمات المفتاحية: تحرير الجينات, بدائل CRISPR, حثل ضموري دوشن, العلاج الجيني الفيروسي, الذكاء الاصطناعي في علم الأحياء