Clear Sky Science · ar
القضاء المعتمد على C1q على ألفا-سينوكلين يسمح للبلعميات بتقييد السِّينوكلينوپاثي المع enteric مؤقتًا في ذكور الفئران
لماذا يهمّ القولون في أمراض الدماغ
يشتهر مرض باركنسون بالرجفات ومشاكل الحركة، لكن الكثير من الأشخاص يعانون سنوات من الإمساك الحاد ومشكلات معوية أخرى قبل ظهور أي أعراض حركية. تستكشف هذه الدراسة ما يحدث في "الدماغ الثاني" للجسم—شبكة الأعصاب في الأمعاء—عندما يطرأ طيّ خاطئ لبروتين مرتبط بباركنسون هناك، وكيف تساعد خلايا المناعة المحلية في البداية ثم تنهار. قد يفتح فهم هذا الصراع المبكر في الأمعاء طرقًا جديدة لتخفيف الأعراض وربما إبطاء تقدم المرض قبل أن يتعرض الدماغ لضرر كبير.
بروتين إشكالي في الدماغ الثاني للجسم
في مرض باركنسون والاضطرابات ذات الصلة، يمكن أن يطرأ طيّ خاطئ على بروتين يُدعى ألفا-سينوكلين ويتجمع إلى عقيدات سامة. توجد هذه التجمعات ليس فقط في الدماغ بل أيضًا في جميع أنحاء الجهاز العصبي المعوي، الشبكة العصبية التي تتحكم بحركة الأمعاء. يشتبه كثير من الباحثين أن ألفا-سينوكلين المطوي خطأً قد يبدأ في الأمعاء لدى بعض المرضى ثم ينتشر تجاه الدماغ على طول المسارات العصبية. استخدم المؤلفون نموذجًا فأريًا تُحقن فيه خيوط ألفا-سينوكلين المُشكّلة مسبقًا في المعدة والجزء العلوي من الأمعاء الدقيقة. على مدار الشهرين التاليين راقبوا زيادة مستمرة في ألفا-سينوكلين الشاذ والموسوم كيميائيًا داخل عصبونات الأمعاء. تزامن هذا التراكم مع بطء حركة المحتوى عبر الأمعاء وانخفاض إخراج البراز، ما يعكس الإمساك الذي تلاحظه العديد من حالات باركنسون.
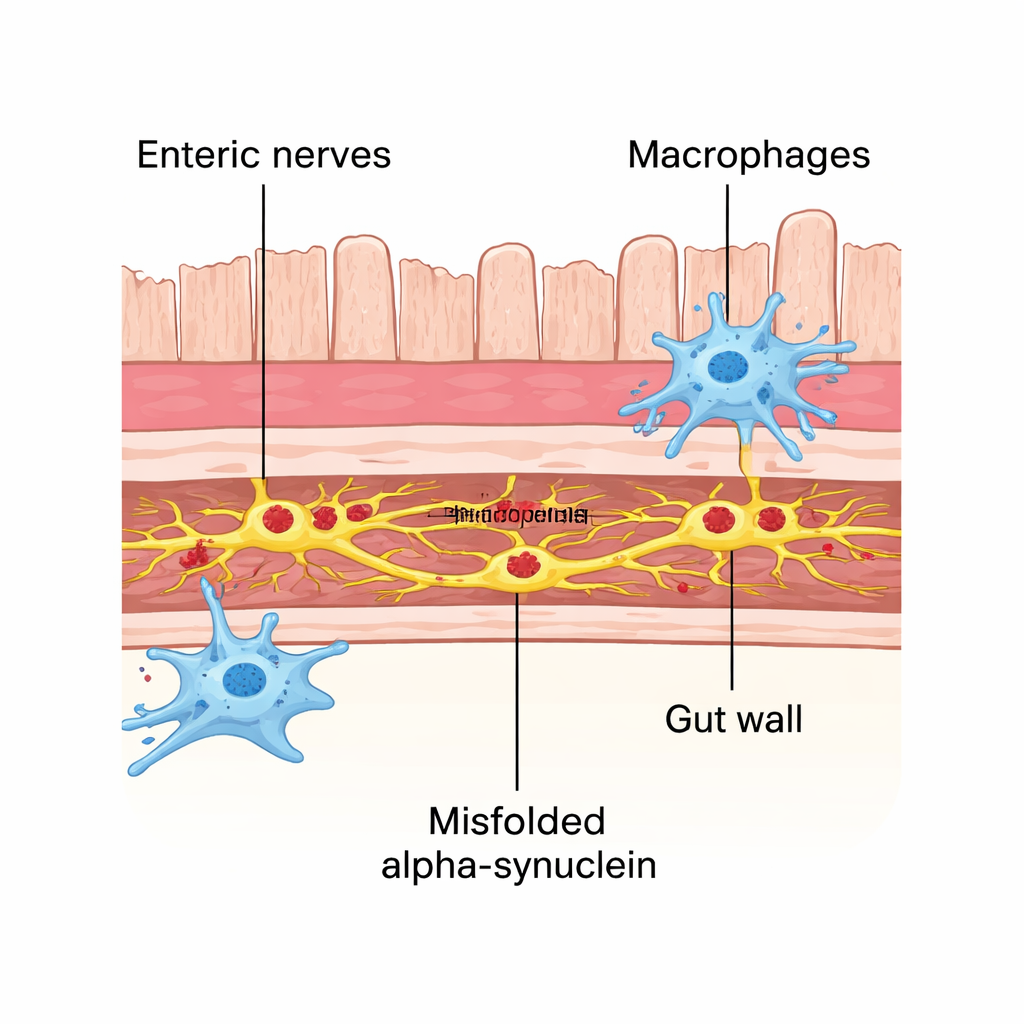
خلايا المناعة المعوية تتدخل كمستجيبين أوائل
تحتوي جدار الأمعاء على خلايا مناعية مقيمة تُدعى البلعميات (البلعميات الحِبَيْبية) التي تتواصل باستمرار مع الأعصاب المجاورة وتساعد في الحفاظ على صحة النسيج. في هذا النموذج، قامت هذه البلعميات بأكثر من مجرد التفاعل مع الضرر: بل تلامست جسديًا مع تجمعات الأعصاب المتأثرة بشكل متكرر واحتوت داخلها نقاطًا صغيرة من البروتين المطوي خطأً. عندما استنزف الباحثون هذه البلعميات باستخدام علاج بأجسام مضادة، تفاقمت آفة ألفا-سينوكلين في عصبونات الأمعاء بشكل ملحوظ. يشير ذلك إلى أن بلعميات الأمعاء تلعب دورًا وقائيًا مبكرًا، تعمل كمنظفات خلوية تبتلع وتزيل البروتين السام من الخلايا العصبية القريبة قبل أن ينتشر.
وسم جزيئي يساعد — ويؤذي
لفهم كيفية تعرف هذه الخلايا المناعية على ما يجب إزالته، لجأ الفريق إلى تحليل RNA لخلايا مفردة، مستعرضين آلاف الخلايا المناعية المعوية الفردية. حددوا أنواعًا فرعية من البلعميات في طبقات العضلات للأمعاء قامت بتشغيل جينات مرتبطة بالابتلاع وتحطيم البروتين، لا سيما مكونات نظام المكمِّل—مسار وسم جزيئي معروف أكثر في مجرى الدم. كان عنصر رئيسي، C1q، نشطًا بكثافة في هذه البلعميات المعوية. تحت المجهر، غطَّى C1q العصبونات المعوية المتأثرة، واحتوت البلعميات على نقاط موجبة لكل من C1q وألفا-سينوكلين المطوي خطأً، ما يشير إلى أن C1q يساعد في وسم البروتين السام لإزالته. عندما استخدم العلماء فئرانًا معدلة وراثيًا تفتقر إلى C1q، ساءت آفة ألفا-سينوكلين العصبية وابتلعت البلعميات عددًا أقل من تجمعات البروتين. ومع ذلك، وبشكل مفاجئ، كان لدى هذه الفئران الخالية من C1q حركة معوية أفضل إلى حد ما من الفئران الطبيعية المعرضة لنفس الخيوط، ما يوحي بأن العملية نفسها التي تزيل البروتين السام يمكن أن تخلّ بوظيفة الأمعاء—على الأرجح عن طريق تقليم أو إضعاف الوصلات العصبية التي تتحكم بالحركة.
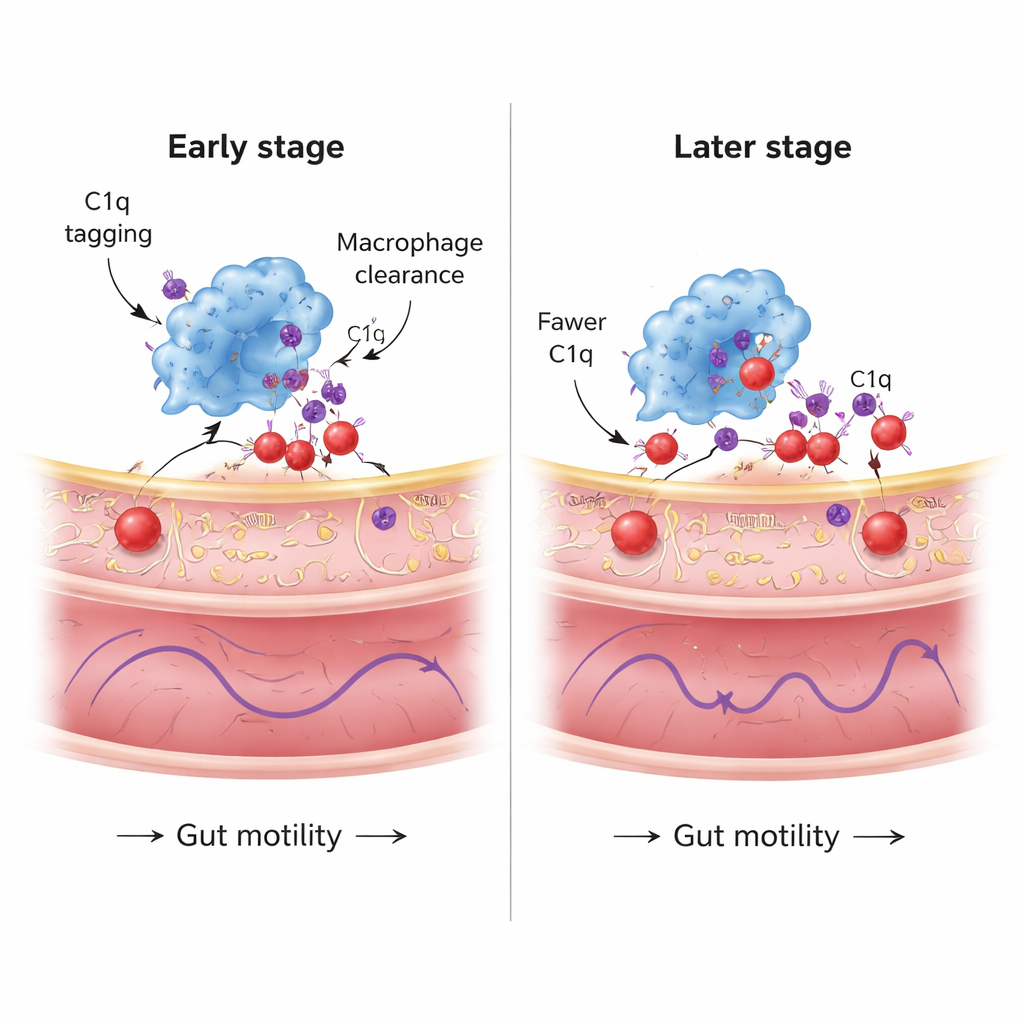
نظام وقائي يتلاشى مع الزمن
تابعت الدراسة أيضًا استجابة التنظيف هذه على مدى أطول. بعد نحو شهر من إدخال ألفا-سينوكلين، أظهرت البلعميات تعبيرًا قويًا عن C1q وعددًا كبيرًا من نقاط البروتين الموشومة بـC1q داخل أجسامها الخلوية، وكان C1q يكسو العصبونات المعوية بكثافة. لكن بحلول الشهر الثاني، رغم بقاء مستويات C1q العامة في البلعميات، انخفض عدد نقاط C1q/ألفا-سينوكلين المبتلعة وكمية C1q المودعة على العصبونات. وفي الوقت نفسه استمرت الآفة العصبية في الأمعاء بالازدياد. اقترحت تحليلات الجينات أن الالتقاط المستمر للبروتين المطوي خطأً يجهد آليات معالجة البروتين في البلعميات، مفعلًا مسارات إجهاد مرتبطة بالبروتينات المطوية خطأً والليسوزومات وحتى موت الخلايا. بعبارة أخرى، يبدو أن القدرة الوقائية للبلعميات محدودة: فهي تقيد الآفة في البداية، لكن مع تراكم الإجهاد يتناقص قدرتها على إزالة ألفا-سينوكلين.
ما الذي يعنيه هذا لباركنسون والأمعاء
تقدم هذه العمل صورة معقّدة لكيف تشكّل خلايا المناعة المعوية التغيرات المبكرة الشبيهة بباركنسون في الأمعاء. في البداية تساعد البلعميات المقيمة باستخدام C1q لوضع علامات وابتلاع ألفا-سينوكلين المطوي خطأً من عصبونات الأمعاء، محدودةً انتشاره. لكن هذا التقليم المدفوع بالمكمِّل قد يضعف الإشارة العصبية ويبطئ الأمعاء، مساهمًا في الإمساك. مع مرور الوقت يضعف نظام التنظيف المثقل بالإجهاد لدى البلعميات، مما يسمح لتراكم مزيد من الآفات حتى مع تباعد وظيفة الأمعاء وتورط الدماغ. بالنسبة للمرضى، يشير هذا إلى أن استهداف نشاط البلعميات أو إشارة المكمِّل في الأمعاء—بهدف تعزيز الإزالة الآمنة مع تجنُّب خسارة المشابك المفرطة—قد يكون في يوم من الأيام استراتيجية لعلاج أو منع أعراض الأمعاء المتعلقة بباركنسون وربما يؤثر على مسار المرض الأوسع.
الاستشهاد: Mackie, P.M., Koshy, J.M., Bhogade, M.H. et al. C1q-dependent clearance of alpha-synuclein allows macrophages to transiently limit enteric synucleinopathy in male mice. Nat Commun 17, 1877 (2026). https://doi.org/10.1038/s41467-026-68641-8
الكلمات المفتاحية: مرض باركنسون, الجهاز العصبي المعوي, ألفا-سينوكلين, خلايا المناعة المعوية, المكمِّل C1q