Clear Sky Science · ar
تقدير استقرار طي البروتين مع النظر الصريح في الحالات غير المطوية
لماذا يهم استقرار البروتين
كل بروتين في جسمك عبارة عن آلة جزيئية صغيرة يجب أن تطوى إلى شكل ثلاثي الأبعاد دقيق لتؤدي وظيفتها بشكل صحيح. إذا كان الطي هشاً جداً، فقد يخطئ البروتين في عمله، أو يتكتل مع بروتينات أخرى، أو يفشل في التكوّن تماماً — مشاكل ترتبط بالأمراض وبفشل تصنيع الأدوية والإنزيمات المبنية على البروتينات. قياس مدى استقرار البروتين في المختبر عملية بطيئة ومعقدة، لذا يبحث العلماء عن طرق حاسوبية يمكنها، من التسلسل وحده، أن تخبرنا بشكل موثوق مدى سهولة انفتاح البروتين.
نظرة جديدة إلى الحالات المطوية وغير المطوية
تركّز معظم الخوارزميات الحديثة تقريباً على الشكل المطوي للبروتين فقط. غالباً ما تبدأ ببنية متنبأ بها بواسطة الذكاء الاصطناعي، مثل تلك من AlphaFold، وتتعامل مع تلك البنية المفردة باعتبارها المحدد الرئيسي للاستقرار. لكن الاستقرار في الواقع هو فجوة الطاقة بين مجموعتين واسعتين: الحالة المطوية المدمجة والأشكال المتعددة المرنة التي تشكّل الحالة غير المطوية. يجادل المؤلفون بأن تجاهل الطرف غير المطوي من هذا التوازن هو سبب رئيسي في صعوبة مطابقة الأدوات الحالية لقياسات طاقة الطي التجريبية، المعروفة باسم ΔG.
نموذج جديد يتعلم الحالتين
يقدّم الباحثون نظام IFUM، وهو نظام تعلّم عميق مصمّم لتقدير ΔG مع تعلّم شكل توازن الحالات المطوية وغير المطوية لكل بروتين. بدلاً من اعتبار الحالة غير المطوية مجرد خلفية غامضة، يستخدم IFUM أفكاراً من فيزياء البوليمرات لتمثيلها كـ «لفافة عشوائية» ويشفّر كلتا الحالتين كخرائط للمسافات بين أزواج الأحماض الأمينية. يستقبل النموذج معلومات من شبكات قوية مُدربة مسبقاً على التسلسل والبُنية، ثم يتنبأ بشكل مشترك بالاستقرار الكلي وخريطة احتمالية تصف مقدار البروتين الموجود في الحالة المطوية مقابل غير المطوية عند كل زوج من الأحماض الأمينية. يساعد التدريب على مجموعة بيانات كبيرة جداً من البروتينات الصغيرة الموصوفة تجريبياً والبروتينات المعروفة بالاضطراب، IFUM على التعرّف على التسلسلات المهيكلة جيداً والمَرِنة على حد سواء.
أرقام أفضل وتغطية أوسع للطفرات
عند الاختبار على مجموعة بيانات مضبوطة بعناية من البروتينات الصغيرة، يتنبأ IFUM بقيم ΔG التجريبية بخطأ أقل وبتوافق أعلى مقارنة بأساليب الذكاء الاصطناعي السابقة التي تعتمد فقط على البنية المطوية أو على نماذج لغوية مدرّبة على التسلسلات. والأهم من ذلك، أن النموذج يتعامل أيضاً مع مجموعة واسعة من تغييرات التسلسل. يلتقط بدقة تأثيرات الطفرات النقطية المفردة والمزدوجة، وكذلك الإدخالات والحذوف التي تغيّر طول البروتين — أوضاع تفشل فيها العديد من الأدوات الحالية أو لم تُصمم للعمل فيها أصلاً. تُظهر مقارنة داخلية أن إزالة الهدف المتعلق بالحالة غير المطوية يفاقم الأداء بشكل كبير، مما يؤكد أن نمذجة التجمع غير المطوي صراحة ليست مجرد فكرة نظرية بل جوهرية لدقة التنبؤات.
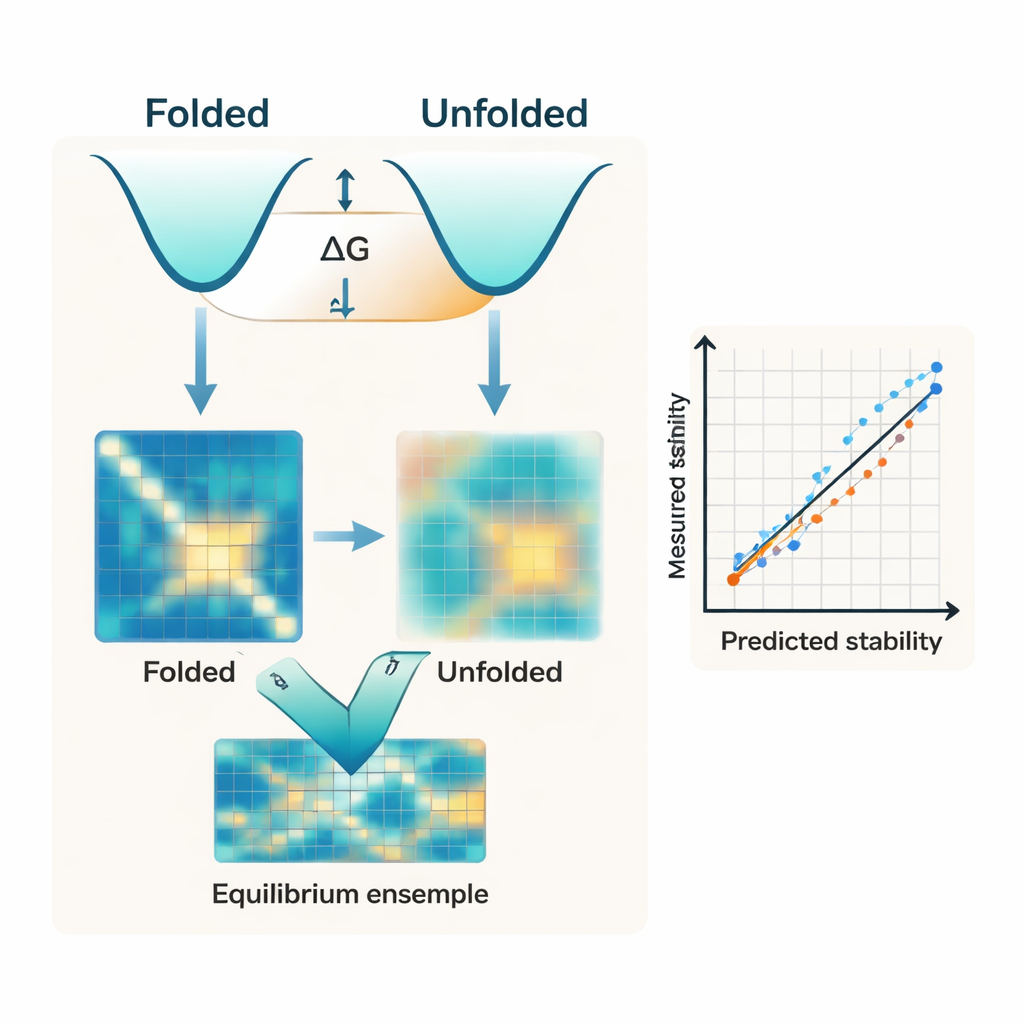
من مقعد التصميم إلى الاختبارات الواقعية
لمعرفة ما إذا كان IFUM يمكن أن يوجّه هندسة البروتين الحقيقية، يطبّقه المؤلفون على ثلاث مشكلات تصميم صعبة: تثبيت بروتينات الإنترفيرون‑لامبدا، إعادة تشكيل بروتين الإشارة المناعية IL‑10، وتحسين إنزيم معدل للسكريات يُسمى UGT76G1. في كل الحالات الثلاث، تتتبع استقراريات IFUM المتنبأ بها جيداً درجات الانصهار المقاسة، والتي تشير إلى مدى تحمل البروتين للحرارة قبل الانفتاح. كما يساعد النموذج في فحص مئات البروتينات المصممة حاسوبياً لاختيار تلك الأرجح في الطي والبقاء قابلة للذوبان داخل الخلايا، متفوقاً على مقاييس الثقة الشائعة المستخدمة في شبكات التنبؤ بالبنية. تشير هذه النتائج إلى أن IFUM يمكن استخدامه كـ «مرشح استقرار» عملي إلى جوار فحوصات قائمة على البنية في سير عمل تصميم البروتين الحديثة.
الحدود والاتجاهات المستقبلية
مثل أي نموذج، لدى IFUM حدود. تم تدريبه أساساً على بروتينات قصيرة ذات سلسلة مفردة وقابلة للذوبان، وتصبح قيم الاستقرار المطلقة أقل موثوقية مع البروتينات الأكبر بكثير أو تلك ذات الحلقات المرنة الطويلة أو المناطق العابرة للغشاء. ولا يزال وصفه للحالة غير المطوية نموذجاً إحصائياً مبسّطاً بدلاً من صورة واقعية كاملة لكل الأشكال الممكنة. ومع ذلك، يبيّن النهج أن تعليم الذكاء الاصطناعي للنظر في كل من التجمعين المطوي وغير المطوي يؤدي إلى تقديرات استقرار أكثر موثوقية. للمستخدمين غير المتخصصين، الخلاصة الأساسية هي أن IFUM يقربنا أكثر من القدرة على سؤال الحاسوب، بثقة كمية، «هل هذا التصميم البروتيني سيثبت فعلاً؟»، ما قد يسرّع تطوير أدوية حيوية أكثر أماناً وإنزيمات صناعية أكثر متانة.
الاستشهاد: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
الكلمات المفتاحية: استقرار البروتين, طي البروتين, التعلّم العميق, تصميم البروتين, طفرات