Clear Sky Science · ar
روبوتات نانوية متخفية تستهدف وتنظم أنماط التراسل بين العضيات داخل البلاعم لتعزيز تجدد الأعصاب
لماذا تهم المساعدات الصغيرة "المتخفية" في إصابات الحبل الشوكي
غالبًا ما تعني إصابة الحبل الشوكي شللًا مدى الحياة لأن نسيج الأعصاب التالف من الصعب جدًا إصلاحه. سبب رئيسي هو أن موقع الإصابة يتحول إلى منطقة معادية مليئة بالالتهاب والإجهاد الخلوي الذي يعيق الشفاء. تصف هذه الدراسة نوعًا جديدًا من الروبوتات النانوية المتخفية التي تسافر عبر مجرى الدم، تتسلل عبر دفاعات الجسم، وتعيد برمجة الخلايا المناعية في موقع الإصابة لتحول وضعها من النمط الهجومي إلى نمط الإصلاح، مما يساعد على نمو الأعصاب لدى الحيوانات المصابة بالحبل الشوكي.
المشكلة: التهاب لا ينطفئ
بعد إصابة الحبل الشوكي، تأتي موجة الضرر الأولى من الصدمة الفيزيائية نفسها. لكن موجة ثانية أبطأ تقودها الالتهابات وجزيئات سامة تُدعى أنواع الأكسجين التفاعلية وموت واسع للخلايا. تتدافع خلايا مناعية تُعرف بالبلاعم لتنظيف الحطام. في المراحل المبكرة، تتبنى حالة "M1" العدوانية التي تقتل الممرضات والخلايا التالفة لكنها أيضًا تطلق إشارات التهابية قاسية. لكي يبدأ الشفاء الحقيقي، يجب أن تنتقل هذه الخلايا لاحقًا إلى حالة مهدئة "M2" تدعم إصلاح الأنسجة ونمو الأوعية الدموية وتجدد الأعصاب. ولسوء الحظ، فإن الإجهاد الشديد داخل النسيج المصاب يمكن أن يحبس البلاعم في حالة M1 الضارة، مما يرسخ دورة من الالتهاب المزمن التي تمنع الاستفاء الوظيفي.
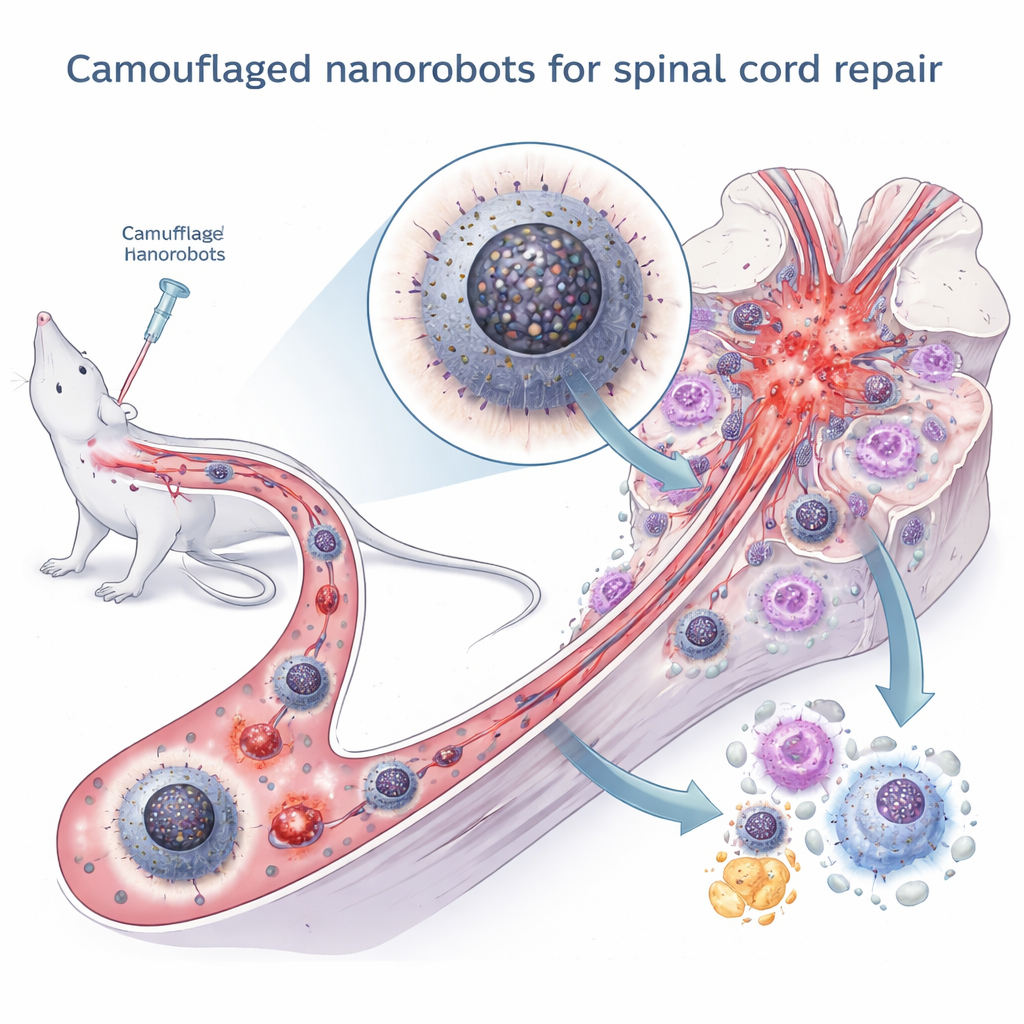
حوار مخفي بين أجزاء الخلية
ركز المؤلفون على "حوار" داخلي دقيق لكنه حاسم داخل البلاعم: التراسل بين مقصودين رئيسيين، الشبكة الإندوبلازمية (التي تساعد على طي البروتينات وتخزن الكالسيوم) والميتوكوندريا (محطات طاقة الخلية). في الظروف الطبيعية، تتشارك هياكل كهذه كميات صغيرة من أيونات الكالسيوم عبر مناطق اتصال متخصصة، ما يساعد على مواءمة إنتاج الطاقة مع احتياجات الخلية. بعد الإصابة، تتسبب أنواع الأكسجين التفاعلية الزائدة في طي خاطئ للبروتينات وإجهاد في الشبكة الإندوبلازمية. هذا الإجهاد يدفع بدوره إلى نقل مفرط للكالسيوم إلى الميتوكوندريا، ما يؤدي إلى انهيار الطاقة، ومزيد من الجزيئات السامة، وتسرب الحمض النووي للميتواكوندريا إلى سائِل الخلية. هذا الحمض النووي الهارب يُفعل مسار إنذار قوي يُسمى cGAS–STING–NFκB، الذي يقفل البلاعم أكثر في حالة الالتهاب M1.
تصميم روبوت نانوي متخفٍ
لكسر هذه الدورة الخبيثة، بنى الفريق روبوتًا نانويًا متعدد الطبقات سموه BP@D/N. في نواته نقاط كمومية من الفسفور الأسود، جزيئات دقيقة ذات نشاط مضاد للأكسدة ومضاد للالتهاب قوي لكنها ضعيفة الاستقرار في الجسم. تُحشى هذه النقاط داخل غلاف أجوف من البوليدوبامين، مادة متوافقة حيويًا تحميها من التفكك المبكر وتضيف خصائصها المضادة للأكسدة. أخيرًا، يُلف الجسيم بأكمله بغشاء مأخوذ من العدلات المنشَّطة، وهو نوع من خلايا الدم البيضاء يجذبها موقع الالتهاب بشكل طبيعي. هذه "الرداءة" تمكّن الروبوت النانوي من تجنب الإزالة المناعية، تتبُّع إشارات الالتهاب إلى الحبل الشوكي المصاب، والالتصاق بالبلاعم لامتصاص فعال.
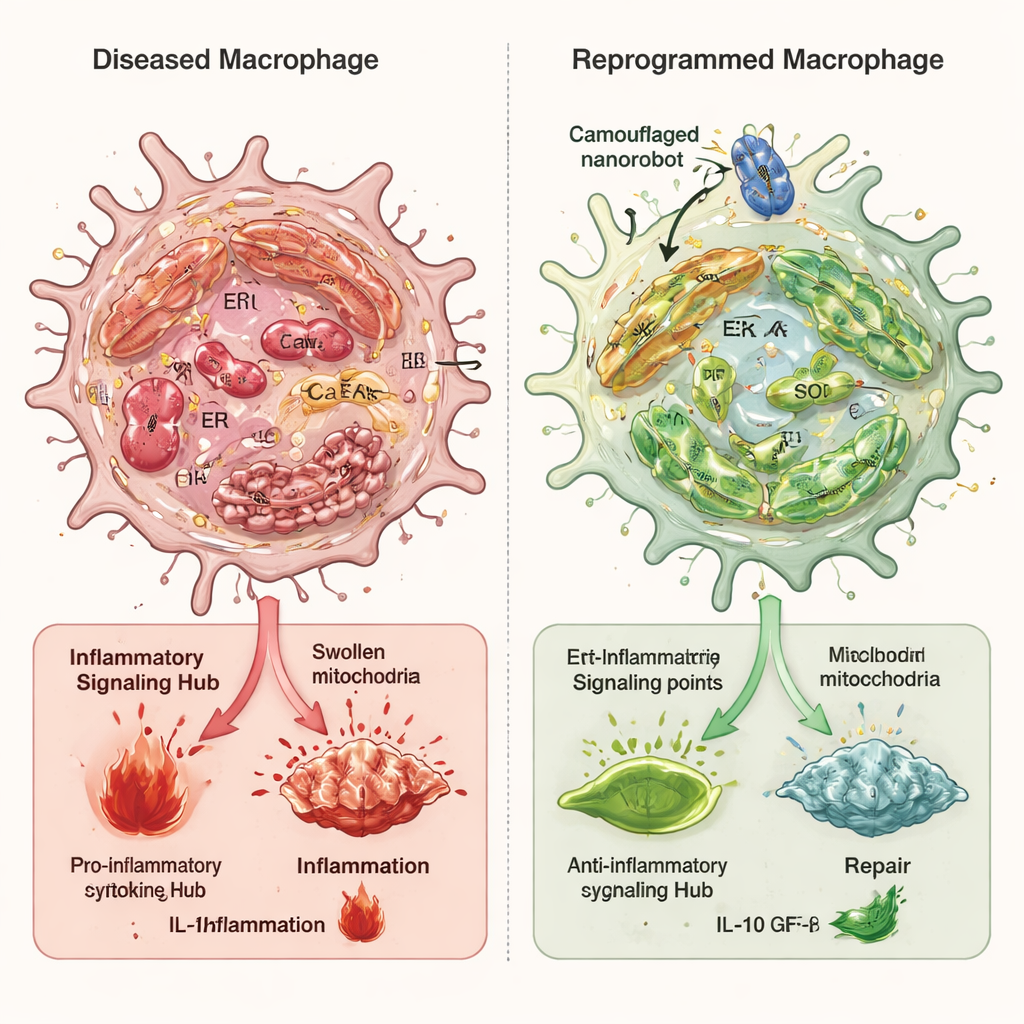
إعادة توصيل الخلايا المناعية المتعبة
في دراسات خلوية، أظهرت البلاعم المعرضة لمحفزات التهابية مستويات عالية من إجهاد الشبكة الإندوبلازمية، وميتوكوندريا متورمة ومتضررة، وحمل زائد من الكالسيوم، وتفعيل قوي لمسار الإنذار cGAS–STING–NFκB. عند المعالجة بالروبوتات النانوية المتخفية، انخفض الإجهاد التأكسدي الكلي بشدة، وأصبحت الأغشية الداخلية بين الشبكة الإندوبلازمية والميتوكوندريا أقل ترابطًا مفرطًا، وعاد كالسيوم الميتوكوندريا إلى القرب من المعدلات الطبيعية. منع ذلك تسرب الحمض النووي الميتوكوندري إلى سائِل الخلية وخفّف من شدة شلال الإشارات الالتهابية. لاعب رئيسي في هذه العملية كان إنزيم يُدعى Ero1α، الذي يساعد في التحكم بالبيئة الأكسدية وإطلاق الكالسيوم من الشبكة الإندوبلازمية. خفّضت الروبوتات النانوية نشاط Ero1α، وعندما عزز الباحثون نشاط Ero1α اصطناعيًا ألغى ذلك إلى حد كبير فوائد الروبوت النانوي، مما أكد دوره المركزي.
من تهدئة الالتهاب إلى إعادة نمو الأعصاب
قلبت هذه التغيرات الداخلية البلاعم من حالة M1 المدمّرة إلى حالة M2 الشافية. في الأطباق، أفرزت الخلايا المنحازة نحو M2 جزيئات التهابية أقل مثل TNF-α وIL-6، ومزيدًا من عوامل النمو التي تشجع خلايا الأعصاب والخلايا الداعمة على النمو وتمديد المحاور العصبية. في نماذج الفئران المصابة بالحبل الشوكي، أدى الحقن المتكرر للروبوتات النانوية إلى إشارات مناعية ضارة أقل عند الآفة، وتندب أقل، وتشكّل تجاويف أصغر، والمزيد من الألياف العصبية المتجددة. استعدت الحيوانات التي تلقت الروبوتات النانوية المتخفية حركة أطراف خلفية أفضل، واستجابات عضلية أقوى، وتحسّنًا في بنية المثانة مقارنة بالحيوانات غير المعالجة أو تلك التي عولجت بجسيمات نانوية أقل استهدافًا.
ماذا قد يعني ذلك للمرضى في المستقبل
تظهر هذه الدراسة أن ضبط الإجهاد الداخلي والتواصل بين مقصورات الخلية بدقة يمكن أن يحول الخلايا المناعية من إلحاق الضرر إلى مساعدة الأعصاب التالفة. من خلال تعبئة جزيئات مضادة للأكسدة قوية لكنها هشة داخل روبوت نانوي متخفٍ ومستهدف، استعاد الباحثون توازنًا أكثر صحة بين الالتهاب والإصلاح في الحبل الشوكي المصاب لدى الفئران. وبينما لا يزال العمل كثيرًا قبل أن يُختبر هذا النهج في البشر، فإنه يقدم مخططًا واعدًا: بدلاً من قمع الالتهاب بشكل واسع، قد توجه العلاجات المستقبلية آليات خلوية محددة داخل البلاعم لتهيئة بيئة أكثر ترحيبًا لتجدد الأعصاب بعد إصابة الحبل الشوكي.
الاستشهاد: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
الكلمات المفتاحية: إصابة الحبل الشوكي, روبوتات نانوية, البلاعم, تجدد الأعصاب, الطب النانوي