Clear Sky Science · ar
تعديل مستويات Nudt21 يكشف أدوارًا معتمدة على الجرعة للتعددية في التحاد الذيل أثناء تجدد الأنسجة
كيف تحافظ الخلايا على شباب أنسجتنا
أجسامنا تصلح نفسها باستمرار. الخلايا الجذعية المختبئة في الجلد والأمعاء ونخاع العظام والعضلات تحل محل الخلايا البالية بهدوء، فتبقي الأنسجة صحية. تستكشف هذه الورقة طبقة تحكم غير مرئية داخل هذه الخلايا الجذعية — كيفية إنهاك رسائل الحمض النووي الريبوزي (RNA) — وتبين أن تغيّرات صغيرة في هذه العملية يمكن أن تقرر ما إذا كانت الأنسجة ستتجدد بسلاسة أو تتعثر أو تفشل. 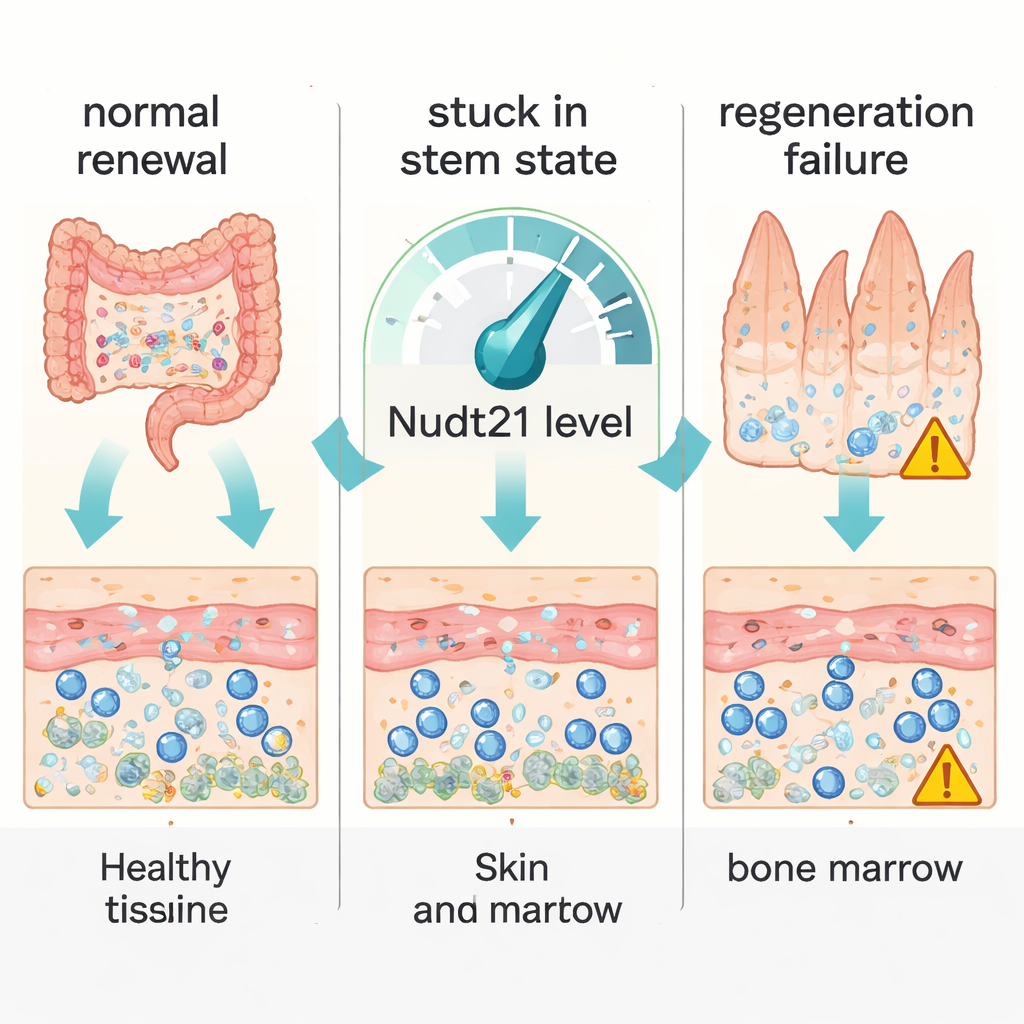
قص ذيول الرسائل الجينية
كل جين يُفعّل في الخلية يُنسخ أولاً إلى رسالة RNA. قبل أن تُستخدم هذه الرسالة لصنع بروتين، يُضاف إلى نهايتها ذيل كيميائي، وهي عملية تسمى التحاد/إضافة ذيل الأدينيل (polyadenylation). لدى العديد من الجينات أكثر من موقع قطع ممكن، لذا يمكن أن تنتهي نفس الرسالة بمنطقة ذيل أطول أو أقصر. تُعرف هذه المناطق الطرفية، 3’UTRs، بأنها لا تشفر بروتينًا لكنها تعمل كمواقع ارتكاز لمنظمات أخرى، بما في ذلك الميكرو RNA التي تضبط بدقة مقدار البروتين المصنوع. يساعد البروتين Nudt21 الخلية على اختيار مكان القطع، وبالتالي يحدد طول هذه الذيول RNA.
مقبض تحكم واحد بتأثيرين مختلفين جدًا
قمع الباحثون هندسيًا فئرانًا يمكن خفض مستوى Nudt21 فيها أو إيقافه تمامًا في الأنسجة البالغة. عندما أُزيل Nudt21 بالكامل في أنحاء الجسم، مرضت الحيوانات بسرعة وماتت، لكن ليس لأن أعضاء «ثابتة» مثل القلب أو الكلى فشلت. بل فقدت الأنسجة عالية الدوران — مثل بطانة الأمعاء والمريء، وجهاز تكون الدم في نخاع العظم، وخلايا العضلات الجذعية المسماة الخلايا الساتلية — قدرتها على التجدد. توقفت الخلايا الجذعية والخلايا السلفية في هذه الأنسجة عن التقدم في دورة الخلية، وفشلت في نسخ حمضها النووي والانقسام. بالمقابل، عندما نُخفضت مستويات Nudt21 جزئيًا فقط، بقيت الخلايا الجذعية قادرة على التكاثر لكنها لم تعد تنضج بشكل صحيح إلى خلايا متخصصة، مما كشف أن التجدد الذاتي والتمايز يستجيبان إلى عتبات جرعة مختلفة لنفس عامل التحكم.
رسائل مقصرة تتملص من المكابح التي تمنع التمايز
لرؤية ما تغير داخل الخلايا، رسم الفريق خريطة لمواضع قطع رسائل RNA وكيف تغيرت مستويات البروتين. مع انخفاض معتدل في Nudt21، تحولت حوالي ألف رسالة RNA من ذيول أطول إلى أقصر. وبما أن العديد من المقاطع المفقودة كانت تحمل مواقع ارتباط للميكرو RNA، أصبحت هذه الرسائل المختصرة أصعب على الصمت. تُنتج مكونات رئيسية منظمة لهوية الخلايا والتطور، بما في ذلك إنزيمات تعيد تشكيل حزم الحمض النووي ومواصلات بروتينية، بكميات مفرطة. أخل هذا الإفراط في الإنتاج بشبكات RNA التنافسية الحساسة التي تشترك فيها العديد من الرسائل مع نفس منظمي الميكرو RNA. النتيجة الصافية كانت أن الخلايا الجذعية حُبست في حالة غير ناضجة: احتفظت بعلاماتها الجذعية لكنها فشلت في تشغيل الجينات اللازمة للتمايز الكامل، حتى عند تعرضها لإشارات قوية تحفز التمايز.
عندما تنهار آلات الخلية
كان لفقدان Nudt21 تمامًا نتيجة أشد وغير متوقعة. بالإضافة إلى حاجز التمايز، اكتسبت العديد من الرسائل التي تُشفّر أجزاء من آلات بروتينية متعددة المكونات ذيولًا مقصرة. هذه الرسائل، على النقيض من ذلك، كانت تميل إلى إنتاج بروتين أقل، لا أكثر. المثال الأبرز كان مركب المسام النووية، البوابة الكبيرة التي تعبر الغشاء النووي وتسمح لخيوط RNA بالخروج من النواة. أظهر ما يقرب من نصف لبنات بناء المسام تغيّرًا في أطوال الذيول وتناقصًا في الوفرة، مما تسبب في اختفاء المسام من السطح النووي، وتراكم RNA داخل النواة، وظهور علامات تلف الحمض النووي. عبر حذف المنطقة ذات الذيل الطويل لمكون وحيد من المسام، Nup160، استطاع الباحثون تقليد كثير من آثار فقدان Nudt21 الكامل: أصبحت المسام غير مستقرة، وانكسرت المادة الوراثية أثناء انقسام الخلايا، وتوقفت الخلايا الجذعية عن التجدد. شوهدت اضطرابات مماثلة في مركبات حيوية أخرى مشاركة في تصنيع البروتين ومعالجة RNA، مما يشير إلى أن اختيار الذيل الصحيح يساعد على تنسيق كيفية تجميع هذه الآلات الكبيرة.
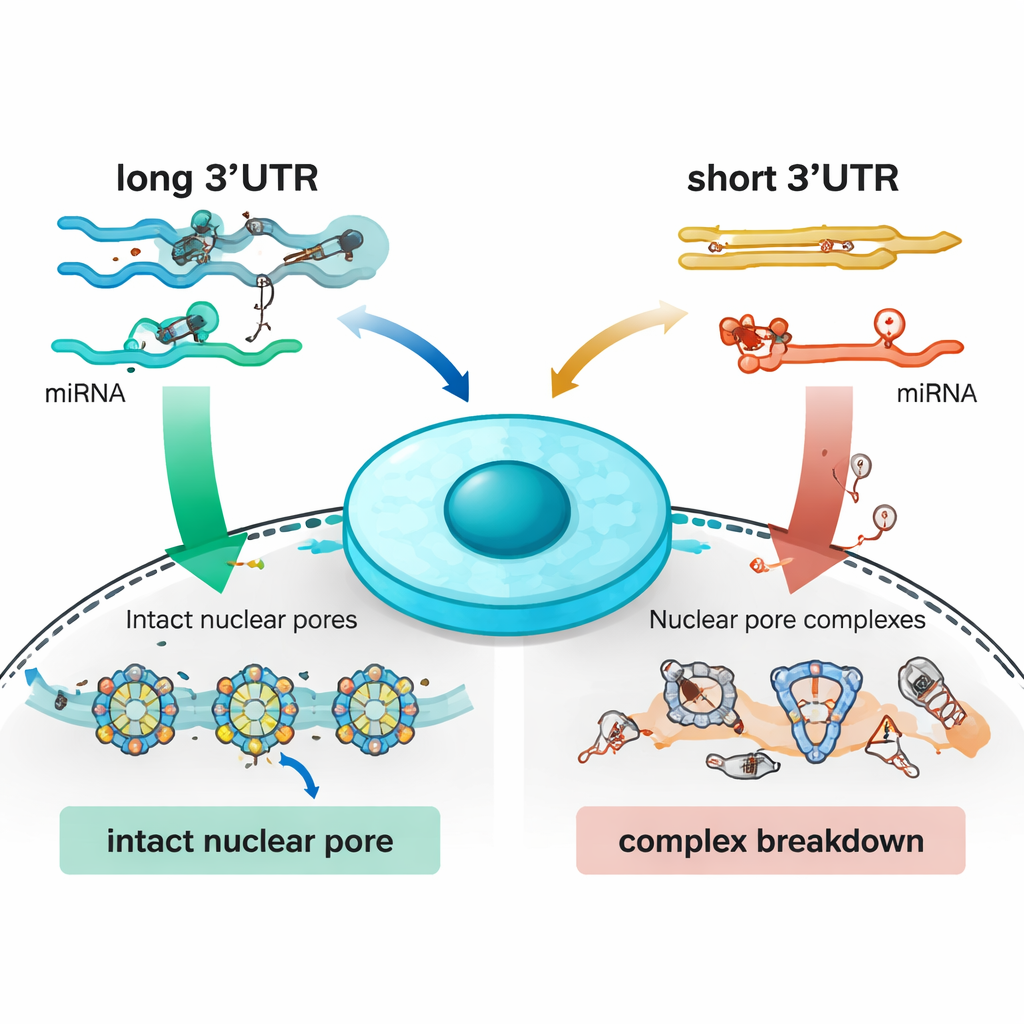
لماذا يهم هذا للصحة والشيخوخة والسرطان
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن إصلاح النسيج المدفوع بالخلايا الجذعية لا يعتمد فقط على أي الجينات تُشغّل أو تُطفأ، بل أيضًا على الكيفية الدقيقة التي تُنهى بها رسائل RNA الخاصة بها. يعمل Nudt21 كمُعدِّل رئيسي حساس للجرعة لهذه الخطوة الختامية. خفضه قليلًا يسمح للخلايا الجذعية بالاستمرار في الانقسام لكنه يحصرها في حالة غير ناضجة يصعب تمايزها — وضع قد يشبه بعض أنواع السرطانات العدوانية. خفضه بدرجة أكبر يتسبب في تفكك آلات خلوية أساسية، مثل المسام النووية، مما يؤدي إلى تلف الحمض النووي وفقدان القدرة التجديدية. فهم هذه الآلية الخاصة بقطع ذيول RNA والتحكم بها قد يفتح سبلًا جديدة لتعزيز تجدد الأنسجة، وحماية ثبات الجينوم أثناء الشيخوخة، أو دفع خلايا السرطان انتقائيًا نحو توقف قاتل.
الاستشهاد: Tsopoulidis, N., Yagi, M., Brumbaugh, J. et al. Modulation of Nudt21 levels reveals dose-dependent roles of alternative polyadenylation in tissue regeneration. Nat Commun 17, 2005 (2026). https://doi.org/10.1038/s41467-026-68630-x
الكلمات المفتاحية: الخلايا الجذعية, تجدد النسيج, معالجة الحمض النووي الريبوزي, مركب المسام النووية, التحاد البديل للذيل (polyadenylation)