Clear Sky Science · ar
H3K9me2 الذي يتوسّطه G9a ينظّم تجدد الظهارة المعوية عبر الصمت اللاجيني لجينات دورة الخلية
لماذا يهمّ الإصلاح الذاتي للأمعاء
يواجه الغشاء المبطن للأمعاء يومياً ظروفاً قاسية: حمض المعدة، وجزيئات الطعام، وتريليونات من الميكروبات. ومع ذلك، لا ينجو هذا النسيج فحسب، بل يصلحه باستمرار. عندما يتعطل نظام الإصلاح هذا — بعد العلاج الإشعاعي، في داء الأمعاء الالتهابي، أو أثناء العدوى الشديدة — قد يعاني المرضى من ألم، ونزف، ومضاعفات مهددة للحياة. تكشف هذه الدراسة عن "مفتاح" مخفي داخل خلايا الأمعاء يساعدها على تقرير متى تتوقف عن الراحة وتبدأ في إعادة البناء، موفّراً دلائل لعلاجات جديدة قد تعزّز طاقم الإصلاح الطبيعي للأمعاء.
بنية رقيقة تحت ضغط دائم
تبدو السطح الداخلي للأمعاء تحت المجهر كأنها سجادة كثيفة، مع زغبات إصبعية الشكل تمتص المغذيات وجيوب تُدعى القُرُون حيث تعيش الخلايا الجذعية. يجب أن تجد هذه الخلايا الجذعية وبناتها سريعة الانقسام توازناً بين التجدد المستمر والإصلاح الطارئ. ركّز المؤلفون على كيفية تأثير العلامات الكيميائية على بروتينات تغليف الحمض النووي، المسماة هستونات، على هذا التوازن. هذه العلامات لا تغيّر الجينات نفسها، بل تعمل أشبه بمفاتيح تعتيم، ترفع أو تخفّض نشاط مجموعات من الجينات بينما تنتقل الأمعاء من الحالة الطبيعية إلى الإصابة ثم العودة إلى الصحة.
علامة فوق جينية تواكب الضرر والشفاء
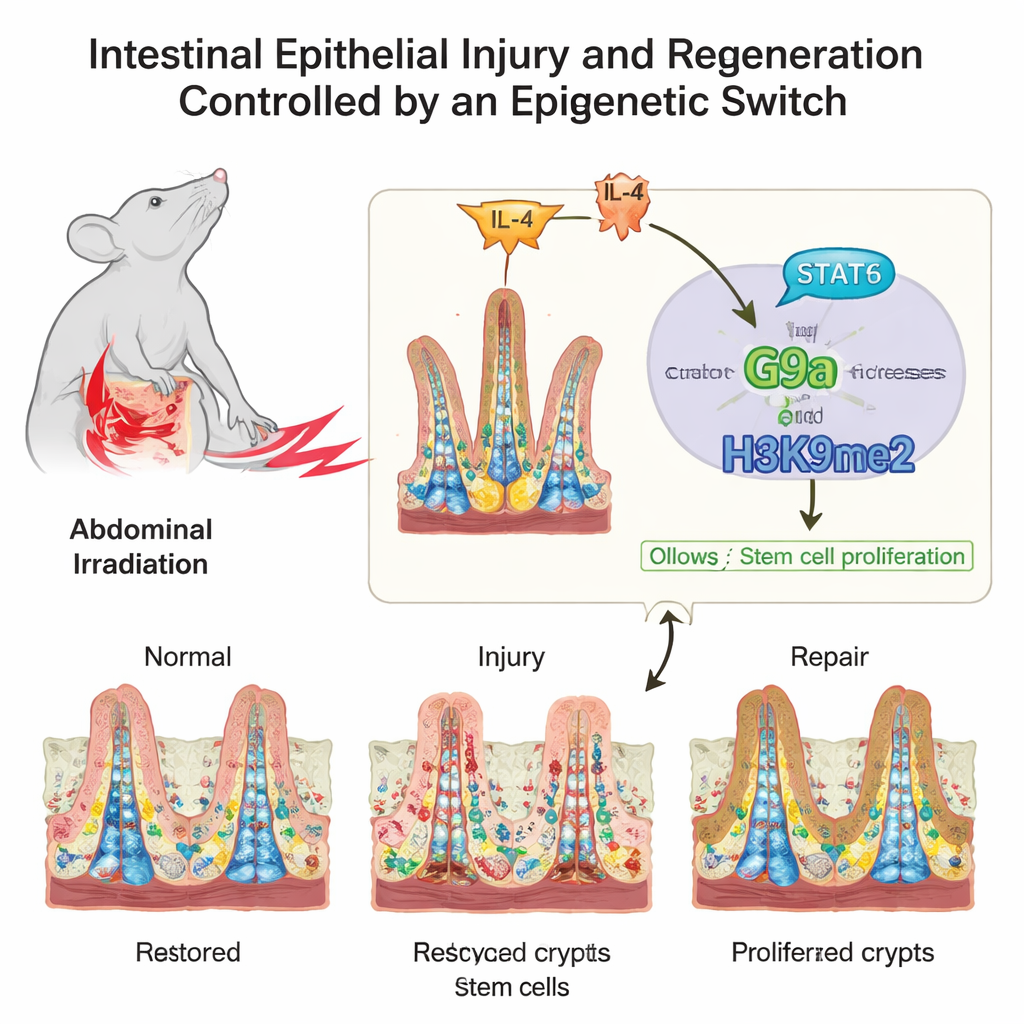
باستخدام فئران تعرّضت للإشعاع — وهو سبب شائع لإصابة الأمعاء أثناء علاج السرطان — فحص الباحثون العديد من علامات الهستون في القُرُون الغنية بالخلايا الجذعية. علامة واحدة، تُعرف باسم H3K9me2، ارتفعت بشكل حاد عندما انتقلت الأمعاء من حالة الإصابة إلى حالة الإصلاح. وتتبع أنزيم كاتب هذه العلامة، بروتين يدعى G9a، نفس النمط. ثم فحص الفريق عينات بشرية من مرضى تلقوا علاجاً إشعاعياً للحوض، وكذلك أشخاصاً مصابين بداء كرون. في كلتا الحالتين، ارتبطت مستويات أعلى من H3K9me2 وG9a في خلايا الأمعاء بعلامات أفضل على إصلاح النسيج، مما يشير إلى أن هذا النظام محفوظ بين الفئران والبشر.
عندما ينكسر مفتاح الإصلاح
لاختبار ما إذا كانت هذه العلامة مجرد مشاهد أم تقود الشفاء فعلاً، أزال العلماء G9a محدداً من بطانة الأمعاء لدى الفئران، أو عطلوا نشاطه بدواء. في الحالتين هبطت مستويات H3K9me2. بعد التعرض للإشعاع أو الإصابة الكيميائية، فقدت هذه الفئران مزيداً من الوزن، وكان لديها أمعاء أقصر وأكثر تلفاً، وأظهرت قُرُوناً متجددة وخلايا جذعية أقل مقارنةً بالحيوانات الطبيعية. حتى من دون أي إصابة متعمدة، بدا بطانة أمعاء الفئران ناقصة G9a قزمة: كانت القُرُون أضحل، والزغبات أقصر، وانخفضت أعداد الخلايا الجذعية وسلالاتها المتمايزة. كما نمت "الأمعاء المصغرة" الصغيرة المزروعة من هذه الخلايا في المختبر بشكل سيئ، ما يبرز أن هذا النظام الجزيئي محوري للتجدد اليومي للأمعاء.
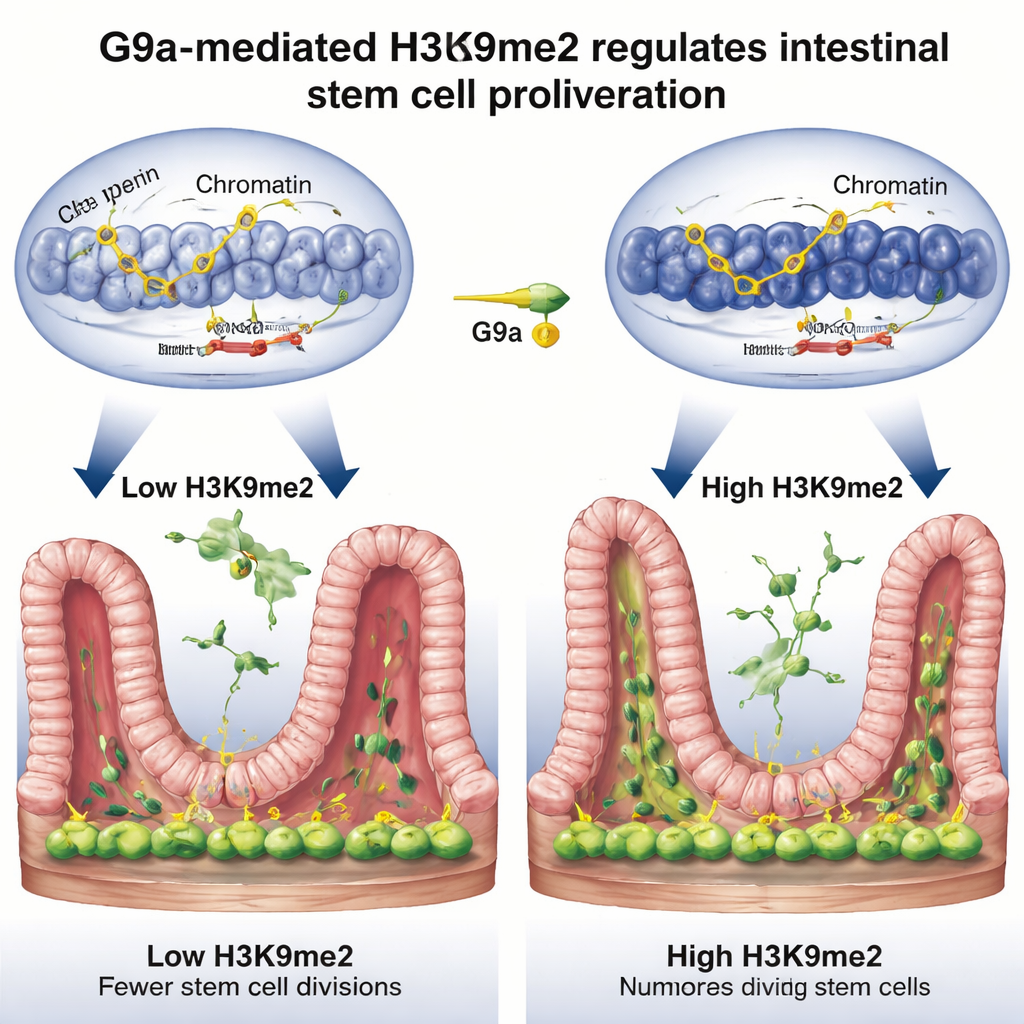
إطلاق المكابح على انقسام الخلايا
بتعمق أكثر، سأل الفريق أي الجينات تُسيطر عليها هذه المفتاح. من خلال دمج ثلاث طرق جينومية قوية على مستوى الجينوم، وجدوا أن H3K9me2، الموضوعة بواسطة G9a، تميل إلى التمركز على مقاطع من الحمض النووي تعمل عادةً كمكابح لدورة الخلية — جينات مثل Rb1cc1 وRb1 وCdkn1a وPten، التي تبطئ أو توقف انقسام الخلايا. عندما غاب G9a، اختفت العلامة الكيميائية من هذه المناطق، وفتحت الحمض النووي المحيط، وارتفع نشاط هذه الجينات المكبحية، مما أدى إلى تباطؤ تكاثر الخلايا الجذعية. أثناء الإصلاح الطبيعي بعد الإصابة، ارتفعت مستويات H3K9me2 عند هذه الجينات، وانخفضت نشاطاتها، وأصبحت الخلايا الجذعية أكثر حرية في الانقسام وإعادة بناء البطانة. جوهرياً، يهدئ G9a وH3K9me2 مؤقتاً إشارات "التوقف" لكي يتمكن النسيج من النمو مجدداً.
سلسلة إشارية من الإشارات المناعية إلى الإصلاح
لا تعمل الأمعاء بمفردها؛ بل تستمع باستمرار إلى إشارات من الجهاز المناعي. تتبّع الباحثون إحدى هذه الإشارات صعودياً نحو G9a. بعد الإصابة، ارتفعت مستويات رسول مناعي يُدعى IL‑4، وهو ما أدى إلى تفعيل بروتين يسمى STAT6 داخل خلايا الأمعاء. ربط STAT6 المنشّط مباشرة بمنطقة التحكم في جين G9a، معزّزاً إنتاجه. خلق ذلك سلسلة قيادة: IL‑4 تفعّل STAT6، وSTAT6 يرفع مستوى G9a، وG9a يضيف H3K9me2 لصمت جينات مكابح دورة الخلية، ما يتيح للخلايا الجذعية التوسع واستعادة البطانة المتضررة.
ماذا يعني هذا لعلاجات المستقبل
لهذا لغير المتخصص، تظهر النتائج أن إصلاح الأمعاء يوجّه ليس فقط بواسطة الجينات، بل بواسطة علامات كيميائية قابلة للعكس تضبط بدقة توقيت استخدام تلك الجينات. يعمل مسار IL‑4–STAT6–G9a–H3K9me2 كشاشة تحكم داخلية تُرخّص مكابح انقسام الخلايا الجذعية لفترة كافية للشفاء، ثم يمكن إعادة ضبطها. في المستقبل، قد تساعد علاجات تعزّز هذا المسار بلطف — مثل أدوية أو أدوات جينية ترفع مستويات G9a في الوقت والمكان المناسبين — المرضى على التعافي أسرع من إصابات الإشعاع، أو نوبات داء الأمعاء الالتهابي، أو حالات أخرى تضر بطانة الأمعاء، مع تقليل مخاطر النمو الخلوي غير المنضبط.
الاستشهاد: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
الكلمات المفتاحية: تجدد الأمعاء, علم التخلق فوق الجيني, الخلايا الجذعية, مثيلة الهستون, داء الأمعاء الالتهابي