Clear Sky Science · ar
توقيع ديناميكي لتبادل النشاط والثبات في تطور لاكتاماز
لماذا هذا مهم لمقاومة المضادات الحيوية
غالبًا ما تبدو مقاومة المضادات الحيوية كصندوق أسود: البكتيريا "بطريقة ما" تتغير وتتوقف الأدوية عن العمل. تفتح هذه الدراسة ذلك الصندوق لإحدى أشهر إنزيمات المقاومة في العالم، TEM‑1 β‑lactamase، الذي يساعد البكتيريا على تدمير المضادات الحيوية الشبيهة بالبنيسيلين. من خلال مراقبة كيف تتغير بنية وحركات هذا الإنزيم أثناء تطوره لمهاجمة أدوية أحدث، يكشف المؤلفون لماذا تؤدي الطفرات التي تعزز النشاط غالبًا إلى إضعاف الثبات، وكيف تجد التطورات طرقًا ذكية لموازنة الأمرين.
من مقاتل البنيسيلين إلى مكسّر أدوية أوسع
كان TEM‑1 في الأصل متفوقًا على تفكيك مضادات البنيسيلين القديمة لكنه ضعيف في مواجهة أدوية أحدث وأكبر حجمًا مثل سيفوتاكسيم. في العديد من السلالات السريرية، تظهر طفرة مفصلية واحدة تسمى G238S بالقرب من الموقع النشط للإنزيم، الجيب الذي تُقطع فيه المضادات الحيوية. تحسّن هذه الطفرة بشكل كبير قدرة الإنزيم على تحطيم سيفوتاكسيم، مع إحداث ضرر طفيف فقط في وظيفته الأصلية في تفكيك البنيسيلين. يوضح المؤلفون أن G238S لا تقوم ببساطة بتوسيع الجيب؛ بل تعيد تنظيم كيفية حركة عدة حلقات ولفائف مجاورة وملفات حلزونية، فتنشئ تشكّلًا وظيفيًا جديدًا يتسع بشكل أفضل للأدوية الكبيرة.
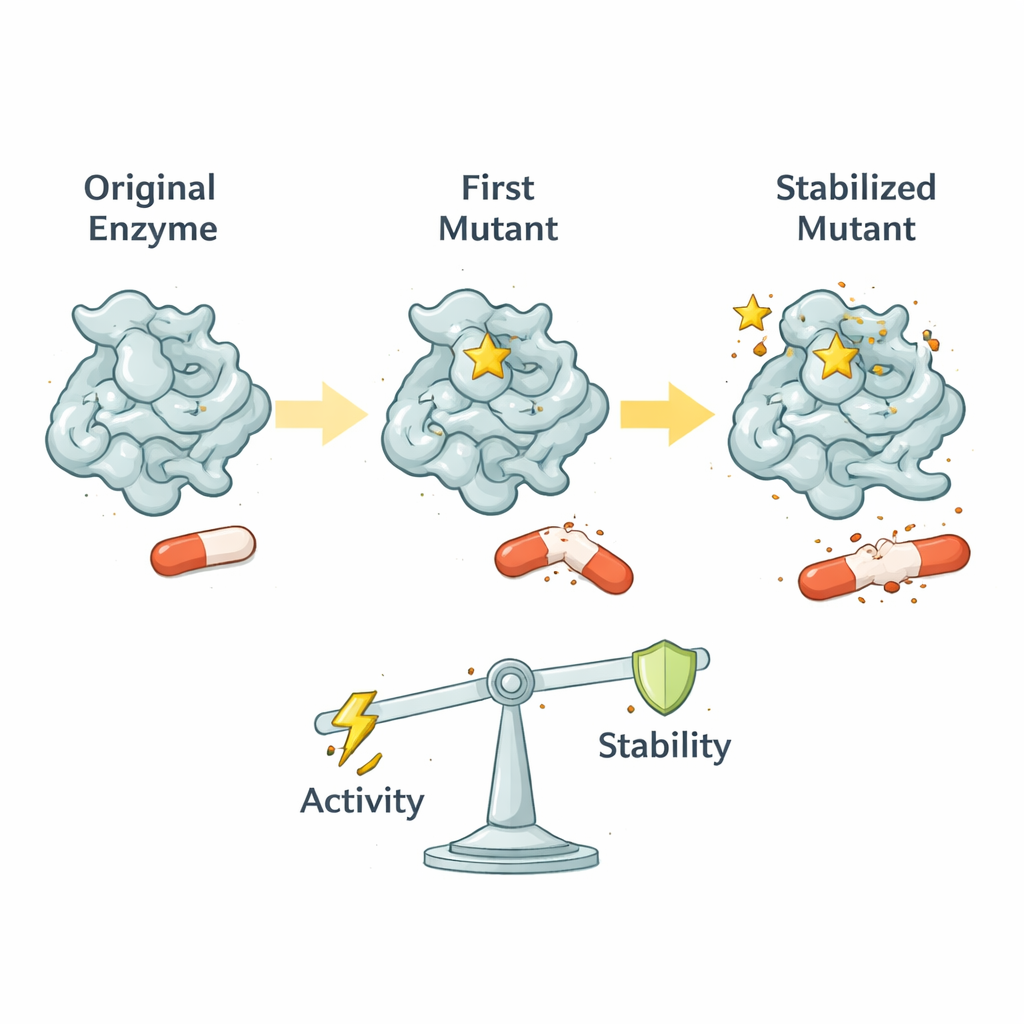
حركة البروتين كمِقْبَض ضبط تطوري
باستخدام تقنيات مطورة من الرنين المغناطيسي النووي (NMR)، قاس الباحثون كيف تتحرك أجزاء مختلفة من TEM‑1 عبر أزمنة تمتد من تريليونيات إلى ألفيات الثانية. النوع البري من TEM‑1 صلب جدًا، ما يساعده على معالجة ركائزه الأصلية بكفاءة. تُبقي G238S معظم هذه الصلابة السريعة على حالها لكنها تُدخل حركات أبطأ ومضبوطة بعناية في العديد من جدران الموقع النشط. هذه الحركات سريعة بما يكفي لمواكبة كيمياء الإنزيم لكنها ليست عشوائية بحيث تعطل بقايا التحفيز الحرجة. النتيجة هي "نافذة مثلى" من المرونة: قدر كافٍ من الحركة لفتح الجيب أمام سيفوتاكسيم، مع الحفاظ على محاذاة آلية الكيمياء الأساسية.
موازنة شكلين بدلًا من اختيار واحد
التطور لا يجمد TEM‑1 في شكل جديد واحد. بدلًا من ذلك، يُجرب الإنزيم على الأقل شكلين رئيسيين: حالة "بنيسيليناز" تشبه البنية الأصلية وحالة أكثر انفتاحًا "سيفوتاكسيماز" تناسب الأدوية الأحدث بشكل أفضل. الطفرات الإضافية التي تظهر لاحقًا، مثل E104K وA42G، تقوم بشيء دقيق. بدلًا من جعل الشكل الجديد المواتي لسيفوتاكسيم أكثر استقرارًا فحسب، فإنها تعيد توازن مزيج الحالتين. تُظهر بيانات NMR أن أجزاء مختلفة من الموقع النشط والهيكل الداعم يمكن أن تغير توزيعاتها بشكل مستقل على طول هذا الطيف ذي الحالتين. يؤدي هذا إلى مجموعة تركيباتية من متغيرات الإنزيم، لكلٍ منها خليط مختلف من التشكّلات الشبيهة بالبنيسيلين وتلك الشبيهة بالسيفوتاكسيم، ومن ثم ملفات محفزة مختلفة.
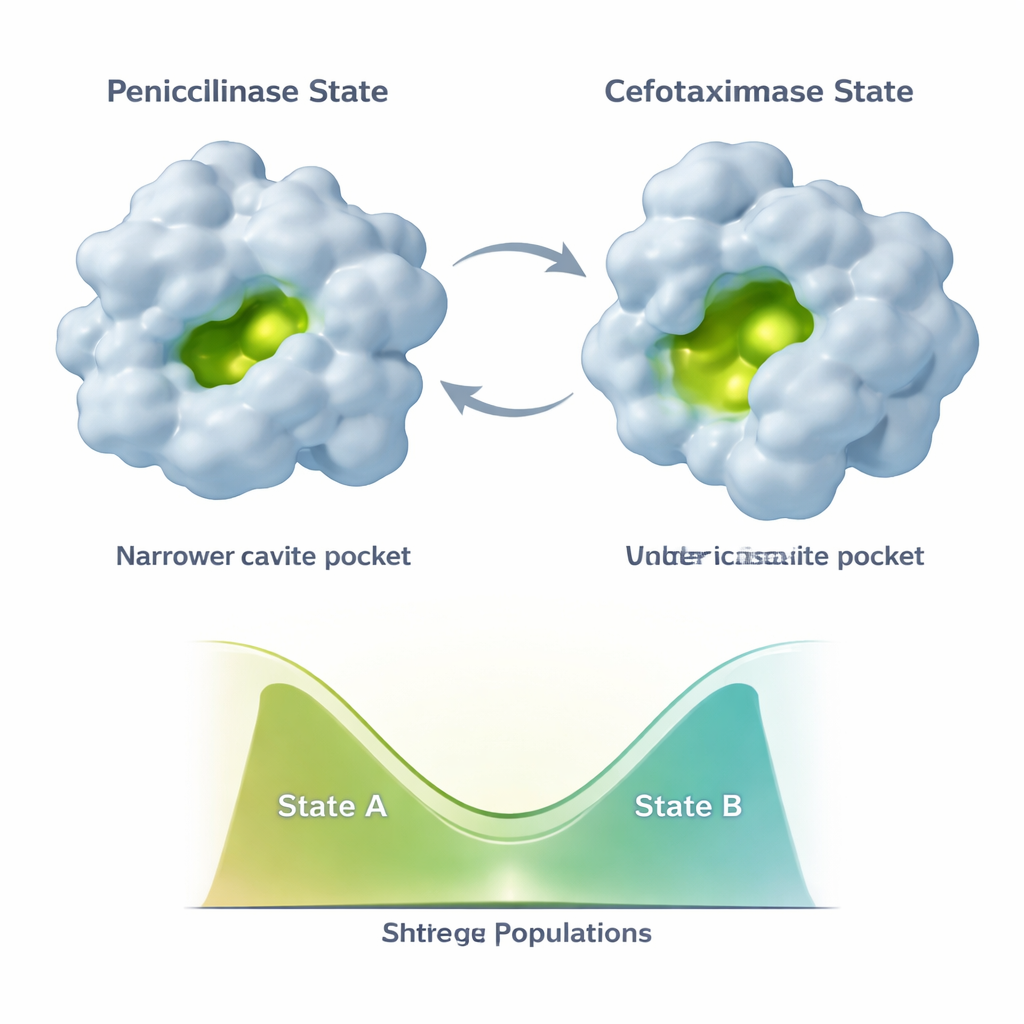
نقاط ضعيفة خفية وإصلاحات بعيدة المدى
غالبًا ما تحمل الطفرات التي تحسّن النشاط تكلفة خفية: إنها تجعل البروتين أقل استقرارًا. بدلًا من النظر فقط إلى الانطياء الكامل، خرّط الفريق الثبات المحلي على مستوى قطع قصيرة باستخدام تبادل الهيدروجين–الديوتيريوم مع مطيافية الكتلة. وُجد أن G238S تُضعف ليس الحلقات القريبة فحسب بل أيضًا الملفات الحلزونية والمناطق الصفائحية البعيدة التي تشكل العمود الفقري الهيكلي. تتداخل بعض هذه المناطق مع جيب علوسترك خفي—فتحة نادرة الظهور في قلب البروتين يمكن أن تربط جزيئات صغيرة وتقلل النشاط. تجعل G238S فتح هذا الجيب أسهل، فتبني فعليًا ميزة تثبيط ذاتي خفيفة في الإنزيم. الطفرات اللاحقة، وخصوصًا A42G، تعزز هذه الشبكة الهيكلية المترهلة، محسنةً الاستقرار المحلي حول ثلاثة ملفات حلزونية متفاعلة من دون إزالة الديناميكيات المفيدة للموقع النشط. بعبارة أخرى، يصلح التطور نقاط الضعف الهيكلية البعيدة بدلًا من التراجع عن الابتكار الأصلي.
ما تكشفه الدراسة عن استراتيجية التطور
بالنسبة للقارئ العام، الرسالة المركزية هي أن بروتينات مثل TEM‑1 لا تطور المقاومة عن طريق قلب مفتاح بسيط إيقاف/تشغيل. كل طفرة تعيد تشكيل كيفية تنفس الإنزيم ومرونه وتقسيم وقته بين أوضاع عمل مختلفة بشكل طفيف. تفتح G238S الباب لوظيفة جديدة—تحطيم مضادات حيوية أحدث—لكنها تخلق أيضًا هشاشة محلية وحالة قيدية ذاتية التثبيط جزئيًا. تعمل الطفرات الثانوية كدعامات مدروسة، مثبتةً السقالة ومضبوطةً التوازن بين الأشكال القديمة والجديدة بحيث يظل الإنزيم نشطًا ومتينًا في آن واحد. يمكن لهذا المنظور الديناميكي على التطور، حيث تهم الحركة والضعف المحلي بقدر البنية الثابتة، أن يوجّه تصميم مضادات حيوية مستقبلية وأدوية تستهدف الإنزيمات تكون أصعب على البكتيريا أن تتغلب عليها.
الاستشهاد: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
الكلمات المفتاحية: مقاومة المضادات الحيوية, بيتا-لاكتاماز, تطور البروتينات, ديناميكيات الإنزيم, ثبات البروتين